
【题目】东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的电子排布式为___,3d能级上的未成对电子数为___。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是___。
②在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为___,提供孤电子对的成键原子是___。
③氨的沸点___(填“高于”或“低于”)膦(PH3),原因是___。
(3)单质铜及镍都是由___键形成的晶体;元素铜与镍的第二电离能分别为ICu=1958kJ·mol-1、INi=1753kJ·mol-1,ICu>INi的原因是___。
(4)某镍白铜合金的立方晶胞结构如图所示。
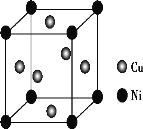
①晶胞中铜原子与镍原子的数量比为___。
【答案】1s22s22p63s23p63d84s2 2 正四面体 配位键 N 高于 氨气分子间有氢键,分子间作用力更强 金属 Cu+的外围电子排布为3d10,Ni+的外围电子排布为3d84s1,Cu+的核外电子排布更稳定,失去第二个电子更难,元素铜的第二电离能高于镍的 3:1
【解析】
(1)Ni元素原子核外电子数为28,核外电子排布式为1s22s22p63s23p63d84s2,3d能级上的未成对电子数为2,
故答案为:1s22s22p63s23p63d84s2;2;
(2)①SO![]() 中S原子的孤电子对数=
中S原子的孤电子对数=![]() =0,价层电子对数=4+0=4,离子空间构型为正四面体,
=0,价层电子对数=4+0=4,离子空间构型为正四面体,
故答案为:正四面体;
②Ni2+提供空轨道,NH3中N原子含有孤电子对,二者之间形成配位键,
故答案为:配位键;N;
③PH3分子之间为范德华力,氨气分子之间形成氢键,分子间作用力更强,增大了物质的沸点,故氨气的沸点高于PH3分子的,
故答案为:高于;氨气分子之间形成氢键,分子间作用力更强;
(3)单质铜及镍都属于金属晶体,都是由金属键形成的晶体;Cu+的外围电子排布为3d10,Ni+的外围电子排布为3d84s1,Cu+的核外电子排布更稳定,失去第二个电子更难,元素铜的第二电离能高于镍的,
故答案为:金属;Cu+的外围电子排布为3d10,Ni+的外围电子排布为3d84s1,Cu+的核外电子排布更稳定,失去第二个电子更难,元素铜的第二电离能高于镍的;
(4)①晶胞中Ni处于顶点,Cu处于面心,则晶胞中Ni原子数目为8×![]() =1、Cu原子数目=6×
=1、Cu原子数目=6×![]() =3,故Cu与Ni原子数目之比为3:1,
=3,故Cu与Ni原子数目之比为3:1,
故答案为:3:1;


科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次增大,X、Y同周期且相邻,Y是地壳中含量最多的元素,Z是短周期中原子半径最大的主族元素,W的单质常温下是一种淡黄色固体。下列叙述正确的是( )
A.元素的非金属性:![]()
B.Z的单质在空气中燃烧生成阴、阳离子个数比为![]() 的氧化物
的氧化物
C.Y的简单气态氢化物的稳定性强于W的
D.工业上一般采用电解对应盐的水溶液制Z单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作及现象能够达到对应实验目的是( )
选项 | 实验操作及现象 | 实验目的 |
A | 向溶液中加入盐酸无现象,再加入氯化钡溶液产生白色沉淀 | 检验溶液中有 |
B | 常温下,向饱和 | 证明常温下, |
C | 常温下,测定盐酸和醋酸溶液的pH:盐酸pH小于醋酸pH | 证明相同条件下,在水中HCl电离程度大于 |
D | 将浓硫酸与碳混合加热,直接将生成的气体通入足量的澄清石灰水,石灰水变浑浊 | 检验气体产物中 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,某同学设计了一个燃料电池并探究氯碱工业原理的相关问题,其中乙装置中X为阳离子交换膜。请按要求回答相关问题:

(1)石墨电极(C)作___极,丙池中滴有酚酞,实验开始后观察到的现象是_____,甲中甲烷燃料电池的负极反应式为________。
(2)若消耗2.24 L(标况)氧气,则乙装置中铁电极上生成的气体体积(标况)为___ L。
(3)丙中以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是_______。
A.b电极为粗铜
B.粗铜接电源正极,发生还原反应
C.CuSO4溶液的浓度保持不变
D.利用阳极泥可回收Ag、Pt、Au等金属
(4)若丙中以稀H2SO4为电解质溶液,电极材料b为铝,则能使铝表面生成一层致密的氧化膜,该电极反应式为__________。
(5)假设乙装置中氯化钠溶液足够多,若在标准状况下,有224 mL氧气参加反应,则乙装置中阳离子交换膜,左侧溶液质量将_______,(填“增大”“减小”或“不变”),且变化了_____克。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求完成下列每一小题
(1)根据系统命名法,![]() 的名称是___;
的名称是___;
(2)根据系统命名法![]() 的名称是___;
的名称是___;
(3)根据系统命名法 的名称是___;
的名称是___;
(4) 核磁共振氢谱吸收峰面积之比是___。
核磁共振氢谱吸收峰面积之比是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,下列叙述不是可逆反应A(g)+3B(g) ![]() 2C(g)达到平衡的标志的是()
2C(g)达到平衡的标志的是()
(1)C的生成速率与C的分解速率相等;
(2)单位时间内生成amol A,同时生成3amol B;
(3)A、B、C的浓度不再变化;
(4)混合气体的总压强不再变化;
(5)混合气体的物质的量不再变化;
(6)单位时间消耗amol A,同时生成3amol B;
(7)A 、B、C的分子数目比为1:3:2。
A.(2)(5)B.(1)(3)C.(2)(7)D.(5)(6)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:![]() 时,
时,![]() ,
,![]() ,
,![]() ,
,![]() ,
,![]() 。
。
![]() 溶液和NaHA溶液反应的主要离子方程式为________________________________
溶液和NaHA溶液反应的主要离子方程式为________________________________![]() 不考虑
不考虑![]() 与
与![]() 发生氧化还原反应
发生氧化还原反应![]() 。
。
![]() 溶液中离子浓度由大到小的顺序为 ____________________________。
溶液中离子浓度由大到小的顺序为 ____________________________。
![]() 时,将
时,将![]() 的HCOOH溶液和
的HCOOH溶液和![]() 的
的![]() 溶液分别与
溶液分别与![]() 的
的![]() 溶液混合,实验测得产生的气体体积
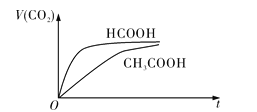
溶液混合,实验测得产生的气体体积![]() 随时间
随时间![]() 变化的示意图如图所示:
变化的示意图如图所示:
![]() 的电离平衡常数表达式
的电离平衡常数表达式![]() __________________________。
__________________________。
![]() 反应初始阶段,两种溶液产生
反应初始阶段,两种溶液产生![]() 气体的速率存在明显差异的原因是__________________________________________________________________________________,反应结束后所得两溶液中,
气体的速率存在明显差异的原因是__________________________________________________________________________________,反应结束后所得两溶液中,![]() ____________
____________![]() 填“
填“![]() ”“
”“![]() ”或“
”或“![]() ”
”![]() 。
。
![]() 时,某溶液中含有
时,某溶液中含有![]() 、
、![]() 加入KOH固体以调节溶液
加入KOH固体以调节溶液![]() 忽略溶液体积的变化、忽略
忽略溶液体积的变化、忽略 ![]() 的挥发和分解
的挥发和分解![]() 。当pH为7时,能否有
。当pH为7时,能否有![]() 沉淀生成?________
沉淀生成?________![]() 填“能”或“否”
填“能”或“否”![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下的四种溶液:①pH=9的 NaOH 溶液 ②pH=9的CH3COONa溶液 ③pH=5的H2SO4溶液 ④pH=5的NaHSO4 溶液,溶液中由水电离产生的c(OH-)相同的是( )
A.①②B.①③C.③④D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】太阳能电池板材料除单晶硅外,还有氮、硼、硒、钛、钴、钙等元素组成的化学物质。
⑴钙原子基态时的电子排布式为____________________,金属钴堆积方式与镁相似,都属于六方最密堆积,其配位数是____。
⑵氮元素的第一电离能在同周期中(稀有气体除外)从大到小排第___位;写出与NO3-互为等电子体的一种非极性分子的化学式__________。
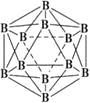
⑶晶体硼的结构单元是正二十面体,每个单元中有12个硼原子(如图),其中有两个原子为10B,其余为11B,则该结构单元有_____________种不同的结构类型。己知硼酸(H3BO3)为一元弱酸,解释其为一元弱酸的原因______________。硼酸的结构与石墨相似,层内的分子以氢键相连,含1 mol硼酸的晶体中有___mol氢键。
⑷硒是动物体必需的营养元素。SeO2是硒的重要化合物,SeO2的价层电子对互斥模型是_______________。
⑸在浓的TiCl3的盐酸溶液中加入乙醚,并通入HC1至饱和,可得到配位数为6,组成为 TiCl36H2O的晶体,该晶体中两种配体的物质的量之比为1:5,则该配离子的化学式为:__________________。
⑹钴晶体的一种晶胞是一种体心立方结构(如图所示),若该晶胞的边长为a nm,密度为ρ gcm-3,NA表示阿伏加德罗常数的值,则钴的相对原子质量可表示为_________________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com