
【题目】根据要求完成下列每一小题
(1)根据系统命名法,![]() 的名称是___;
的名称是___;
(2)根据系统命名法![]() 的名称是___;
的名称是___;
(3)根据系统命名法 的名称是___;
的名称是___;
(4) 核磁共振氢谱吸收峰面积之比是___。
核磁共振氢谱吸收峰面积之比是___。
【答案】2-甲基丁烷 4-甲基-2-戊烯 1,3,5-三甲基苯 1:2:2:3
【解析】
(1)根据烷烃的命名原则给该有机物命名;
(2)根据烯烃的系统命原则给该有机物命名;
(3)根据苯的同系物的系统命原则给该有机物命名;
(4)根据有机物结构中氢的种数判断核磁共振氢谱吸收峰面积之比。
(1)主链为4个C,即为丁烷,编号从右端开始,命名为:2-甲基丁烷;
(2)含碳碳双键的最长碳链有5个碳,即为戊烯,编号从右端开始,命名为:4-甲基-2-戊烯;
(3)根据苯的同系物的系统命原则,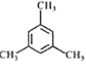 的名称是1,3,5-三甲基苯;
的名称是1,3,5-三甲基苯;
(4)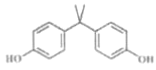 成轴对称,有4种不同化学环境的氢,核磁共振氢谱吸收峰面积之比是1:2:2:3。
成轴对称,有4种不同化学环境的氢,核磁共振氢谱吸收峰面积之比是1:2:2:3。


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:
【题目】以镍黄铁矿为原料制备![]() 的工艺流程如下:
的工艺流程如下:
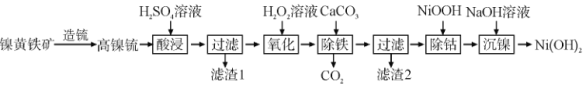
已知:①高镍锍的主要成分为![]() 、
、![]() 、
、![]() 、
、![]() 的低价硫化物及合金;
的低价硫化物及合金;
②氧化性:![]() ;
;
③![]() ,
,![]() ,
,![]() 。
。
回答下列问题:
(1)“酸浸”时,![]() 溶液需过量,其目的是________。
溶液需过量,其目的是________。
(2)“氧化”时反应的化学方程式为________,若用![]() 代替
代替![]() 溶液,使
溶液,使![]() 转化为
转化为![]() ,则需
,则需![]() 至少为________
至少为________![]() 。
。
(3)“除铁”的原理是________。
(4)“过滤”时滤渣1的主要成分是________。
(5)“沉镍”后需过滤、洗涤,证明沉淀已洗涤干净的方法是________________。若“沉镍”后的滤液中![]() ,则滤液的
,则滤液的![]() ________。
________。
(6)“除钴”时,发生反应的离子方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在复习元素化合物的性质时,做了如下学习笔记,请你一起完成。
氯气的颜色为__________;由氯的原子结构示意图推测,氯气具有很强的______ 性。为了证明推测是否正确,进行如下实验:
I:将红热的铁丝伸入盛满氯气的集气瓶,观察铁丝在氯气中燃烧,有大量棕黄色烟。该反应的化学方程式是___________。
II:在空气中点燃H2,然后将导管缓缓伸入盛满氯气的集气瓶,可观察到H2在氯气中安静燃烧,产生______色的火焰,瓶口有白雾的现象。
由实验I、II可知,上述推测_____(填“正确”或“不正确”)。
III:将氯气溶于水,制得氯水。下列物质不能与新制氯水反应的是_____。
A.Na2CO3溶液 B.FeCl2溶液 C.AgNO3 溶液 D.CuCl2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.PM2.5是指大气中直径≤2.5×10-6 m的颗粒物,则受PM2.5污染的大气定能产生丁达尔效应
B.根据电解质在水溶液中电离的程度,将电解质分为强电解质和弱电解质
C.黑火药的配方为“一硫二硝三木炭”,其中“硝”是指硝酸
D.![]() 、
、![]() 是制造氢弹的原料,它们是同一种核素
是制造氢弹的原料,它们是同一种核素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型氨法烟气脱硫技术的化学原理是采用氨水吸收烟气中的![]() ,再用一定量的磷酸与上述吸收产物反应。该技术的优点除了能回收利用
,再用一定量的磷酸与上述吸收产物反应。该技术的优点除了能回收利用![]() 外,还能得到一种复合肥料。
外,还能得到一种复合肥料。
(1)①若氨水与![]() 恰好完全反应生成正盐,则此时溶液呈________性
恰好完全反应生成正盐,则此时溶液呈________性![]() 填“酸”或“碱”
填“酸”或“碱”![]() 。常温下弱电解质的电离平衡常数如下:氨水
。常温下弱电解质的电离平衡常数如下:氨水![]()
![]() 溶液中通入________气体可使溶液呈中性。
溶液中通入________气体可使溶液呈中性。![]() 填“
填“![]() ”或
”或![]() ”
”![]() 此时溶液中
此时溶液中![]() ________
________![]() 填“
填“![]() ”“
”“![]() ”或“
”或“![]() ”
”![]()
(2)向![]() 溶液通入过量
溶液通入过量![]() ,充分反应后所得溶液中离子浓度大小顺序为________________。
,充分反应后所得溶液中离子浓度大小顺序为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的电子排布式为___,3d能级上的未成对电子数为___。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是___。
②在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为___,提供孤电子对的成键原子是___。
③氨的沸点___(填“高于”或“低于”)膦(PH3),原因是___。
(3)单质铜及镍都是由___键形成的晶体;元素铜与镍的第二电离能分别为ICu=1958kJ·mol-1、INi=1753kJ·mol-1,ICu>INi的原因是___。
(4)某镍白铜合金的立方晶胞结构如图所示。
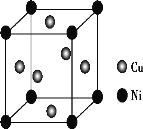
①晶胞中铜原子与镍原子的数量比为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将TiO2转化为TiCl4是工业冶炼金属钛的主要反应之一。已知:
TiO2(s)+2Cl2(g)===TiCl4(l)+O2(g) ΔH=+140.5 kJ·mol-1
C(s,石墨)+O2(g)===CO(g) ΔH=-110.5 kJ·mol-1
则反应TiO2(s)+2Cl2(g)+2C(s,石墨)===TiCl4(l)+2CO(g)的ΔH是
A.-80.5 kJ·mol-1 B.+30.0 kJ·mol-1
C.-30.0 kJ·mol-1 D.+80.5 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式中,ΔH能正确表示物质的燃烧热的是( )
A.C(s) +O2(g) = CO2(g) ΔH=+110.5 kJ·mol1
B.CH4(g) +2O2(g) = CO2(g)+2H2O(l) ΔH=-890.31 kJ·mol1
C.H2(g) +![]() O2(g)= H2O(g) ΔH=-241.8 kJ·mol1
O2(g)= H2O(g) ΔH=-241.8 kJ·mol1
D.2C8H18(l) +25O2(g) = 16CO2(g)+18H2O(l) ΔH=-11036 kJ·mol1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
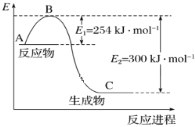
(1)上图是![]() 和
和![]() 反应生成
反应生成![]() 过程中能量的变化示意图,下列有关说法正确的是_______。
过程中能量的变化示意图,下列有关说法正确的是_______。
a. 反应物的总能量比生成物的总能量高
b. 反应物的活化能比生成物的活化能高
c. 反应物的总键能比生成物的总键能高
d. 该反应为熵增反应
(2)请写出![]() 和
和![]() 反应的热化学方程式:_______,决定该反应进行方向的主要判据为________。
反应的热化学方程式:_______,决定该反应进行方向的主要判据为________。
(3)试根据表中及图中数据计算![]() 的键能______________ kJ/mol;
的键能______________ kJ/mol;
化学键 |
|
|
键能/ kJ/mol | 390 | 943 |
(4)用![]() 催化还原
催化还原![]() 还可以消除氮氧化物的污染。已知:
还可以消除氮氧化物的污染。已知:
4NH3(g)+3O2(g)=2N2(g)+6H2O(g);△H1=-akJ/mol
N2(g)+O2(g)=2NO(g);△H2=-bkJ/mol
若1molNH3还原NO至N2,则该反应过程中的反应热△H3=_____________kJ/mol(用含a、b的式子表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com