
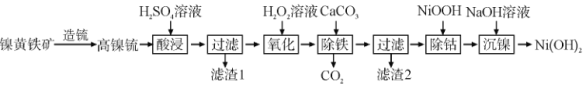
【题目】以镍黄铁矿为原料制备![]() 的工艺流程如下:
的工艺流程如下:
已知:①高镍锍的主要成分为![]() 、
、![]() 、
、![]() 、
、![]() 的低价硫化物及合金;
的低价硫化物及合金;
②氧化性:![]() ;
;
③![]() ,
,![]() ,
,![]() 。
。
回答下列问题:
(1)“酸浸”时,![]() 溶液需过量,其目的是________。
溶液需过量,其目的是________。
(2)“氧化”时反应的化学方程式为________,若用![]() 代替
代替![]() 溶液,使
溶液,使![]() 转化为
转化为![]() ,则需
,则需![]() 至少为________
至少为________![]() 。
。
(3)“除铁”的原理是________。
(4)“过滤”时滤渣1的主要成分是________。
(5)“沉镍”后需过滤、洗涤,证明沉淀已洗涤干净的方法是________________。若“沉镍”后的滤液中![]() ,则滤液的
,则滤液的![]() ________。
________。
(6)“除钴”时,发生反应的离子方程式为________。
【答案】提高镍元素的浸取率 ![]() 0.1
0.1 ![]() 与
与![]() 反应使溶液
反应使溶液![]() 升高,
升高,![]() 解生成
解生成![]() 沉淀而除去
沉淀而除去 ![]() 、
、![]() 取最后一次洗涤液少量,向其中滴加盐酸酸化的
取最后一次洗涤液少量,向其中滴加盐酸酸化的![]() 溶液,若无白色沉淀生成,则沉淀已洗涤干净 9
溶液,若无白色沉淀生成,则沉淀已洗涤干净 9 ![]()
【解析】
用硫酸溶液溶解高镍铳并过滤,除去不溶于酸和水的杂质Cu和CuS,同时得到含有Ni2+、Fe2+及Co2+的滤液,向滤液加入H2O2主要是氧化溶液中的Fe2+得Fe3+,后用CaCO3调节溶液pH,使Fe3+转化为Fe(OH)3沉淀,通过过滤除去,达到除铁的目的,过滤后的滤液中继续加入NiOOH,可生成Co(OH)3,再过滤除去,达到除钴的目的,最后滤液中加入NaOH溶液,并过滤即可得到Ni(OH)2。
(1)“酸浸”时,加入过滤的硫酸溶液,可使高镍铳完全溶解,提高镍元素的浸取率;
(2) H2O2氧化溶液中的Fe2+得Fe3+,发生反应的化学方程式为2FeSO4+H2O2+H2SO4=Fe2(SO4)3+2H2O;若用NaClO代替H2O2溶液,使0.2mol Fe2+转化为Fe3+,共转移0.2mole-,NaClO的还原产物为NaCl,则需NaClO至少为![]() =0.1mol;
=0.1mol;
(3)Fe3+在溶液中存在水解平衡为Fe3++3H2O![]() Fe(OH)3+3H+,加入CaCO3能与H+反应使溶液pH升高,Fe3+水解生成Fe(OH)3沉淀而除去;
Fe(OH)3+3H+,加入CaCO3能与H+反应使溶液pH升高,Fe3+水解生成Fe(OH)3沉淀而除去;
(4)由分析知,“过滤”时滤渣1的主要成分是不溶液于稀硫酸的Cu为CuS;
(5) Ni(OH)2的表面附着液中含有SO42-,则取最后一次洗涤液少量,向其中滴加盐酸酸化的BaCl2溶液,若无白色沉淀生成,则沉淀已洗涤干净;已知Ksp[Ni(OH)2]=1×10-15=c(Ni2+)×c2(OH-),则c(OH-)=![]() mol/L=10-5mol/L,此时溶液pH=9;
mol/L=10-5mol/L,此时溶液pH=9;
(6)“除钴”时NiOOH可生成Co(OH)3,则发生反应的离子方程式为NiOOH+Co2++H2O=Ni2++Co(OH)3。


 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源: 题型:
【题目】1909年化学家哈伯在实验室首次合成了氨。2007年化学家格哈德·埃特尔在哈伯研究所证实了氢气与氮气在固体表面合成氨的反应过程,示意如下图:
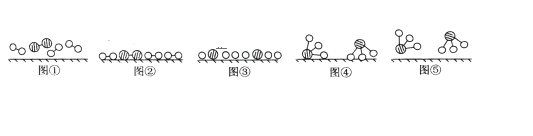
(1)图⑤表示生成的NH3离开催化剂表面,图③的含义分别是_____________。
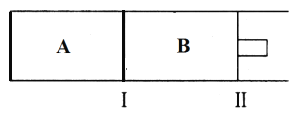
(2)500℃下,在A、B两个容器中均发生合成氨的反应。起始两容器充入两气体两相同,体积相同,隔板Ⅰ固定不动,活塞Ⅱ可自由移动。
①两容器的N2的转化率关系为αA____αB(填“>”、“<”或“=”)
②在B容器中,反应达到平衡的标志有________。
A 容器中气体压强不再发生变化
B 容器中气体密度不再发生变化
C 容器中气体平均摩尔质量不再发生变化
③当合成氨在容器B中达平衡时,测得其中含有1.0molN2,0.4molH2,0.4molNH3,此时容积为2.0L。保持温度和压强不变,向此容器中通入0.36molN2,平衡将____________(填“正向”、“逆向”或“不”)移动。
④向A、B两容器中均通入xmolN2和ymolH2,初始A、B容积相同,并保持温度不变。若要平衡时保持N2在A、B两容器中的体积分数相同,则x与y之间必须满足的关系式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 时,下列溶液中,离子浓度关系正确的是
时,下列溶液中,离子浓度关系正确的是![]()
A.![]() 的氨水稀释10倍后,其
的氨水稀释10倍后,其![]() ,则
,则![]()
B.浓度相同的![]() ,三种溶液中的
,三种溶液中的![]()
C.将相同浓度的氨水与盐酸等体积混合,所得溶液中的离子浓度关系:![]()
D.将![]() 与
与![]() 溶液等体积混合,测得溶液pH为7,则a与b的关系:
溶液等体积混合,测得溶液pH为7,则a与b的关系:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁、铝、硅、银、铁的单质及其化合物在建筑业、飞机制造业、电子工业和石油化工等方面应用广泛。回答下列问题:
(1)Fe3+价层电子的轨道表达式(电子排布图)为__。
(2)晶体硅属于______晶体。硅能形成多种化合物(如SiH4、Si2H4等),SiH4的分子的立体构型为____;Si2H4分子中含有的σ键和π键的数目之比为____。
有机物种类繁多的原因其中之一就是因为碳原子之间既可以形成单键又可以形成双键和三键,Si和Ge与C是同主族价电子数相同,但是Si和Ge就难形成双键或三键,原因是________
(3)Mg、Al、Si的第一电离能由大到小顺序:______________
(4)Ca和Fe属于同一周期,且核外最外层电子构型相同,但金属Ca的熔点、沸点等都比金属Fe低,原因是______。
(5)Ag晶体的堆积方式为面心立方最密堆积(如图所示),晶胞中Ag原子的配位数为______;设Ag原子半径为rcm,阿伏加德罗常数的值用NA表示,则Ag晶体的密度为______g·cm-3(写出表达式)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在药物制剂中,抗氧剂与被保护的药物在与![]() 发生反应时具有竞争性,抗氧性强弱主要取决于其氧化反应的速率。
发生反应时具有竞争性,抗氧性强弱主要取决于其氧化反应的速率。![]() 、
、![]() 和
和![]() 是三种常用的抗氧剂。已知:
是三种常用的抗氧剂。已知:![]() 溶于水发生反应:
溶于水发生反应:![]() ;
;![]() 以原溶液和一定量的酸或碱混合,保持总体积不变的方式调节pH。
以原溶液和一定量的酸或碱混合,保持总体积不变的方式调节pH。
实验用品 | 实验操作和现象 |
| 实验1:溶液 |
| 实验2:溶液
|
| 实验3:调溶液 |
下列说法中不正确的是 ![]()
A.![]() 溶液显碱性,原因是
溶液显碱性,原因是![]()
B.![]() 溶液中
溶液中![]() 的电离程度大于水解程度
的电离程度大于水解程度
C.实验2说明,![]() 在
在![]() 时抗氧性最强
时抗氧性最强
D.实验3中,三种溶液在pH相同时起抗氧作用的微粒种类和浓度相同,因此反应速率相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次增大,X、Y同周期且相邻,Y是地壳中含量最多的元素,Z是短周期中原子半径最大的主族元素,W的单质常温下是一种淡黄色固体。下列叙述正确的是( )
A.元素的非金属性:![]()
B.Z的单质在空气中燃烧生成阴、阳离子个数比为![]() 的氧化物
的氧化物
C.Y的简单气态氢化物的稳定性强于W的
D.工业上一般采用电解对应盐的水溶液制Z单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C1O2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得C1O2:2KClO3+H2C2O4+H2SO4![]() 2ClO2↑+K2SO4+2CO2↑+2H2O,下列说法中正确的是
2ClO2↑+K2SO4+2CO2↑+2H2O,下列说法中正确的是
A. 在反应中H2C2O4既不是氧化剂也不是还原剂
B. 1 mol KClO3参加反应,在标准状况下能得到22.4 L气体
C. 1 mol KClO3参加反应有2 mol电子转移
D. KClO3在反应中是氧化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用石墨电极电解饱和食盐水的原理示意图如图所示。下列说法正确的是( )
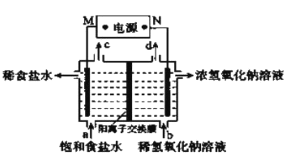
A.M为负极
B.Na+移动方向:通过离子交换膜由右向左
C.c出口收集到的物质是氯气
D.电解一段时间后,阴极区pH降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求完成下列每一小题
(1)根据系统命名法,![]() 的名称是___;
的名称是___;
(2)根据系统命名法![]() 的名称是___;
的名称是___;
(3)根据系统命名法 的名称是___;
的名称是___;
(4) 核磁共振氢谱吸收峰面积之比是___。
核磁共振氢谱吸收峰面积之比是___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com