
【题目】下列有关说法正确的是
A. 298K时,反应2Mg(s)+CO2(g)===C(s)+2MgO(s)能自发进行,则该反应的ΔH>0
B. 电解法精炼铜时,粗铜作阳极,精铜作阴极
C. 在硫酸钡悬浊液中加入足量饱和Na2CO3溶液处理,向所得沉淀中加入盐酸有气体产生,说明Ksp(BaSO4)>Ksp(BaCO3)
D. 常温下,pH均为5的盐酸与氯化铵溶液中,水的电离程度相同
科目:高中化学 来源: 题型:
【题目】下列反应不属于取代反应的是( )
A.淀粉水解制葡萄糖 B.石油裂解制丙烯
C.乙醇与乙酸反应制乙酸乙酯 D.油脂与浓NaOH反应制高级脂肪酸钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属晶体的堆积方式、空间利用率和配位数的关系正确的是 ( )
A.钋——简单立方堆积——52%——8
B.钠Na——体心立方堆积——74%——12
C.锌Zn——六方最密堆积——68%——8
D.银Ag——面心立方最密堆积——74%——12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氧化还原反应的原理分析,正确的是
A.失电子越多,该物质的还原性就越强
B.含有最高价元素的化合物一定具有强氧化性
C.氧化剂氧化其他物质时,本身被还原
D.某元素由化合态变成游离态一定被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,将a L HCl完全溶于水得到V mL盐酸,溶液的密度为ρ g·cm-3,溶质的质量分数为w,溶质的物质的量浓度为c mol·L-1。下列叙述中正确的是
①c=![]() ×100% ②c=
×100% ②c=![]() ③若上述溶液中再加入V mL水后,所得溶液的质量分数大于0.5w ④将50 g上述溶液加入一定量的水稀释成0.5c mol·L-1,则加入水的体积应大于50 mL
③若上述溶液中再加入V mL水后,所得溶液的质量分数大于0.5w ④将50 g上述溶液加入一定量的水稀释成0.5c mol·L-1,则加入水的体积应大于50 mL
A. ①④ B. ②③
C. ①③ D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,l mol X和n mol Y在体积为2L的密闭容器中发生如下反应:X(g) + Y(g)![]() 2Z(g) + M(s),5min后达到平衡,此时生成2a mol Z。下列说法正确的是
2Z(g) + M(s),5min后达到平衡,此时生成2a mol Z。下列说法正确的是
A. 用X表示5min内此反应的反应速率是(0.1—0.2a)mol·(L·min)—1
B. 当混合气体的质量不再发生变化时,说明反应达到平衡状态
C. 向平衡后的体系中加入l mol M,平衡向逆反应方向移动
D. 向上述平衡体系中再充入l mol X,v(正)增大,v(逆)减小,平衡正向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于硅酸盐工业的叙述正确的是
A. 普通玻璃的主要成分可以表示为Na2O·CaO·6SiO2,说明玻璃为纯净物
B. 陶瓷、玻璃、水泥都属于硅酸盐产品
C. 制玻璃、水泥时都用到了石灰石和黏土
D. 制玻璃的过程中发生了反应:Na2CO3+SiO2![]() Na2SiO3+CO2↑,说明酸性:H2SiO3>H2CO3
Na2SiO3+CO2↑,说明酸性:H2SiO3>H2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前已开发出用电解法制取ClO2的新工艺。
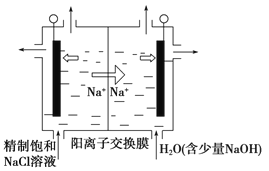
(1)图中用石墨做电极,在一定条件下电解饱和食盐水制取ClO2。则阳极产生ClO2的电极反应式为___________________________________________。
(2)电解一段时间,当阴极产生的气体体积为112 mL(标准状况)时,停止电解。通过阳离子交换膜的阳离子的物质的量为________mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷精矿湿法制备磷酸的一种工艺流程如下:

已知:磷精矿主要成分为Ca5(PO4)3(OH),还含有Ca5(PO4)3F和有机碳等。
溶解度:Ca5(PO4)3(OH)<CaSO4·0.5H2O
(1)上述流程中能加快反应速率的措施有__________。
(2)磷精矿粉酸浸时发生反应:
2Ca5(PO4)3(OH)+3H2O+10H2SO4![]() 10CaSO4·0.5H2O+6H3PO4
10CaSO4·0.5H2O+6H3PO4
①该反应体现出酸性关系:H3PO4__________H2SO4(填“>”或“<”)。
②结合元素周期律解释①中结论:P和S电子层数相同,__________。
(3)酸浸时,磷精矿中Ca5(PO4)3F所含氟转化为HF,并进一步转化为SiF4除去。写出生成HF的化学方程式:__________。
(4)H2O2将粗磷酸中的有机碳氧化为CO2脱除,同时自身也会发生分解。相同投料比、相同反应时间,不同温度下的有机碳脱除率如图所示。80℃后脱除率变化的原因:____________________。

(5)脱硫时,CaCO3稍过量,充分反应后仍有SO42残留,原因是__________;加入BaCO3可进一步提高硫的脱除率,其离子方程式是____________________。
(6)取a g所得精制磷酸,加适量水稀释,以百里香酚酞作指示剂,用b mol·L1NaOH溶液滴定至终点时生成Na2HPO4,消耗NaOH溶液c mL,精制磷酸中H3PO4的质量分数是________。(已知:H3PO4摩尔质量为98 g·mol1)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com