
【题目】下列关于硅酸盐工业的叙述正确的是
A. 普通玻璃的主要成分可以表示为Na2O·CaO·6SiO2,说明玻璃为纯净物
B. 陶瓷、玻璃、水泥都属于硅酸盐产品
C. 制玻璃、水泥时都用到了石灰石和黏土
D. 制玻璃的过程中发生了反应:Na2CO3+SiO2![]() Na2SiO3+CO2↑,说明酸性:H2SiO3>H2CO3
Na2SiO3+CO2↑,说明酸性:H2SiO3>H2CO3
科目:高中化学 来源: 题型:
【题目】下列关于金属钠说法正确的是( )
A.钠是银白色金属,熔点低,硬度大
B.钠放置在空气中,会迅速被氧化而生成淡黄色的氧化钠
C.在空气中加热时,金属钠剧烈燃烧,发出黄色火焰
D.金属钠着火可以用二氧化碳灭火器或用干燥的沙土灭火
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A. 298K时,反应2Mg(s)+CO2(g)===C(s)+2MgO(s)能自发进行,则该反应的ΔH>0
B. 电解法精炼铜时,粗铜作阳极,精铜作阴极
C. 在硫酸钡悬浊液中加入足量饱和Na2CO3溶液处理,向所得沉淀中加入盐酸有气体产生,说明Ksp(BaSO4)>Ksp(BaCO3)
D. 常温下,pH均为5的盐酸与氯化铵溶液中,水的电离程度相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在常温下,用0.1000mol/L的盐酸滴定25mL0.100mol/Lna2CO3溶液,所得滴定曲线如下图所示。下列相关微粒浓度间的关系不正确的是

A. a点:c(CO32-)>c(Cl-)>c(HCO3-)
B. b点:c(Na+)+c(H+)= c(Cl-)+ c(HCO3-)+2c(CO32-)+c(OH-)
C. c点:c(OH-)+ c(CO32-)= c(H+)+c(H2CO3)
D. d点:c(Cl-)= c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知CO和H2在一定条件下合成甲醇的反应为CO(g)+2H2(g)![]() CH3OH(g)。现在容积均为1 L的a、b、c三个密闭容器中分别充入1 mol CO和2 mol H2的混合气体,控制温度进行反应,测得相关数据的关系如图所示。下列说法正确的是( )
CH3OH(g)。现在容积均为1 L的a、b、c三个密闭容器中分别充入1 mol CO和2 mol H2的混合气体,控制温度进行反应,测得相关数据的关系如图所示。下列说法正确的是( )
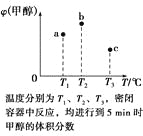
A. 正反应的ΔH>0
B. 反应进行到5 min时,b容器中v正=v逆
C. 减压可将b中的平衡状态转变成c中的平衡状态
D. 达到平衡时,a、b、c中CO的转化率为b>a>c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国是世界上最早制得和使用金属锌的国家,一种以闪锌矿(ZnS,含有SiO2和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如图所示:

相关金属离子[c0(Mn+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下:
金属离子 | Fe3+ | Fe2+ | Zn2+ | Cd2+ |
开始沉淀的pH | 1.5 | 6.3 | 6.2 | 7.4 |
沉淀完全的pH | 2.8 | 8.3 | 8.2 | 9.4 |
回答下列问题:
(1)焙烧过程中主要反应的化学方程式为_______________________。
(2)滤渣1的主要成分除SiO2外还有___________;氧化除杂工序中ZnO的作用是____________,若不通入氧气,其后果是________________。
(3)溶液中的Cd2+可用锌粉除去,还原除杂工序中反应的离子方程式为_________________。
(4)电解硫酸锌溶液制备单质锌时,阴极的电极反应式为______________;沉积锌后的电解液可返回_______工序继续使用。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)同温同压下,同体积的N2和SO2分子数之比为__________________,物质的量之比为____________,原子总数之比为____________,摩尔质量之比为__________,质量之比为________________,密度之比为______________。
(2)现有质量比为11:14的CO2和CO的混合气体,则该混合气体中的CO2和CO物质的量之比为________,碳原子和氧原子的个数比为________,该混合气体的摩尔质量为________。
(3)12.4gNa2X中含Na+ 0.4mol,则Na2X的摩尔质量是________,X的相对原子质量是________。
(4)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状况下,11.2L“人造空气”的质量是4.8g,其中氧气和氦气的分子数之比是______,氧气的质量是_______。
(5)某元素的一个原子的质量为ag,一个12C原子的质量为bg,阿伏加德罗常数为NA,则该原子的相对原子质量数值可表示为______________或_______________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物异搏定合成路线中,其中的一步转化如下:
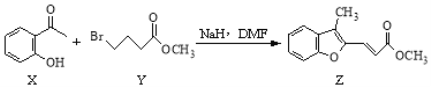
下列说法正确的是
A. Y的分子式为C5H9O2Br
B. X分子中所有原子在同一平面内
C. Z和足量H2加成后的分子中有5个手性碳原子
D. 等物质的量的X、Z分别与溴水反应,最多消耗Br2的物质的量之比1:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com