
����Ŀ���ҹ��������������Ƶú�ʹ�ý���п�Ĺ��ң�һ������п��ZnS������SiO2������FeS��CdS��PbS���ʣ�Ϊԭ���Ʊ�����п��������ͼ��ʾ��

��ؽ�������[c0(Mn+)=0.1 mol��L-1]�γ��������������pH��Χ���£�
�������� | Fe3+ | Fe2+ | Zn2+ | Cd2+ |
��ʼ������pH | 1.5 | 6.3 | 6.2 | 7.4 |
������ȫ��pH | 2.8 | 8.3 | 8.2 | 9.4 |
�ش��������⣺
��1�����չ�������Ҫ��Ӧ�Ļ�ѧ����ʽΪ_______________________��
��2������1����Ҫ�ɷֳ�SiO2���___________���������ӹ�����ZnO��������____________������ͨ��������������________________��
��3����Һ�е�Cd2+����п�۳�ȥ����ԭ���ӹ����з�Ӧ�����ӷ���ʽΪ_________________��
��4���������п��Һ�Ʊ�����пʱ�������ĵ缫��ӦʽΪ______________������п��ĵ��Һ�ɷ���_______�������ʹ�á�
���𰸡� ZnS+![]() O2
O2 ZnO+SO2 PbSO4 ������Һ��pH ����ȥ����Fe2+ Zn+Cd2+
ZnO+SO2 PbSO4 ������Һ��pH ����ȥ����Fe2+ Zn+Cd2+![]() Zn2++Cd Zn2++2e��
Zn2++Cd Zn2++2e��![]() Zn �ܽ�
Zn �ܽ�
������������������ʱ��Ԫ��ת��ΪSO2��Ȼ����ϡ�����ܽ�����������п�����������������ӣ�����������ϡ�����Ӧת��Ϊ��������������Ǧ������ˮ���������1�л���������Ǧ�����ڳ����������ӵ�pH�ϴ���Ҫ��������Ϊ�����ӣ�ͨ������pH�õ�����������������Һ�м���п���û���Cd�������Һ���õ�����п���ݴ˽����
��⣺��1��������п�����Ҫ�ɷ���ZnS����˱��չ�������Ҫ��Ӧ�Ļ�ѧ����ʽΪ2ZnS+3O2![]() 2ZnO+2SO2��
2ZnO+2SO2��
��2����������Ǧ������ˮ���������1����Ҫ�ɷֳ�SiO2���PbSO4��Ҫ�ⶨ�����ӣ���Ҫ������Һ��pH������Ϊ�������������ʣ�������Ҫ��������п����pH�����������ӹ�����ZnO�������ǵ�����Һ��pH�����ݱ������ݿ�֪�����������ӵ�pH�ϴ���������ͨ������������������ȥ����Fe2+��
��3����Һ�е�Cd2+����п�۳�ȥ����Ӧ�����ӷ���ʽΪZn+Cd2+��Zn2++Cd��
��4���������п��Һ�Ʊ�����пʱ�����������õ����ӵĻ�ԭ��Ӧ�����������п���ӷŵ磬�������ĵ缫��ӦʽΪZn2++2e����Zn���������������ŵ磬�ƻ�ˮ�ĵ���ƽ�⣬���������ӣ����Ե����������������˳���п��ĵ��Һ�ɷ����ܽ��������ʹ�á�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������е�һ��ѧУ����һ�ֽ�������ֲ�����֯�к��е������ǡ����ۡ���ά�ص����࣬֬������֬�����з����Ե���֬��֬�ʣ�DNA��RNA�Ⱥ�����Ӻ��ָ����ĵ����ʣ���Щ�л����ж����е�Ԫ����(����)
A. C��H��O B. C��H��O��N C. C��H��O��N��P D. C��H��O��N��P��S
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڱ�״���£���a L HCl��ȫ����ˮ�õ�V mL���ᣬ��Һ���ܶ�Ϊ�� g��cm��3�����ʵ���������Ϊw�����ʵ����ʵ���Ũ��Ϊc mol��L��1��������������ȷ����
��c��![]() ��100%����c��
��100%����c��![]() ������������Һ���ټ���V mLˮ��������Һ��������������0.5w���ܽ�50 g������Һ����һ������ˮϡ�ͳ�0.5c mol��L��1�������ˮ�����Ӧ����50 mL
������������Һ���ټ���V mLˮ��������Һ��������������0.5w���ܽ�50 g������Һ����һ������ˮϡ�ͳ�0.5c mol��L��1�������ˮ�����Ӧ����50 mL
A. �٢� B. �ڢ�
C. �٢� D. �ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڹ����ι�ҵ��������ȷ����
A. ��ͨ��������Ҫ�ɷֿ��Ա�ʾΪNa2O��CaO��6SiO2��˵������Ϊ������
B. �մɡ�������ˮ����ڹ����β�Ʒ
C. �Ʋ�����ˮ��ʱ���õ���ʯ��ʯ�����
D. �Ʋ����Ĺ����з����˷�Ӧ��Na2CO3+SiO2![]() Na2SiO3+CO2����˵�����ԣ�H2SiO3>H2CO3
Na2SiO3+CO2����˵�����ԣ�H2SiO3>H2CO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С�����þ��CO2�ķ�Ӧ���ʵ��̽��þ��NO2�ķ�Ӧ��
��ͬѧ�Ʋ������MgO��N2��
��ͬѧ�Ʋ�������MgO��N2�⣬�����л����ܺ���Y��
��С��ͬѧ���������װ��̽��þ��NO2��Ӧ�Ĺ��������ⶨ����ɡ�

��1��ʵ�鿪ʼʱ���ȹر�ֹˮ�к���ɼУ��ٴ�Һ©����������Ӳ�ʲ����ܳ�������ɫ�����ֹˮ�У��رյ��ɼУ�����ȼ�ƾ��ơ���������Ŀ����___________________________________________________________
��2��װ��B�е��Լ�����ѡ��________
A��Ũ���� B����ˮ�Ȼ��� C������������ D����ʯ��
��3��װ��C��ʢװ����������Һ�������ǣ�___________________________________
��4��Ϊ��֤�������������ȷ�ԣ���ȡ��Ͳ�̶�ʱӦע��������Ǣ�����ָ��������ٶ�������_______________________________����______________________________��
��5��ʵ���������ͬѧ�ǽ��������ȡ����ˮ��Ӧ�������д̼�����ζ�������������������ʹʪ���ʯ����ֽ������˵������ͬѧ�Ʋ���ȷ����д��Y��ˮ��Ӧ�Ļ�ѧ����ʽ__________________________________
��6������ʼ����þ������Ϊ3.6 g����������NO2�г�ַ�Ӧ�� ���ռ���N2���Ϊ448mL (��״��)���������MgO��������_________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ŀǰ�ѿ������õ�ⷨ��ȡClO2���¹��ա�
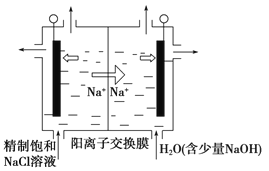
��1��ͼ����ʯī���缫����һ�������µ�ⱥ��ʳ��ˮ��ȡClO2������������ClO2�ĵ缫��ӦʽΪ___________________________________________��
��2�����һ��ʱ�䣬�������������������Ϊ112 mL(��״��)ʱ��ֹͣ��⡣ͨ�������ӽ���Ĥ�������ӵ����ʵ���Ϊ________mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ��ȡһ��������MgCl2���������Һ���ڸ���Һ�м���һ������ϡ���ᣬȻ����˻����Һ����μ���NaOH��Һ(����ͼ����ʾ)���μӹ����в������������������NaOH��Һ������Ĺ�ϵ����ͼ����ʾ��

��ش��������⣺
(1)�ܽ�MgCl2�������õIJ���������______(����ĸ)��
a����ƽ b���ձ�
c��©�� d��������
(2)OA�η�Ӧ�����ӷ���ʽΪ______________________________________��
(3)AB�η�Ӧ�����ӷ���ʽΪ______________________________________��
(4)��B���Ӧ����Һ�еμ�AgNO3��Һ���۲쵽��������________����Ӧ�����ӷ���ʽΪ_________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ⶨ0.1 mol��L-1 Na2SO3��Һ�������ٽ��¹����е�pH���������¡�
ʱ�� | �� | �� | �� | �� |
�¶�/�� | 25 | 30 | 40 | 25 |
pH | 9.66 | 9.52 | 9.37 | 9.25 |
ʵ������У�ȡ�٢�ʱ�̵���Һ�����������ữ��BaCl2��Һ���Ա�ʵ�飬�ܲ�����ɫ�����ࡣ
����˵������ȷ����
A. Na2SO3��Һ�д���ˮ��ƽ����![]() +H2O
+H2O![]()
![]() +OH
+OH
B. ����pH������ͬ��������![]() Ũ�ȼ�С��ɵ�
Ũ�ȼ�С��ɵ�
C. �١����Ĺ��������¶Ⱥ�Ũ�ȶ�ˮ��ƽ���ƶ������Ӱ��һ��
D. ��������Kwֵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ϸͭ������Ҫ��;����ҵ�Ͽ���ͨ������ͭ�Ͻ𣨺�Cu��Al��Zn���Ƴ�ϸͭ�ۡ�ijС����ʵ����ģ���Ʊ���ϸͭ�۵ķ�������:
�����ȡ����ͭ�Ͻ������Ũ�����ܽ⣬�ټ������NaOH��Һֻ����Cu(OH)2���������ˣ�ϴ�ӡ�
�������Cu(OH)2�����м������ܽ⣬�ټӰ�ˮ���γ� [Cu(NH3)4]SO4��Һ��
�������[Cu(NH3)4]SO4��Һ��ͨ��SO2��������Һ�����ԣ�����NH4CuSO3������������1.000mol��L-1��ϡ�����ϲ��ȣ��õ���ϸͭ�ۡ�
��1�����������ȫ�ܽ�����ͭ�Ͻ���Լ���ϡ�����____��
A��FeCl3 B������ C���ȿ���
��2������500 mL 1.000 mol��L-1��ϡ���ᣬ��Ҫ��98%��Ũ���ᣨ�ܶ�Ϊ1.84 g��mL-1��____mL��
��3���ڲ����������NH4CuSO3�Ļ�ѧ��Ӧ����ʽΪ____��
��4��ȷ��ȡ1.000 g����ͭ�Ͻ���������1.000 mol��L-1ϡ������ȫ��Ӧ�����ɱ�״�����������Ϊ134.4 mL������ͬ�����ĺϽ���ȫ�����ȵ�������Ũ���ᣬ������״�����������Ϊ380.8mL������˺Ͻ���ͭ����������________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com