
【题目】铁和铜都是日常生活中常见的金属,有着广泛的用途。请回答下列问题:
(1)配合物Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于__________(填晶体类型);Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=_____________;![]() 的核外电子排布式为_____________________。
的核外电子排布式为_____________________。
(2)![]() 溶液可用于检验_________(填离子符号);
溶液可用于检验_________(填离子符号);![]() 中碳原子杂化轨道类型为_____;1mol
中碳原子杂化轨道类型为_____;1mol![]() 含有的π键数目为_______(用N表示);C、N、O第一电离能由大到小的顺序为_________(用元素符号表示)。
含有的π键数目为_______(用N表示);C、N、O第一电离能由大到小的顺序为_________(用元素符号表示)。
(3)某M原子的外围电子排布式为![]() ,铜与M形成的某化合物的晶胞结构如下图所示(黑点代表铜原子)。
,铜与M形成的某化合物的晶胞结构如下图所示(黑点代表铜原子)。

①该晶体的化学式为__________________。
②已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于___________(填“离子”或“共价”)化合物。
③已知该晶体的密度为![]() ,阿伏加德罗常数为
,阿伏加德罗常数为![]() ,则该晶体中铜原子和M原子之间的最短距离为____________________pm(只需写出计算式)。
,则该晶体中铜原子和M原子之间的最短距离为____________________pm(只需写出计算式)。
【答案】分子晶体 5 ![]() 或
或![]()
![]() sp 2
sp 2![]() N>O>C CuCl 共价
N>O>C CuCl 共价 ![]() 或
或 或
或
【解析】
(1)Fe(CO)x常温下呈液态,熔沸点较低,易溶于非极性溶剂,符合分子晶体的特点,因此Fe(CO)x属于分子晶体;中心原子铁价电子数为8,配体CO提供2个电子形成配位键,因此x=(18-8)/2=5;![]() 的核外电子排布式为
的核外电子排布式为![]() 或
或![]() ;
;
(2)含Fe2+的溶液与铁氰化钾K3[Fe(CN)6]溶液反应生成具有特征蓝色的铁氰化亚铁沉淀,所以![]() 溶液可用于检验
溶液可用于检验![]() ;C、N之间是叁键,CN-中C有一个孤电子对,CN-中心原子C价电子对数2,C杂化轨道类型为sp;C、N之间是叁键,1mol
;C、N之间是叁键,CN-中C有一个孤电子对,CN-中心原子C价电子对数2,C杂化轨道类型为sp;C、N之间是叁键,1mol![]() 含有的π键数目为2
含有的π键数目为2![]() ;C、N、O属于同一周期,电离能同周期从左向右增大,但是第ⅡA族大于第ⅢA族,第ⅤA族大于ⅥA族,因此N>O>C;
;C、N、O属于同一周期,电离能同周期从左向右增大,但是第ⅡA族大于第ⅢA族,第ⅤA族大于ⅥA族,因此N>O>C;
(3)①M原子的外围电子排布式3s23p5,M是第三周期第ⅦA族元素,即Cl,铜在晶胞占有的位置为8个顶点、6个面,铜原子的个数8×1/8+6×1/2=4,Cl原子在晶胞的位置在体心,全部属于晶胞,Cl个数是4,化学式:CuCl;
②一般认为两个成键元素原子间的电负性差值大于1.7形成离子键,小于1.7形成共价键,铜与Cl电负性差值3.0-1.9=1.1<1.7,该化合物属于共价化合物;
③设边长为acm,ρ=![]() ,a=
,a=![]() ,该晶胞类似与金刚石的晶胞,Cu和Cl最近的距离是体对角线的1/4,即距离为:
,该晶胞类似与金刚石的晶胞,Cu和Cl最近的距离是体对角线的1/4,即距离为:![]() pm。
pm。


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:
【题目】一种熔融碳酸盐燃料电池原理示意如图。下列有关该电池的说法正确的是

A.电极A上发生的是还原反应
B.电池工作时,![]() 向电极B移动
向电极B移动
C.电极B上发生的电极反应为:O2+2CO2+4e-=2![]()
D.电极A上H2参与的电极反应为:H2+2OH--2e-=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素铜(Cu)、砷(As)、镓(Ga)等形成的化合物在现代工业中有广泛的用途,回答下列问题:
(1)基态铜原子的价电子排布式为_____________,价电子中未成对电子占据原子轨道的形状是__________________________。
(2)化合物AsCl3分子的立体构型为________________,其中As的杂化轨道类型为_____________。
(3)第一电离能Ga__________As。(填“>”或“<”)
(4)若将络合离子[Cu(CN)4]2-中的2个CN- 换为两个Cl-,只有一种结构,则[Cu(CN-)4]2-中4个氮原子所处空间构型为_______________,一个CN-中有__________个π键。
(5)砷化镓是一种重要的半导体材料,晶胞结构如图所示。

熔点为1238℃,密度为g·cm-3,该晶体类型为______________,Ga与As以__________键键合,Ga和As的相对原子质量分别为Ma和Mb,原子半径分别为racm和rbcm,阿伏加德罗常数值为NA,GaAs晶胞中原子体积占晶胞体积的百分率为____________________。(列出计算公式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 0.1molFe溶于硝酸,电子转移数目一定为0.3![]()
B. 标准状况下,14.4g正戊烷(![]() )中含C-C键数目为0.8N
)中含C-C键数目为0.8N
C. 18g重水(![]() )中含中子数目为10
)中含中子数目为10![]()
D. 12g熔融![]() 中含离子总数目为0.3
中含离子总数目为0.3![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是298K时,N2与H2反应过程中能量变化的曲线图,下列叙述不正确的是

A. 在温度、体积一定的条件下,通入1mol N2和3mol H2 反应后放出的热量为92kJ
B. a曲线是加入催化剂时的能量变化曲线
C. 加入催化剂,也不能提高N2的转化率
D. 该反应的热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) △H=﹣92 kJ/mol
2NH3(g) △H=﹣92 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水煤气(CO 和H2)是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:C(s) + H2O(g)![]() CO(g) +H2(g) △H=+131.3 kJ·mol-1
CO(g) +H2(g) △H=+131.3 kJ·mol-1
(1)该反应的平衡常数K随温度的升高而___________(选填“增大”“ 减小”或“不变”)
(2)上述反应达到平衡后,将体系中的C(s)部分移走,平衡____________(选填“向左移”“向右移”或“不移动”)。
(3)下列事实能说明该反应在一定条件下已达到平衡状态的有___________(填序号)。
A.单位体积内每消耗1 mol CO的同时生成1molH2
B.混合气体总物质的量保持不变
C.生成H2O(g)的速率与消耗CO的速率相等
D.H2O(g)、CO、H2的浓度相等
(4)某温度下,将4.0 mol H2O(g)和足量的炭充入2 L的密闭容器中,发生如下反应,C(s)+ H2O(g)![]() CO(g)+H2(g),达到平衡时测得K=1,则此温度下H2O(g)的转化率为________________。
CO(g)+H2(g),达到平衡时测得K=1,则此温度下H2O(g)的转化率为________________。
(5)己知:① C(s)+H2O(l)![]() CO(g)+H2(g) △H1
CO(g)+H2(g) △H1
② 2CO(g)+O2(g)=2CO2 (g) △H2
③ H2O (l)=H2 (g)+1/2 O2 (g) △H3
则C(s)+O2 (g)=CO2 (g)的△H=_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用浓盐酸与高锰酸钾发生反应快速制备氯气。化学方程式为:2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O。
(1)用单线桥法表示该反应过程中的电子转移情况。________________,该反应中HCl被氧化和未被氧化的物质的量之比为________。
(2)下列装置为实验室制备氯气的装置。
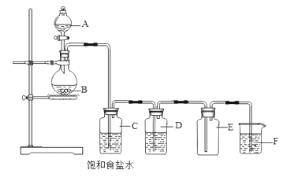
装置C的作用是______________________,装置E的作用是_______________________________。装置F中的试剂是_________________。
(3)写出F中发生的离子反应方程式________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:X(g)+2Y(g)![]() 3Z(g) △H=-akJ·mol-1(a>0),下列说法不正确的是
3Z(g) △H=-akJ·mol-1(a>0),下列说法不正确的是
A. 0.1molX和0.2molY充分反应生成Z的物质的量一定小于0.3mol
B. 达到化学平衡状态时,X、Y、Z的浓度不再发生变化
C. 达到化学平衡状态时,反应放出的总热量可达a Kj
D. 升高反应温度,逆反应速率增大,正反应速率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要配制0.5molL-1的烧碱溶液480mL,根据溶液配制的过程,回答下列问题:
(1)实验中除了托盘天平(带砝码)、药匙、烧杯、量筒和玻璃棒外,还需要的其他玻璃仪器有:___和___。
(2)根据计算得知,所需NaOH固体的质量为___g。
(3)实验开始前,需要先___。
(4)配制溶液的过程中,有以下操作,其中正确的是___(填代号)。
A.将氢氧化钠固体放在纸片上称量;
B.在烧杯中溶解氢氧化钠固体后,立即将溶液倒入容量瓶中;
C.将溶解氢氧化钠的烧杯用蒸馏水洗涤2~3次,并将洗涤液转移到容量瓶中
(5)下列各项操作中,可能导致实际浓度偏高的是___(填选项字母)
A.称量NaOH固体时,砝码和物质的位置对调
B.向容量瓶中转移时,不慎洒出
C.NaOH溶解时放出大量的热,未及冷却立即配制溶液
D.定容时,仰视容量瓶的刻度线
E.定容时,加水超过刻度线,再用胶头滴管吸出多余的部分
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com