
【题目】亚氯酸钠(NaClO2)是重要漂白剂。某化学兴趣小组同学展开对亚氯酸钠(NaClO2)的研究。
实验Ⅰ:制取NaClO2晶体
已知:NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO23H2O,高于38℃时析出的晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。Ba(ClO2)2可溶于水。
利用下图所示装置进行实验。

(1)装置②中产生ClO2气体的化学方程式为 。
(2)从装置④反应后的溶液获得晶体NaClO2的操作步骤为:
①减压,55℃蒸发结晶;②趁热过滤;③ ;④低于60℃干燥,得到成品。过滤用到的玻璃仪器有 。
(3)设计实验检验所得NaClO2晶体是否含有杂质Na2SO4,操作是: 。
(4)反应结束后,关闭K2、打开K1,装置①的作用是 ;如果撤去D中的冷水浴,可能导致产品中混有的杂质是 。
实验Ⅱ:测定某亚氯酸钠样品的纯度。
设计如下实验方案,并进行实验:
①准确称取所得亚氯酸钠样品m g于烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应(已知:ClO2-+ 4I-+4H+ =2H2O+2I2+Cl-)。将所得混合液配成100mL待测溶液。
②移取25.00mL待测溶液于锥形瓶中,用c molL-1 Na2S2O3标准液滴定,至滴定终点。重复2次,测得消耗标准溶液的体积的平均值为V mL(已知:I2 +2S2O32-=2I-+S4O62-)。
(5)滴定中使用的指示剂是 ,达到滴定终点时的现象为 。
(6)样品中NaClO2的质量分数为 (用含m、c、V的代数式表示,式量:NaClO2 90.5)。
【答案】(1)2NaClO3+Na2SO3+H2SO4==2ClO2↑+2Na2SO4+H2O
(2)用38℃~60℃的温水洗涤 烧杯、漏斗、玻璃棒
(3)取晶体少许溶于水,先加足量的盐酸,再加BaCl2溶液,若产生白色沉淀,则说明含有SO42-。
(4)吸收装置B中多余的ClO2和SO2;NaClO3和NaCl
(5)淀粉溶液;溶液由蓝色变为无色且半分钟不变色
(6)![]() 或
或 ![]()
【解析】
试题分析:(1)根据反应物NaClO3、Na2SO3、H2SO4,生成物为ClO2和2Na2SO4,配平方程式为2NaClO3 + Na2SO3 + H2SO4=2ClO2 + 2Na2SO4 + H2O;
(2)因为NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·3H2O,高于38℃时析出晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl,若要得到NaClO2晶体,需在38-60℃得到晶体,故操作为趁热过滤并用38-60℃的温水洗涤;过滤用到的玻璃仪器有烧杯、漏斗、玻璃棒;
(3)SO42-的检验方法是加入足量的盐酸酸化,再加BaCl2溶液,根据是否有沉淀判断。故操作是:取晶体少许溶于水,先加足量的盐酸,再加BaCl2溶液,若产生白色沉淀,则说明含有SO42-;
(4)本实验产生污染性气体,直接排放会污染环境,故需要尾气处理,反应结束后,关闭K2、打开K1,装置①的作用是吸收装置B中多余的ClO2和SO2;如果撤去D中的冷水浴,可能导致产品中混有的杂质是NaClO3和NaCl;
(5)有碘单质参和生成的反应,一般采用淀粉溶液做指示剂,该反应是Na2S2O3标准液滴定碘,终点溶液由蓝色变为无色且半分钟内不变色;
(6)计算时一般找出关系式,由此进行计算,关系式为ClO2-——2I2——4S2O32-
n(ClO2-)= 1/4 n(S2O32-)=1/4×c×V×10-3×4=cV×10-3mol
m(NaClO2)=cV×10-3×90.5
该样品中NaClO2的质量分数为cV×10-3×90.5÷m=![]()


 名题金卷系列答案
名题金卷系列答案科目:高中化学 来源: 题型:
【题目】高锰酸钾可用于生活消毒,是中学化学常见的氧化剂。工业上,用软锰矿制高锰酸钾的流程如下:

请回答下列问题:
(1)该生产中需要纯净的CO2气体.写出实验室制取CO2的化学方程式 。
(2)KMnO4稀溶液是一种常用的消毒剂.其消毒原理与下列物质相同的是 (填字母).
a.75%酒精 b.双氧水 c.苯酚 d. 84消毒液(NaClO溶液)
(3)写出二氧化锰和氢氧化钾熔融物中通入空气时发生的主要化学反应的方程式: 。
(4)上述流程中可以循环使用的物质有 、 (写化学式).
(5)测定高锰酸钾样品纯度采用硫酸锰滴定:向高锰酸钾溶液中滴加硫酸锰溶液,产生黑色沉淀。当溶液由紫红色刚好褪色且半分钟不恢复,表明达到滴定终点。写出该反应的离子方程式: 。
(6)已知:常温下,Ksp[Mn(OH)2]=2.4×10-13。工业上,调节pH可以沉淀废水中Mn2+,当pH=10时,溶液中c(Mn2)= ___________________。
(7)操作Ⅰ的名称是 ;操作Ⅱ根据KMnO4和K2CO3两物质在溶解性上的差异,采用 (填操作步骤)、趁热过滤得到KMnO4粗晶体.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W、V、U是短周期的主族元素,原子序数依次增大。X与V同主族,且与W都能形成A2B、A2B2型化合物;Z、W的单质常温下均为无色气体;Y与U同主族且Y原子的L层电子数是K层电子数的2倍。试回答下列问题:
(1)写出U元素在周期表中的位置 ;V离子结构示意图为 ;YW2的电子式 。
(2)Y、U的简单氢化物的稳定性由弱到强的顺序是 。
(3)V的最高价氧化物的水化物不能使用玻璃塞试剂瓶盛放的原因是 。(用化学方程式表示)
(4)由X、Z组成的一种化合物化学式为ZX5,其各原子均达到同周期稀有气体原子的稳定结构,该物质属于 (填“离子”或“共价”)化合物。
(5)X、Y、Z、W四种元素(按顺序)可组成原子个数比为5:1:1:3的化合物,该化合物的稀溶液与足量氢氧化钠溶液在加热条件下反应的离子方程式为: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用铝土矿(主要成分为主要成份是Al2O3,还含有SiO2和Fe2O3)提取氧化铝并冶炼Al的操作过程如下:

(1)滤渣A是 ,滤渣B是 。
(2)过程I、II、III的分离操作的名称是 。
(3)过程IV中灼烧时盛放药品的仪器名称是 ,发生反应的化学方程式是 。
(4)过程III中发生反应生成滤渣C的离子方程式表示为 。
(5)取滤液B100mL,加入1molL-1盐酸200mL时,沉淀量达到最大且质量为11.7g。则溶液B中c(Al[(OH)4]-)= ,c(Na+)> mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛铁矿的主要成分为FeTiO3(可表示为FeO·TiO2),含有少量MgO、CaO、SiO2等杂质。利用钛铁矿制备锂离子电池电极材料(钛酸锂Li4Ti5O12和磷酸亚铁锂LiFePO4)的工艺流程如下图所示:
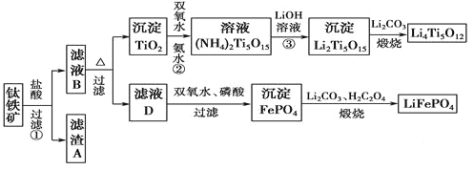
已知:FeTiO3与盐酸反应的离子方程式为:FeTiO3+4H++4Cl-===Fe2++TiOCl42-+2H2O。
(1)化合物FeTiO3中铁元素的化合价是 。
(2)滤渣A的成分是 。
(3)滤液B中TiOCl42-转化生成TiO2的离子方程式为 。
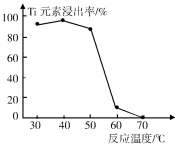
(4)反应②中固体TiO2转化成(NH4)2Ti5O15溶液时,Ti元素的浸出率与反应温度的关系如图所示。反应温度过高时,Ti元素浸出率下降的原因是 。
(5)写出由滤液D生成FePO4的离子方程式 。
(6)由滤液D制备LiFePO4的过程中,所需17%双氧水与H2C2O4的质量比是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天津是我国研发和生产锂离子电池的重要基地。锂离子电池正极材料是含锂的二氧化钴(LiCoO2),充电时LiCoO2中Li被氧化,Li+迁移并以原子形式嵌入电池负极材料碳(C6)中,以LiC6表示。电池反应为CoO2+LiC6![]() LiCoO2+C6,下列说法正确的是( )
LiCoO2+C6,下列说法正确的是( )
A. 充电时,电池的负极反应为LiC6-e-Li++C6
B. 放电时,电池的正极反应为CoO2+Li++e-LiCoO2
C. 羧酸、醇等含活泼氢的有机物可用作锂离子电池的电解质
D. 锂离子电池的比能量(单位质量释放的能量)低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学—选修3:物质结构与性质]
(1)下列有关微粒间作用力的说法正确的是
A.配位键的强度有大有小,所以有的配合物很稳定,有的很不稳定
B.水加热到很高的温度都难以分解是因为水分子间存在氢键
C.壁虎能在光滑的墙壁上行走是因为壁虎脚底的细毛与物体表面的分子产生分子间作用力
D.互为手性异构本的分子具有完全相同的组成和原子排列,所以生产手性药物时无需分离手性异构体
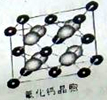
(2)判断下列哪个模型代表金属晶体锌的堆积方式 。

(3)第四周期未成对电子数最多的P区元素的元素符号是 ,核外电子占据
个原子轨道。
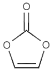
(4)碳酸亚乙烯酯是锂离子电池低温电解液的重要添加剂,其结构如图。碳原子的杂化方式有 ,分子中σ键与π键之比为 。
(5)比较NH2-和NH3的键角∠HNH的大小:NH2- NH3(填“﹥”“=”“﹤”),请用价层电子对互斥规解释: 。
(6)SO32-中硫原子的价层电子对互斥模型是 ;写出一种与SO32-互为等电子体的分子 。
(7)SiC晶胞与金刚石晶胞相似,设晶胞边长为a cm,碳原子直径为b cm,硅原子直径为c cm,则该晶胞的空间利用率为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[物质结构与性质]
已知碳元素能形成多种金属碳化物,如碳化钙,俗称为电石。
(1)电石(CaC2)是用CaO与焦炭在电炉中加强热反应生成的,写出此反应的化学方程式 ,CaC2中含有化学键的类型为 ,C22-与N2互为等电子体,C22-的电子式可表示为 ,其中σ键和π键数目之比为 。
(2)已知MgO、CaO的熔点分别为2852℃、2614℃,分析熔点差异的原因是 。
(3)苯丙氨酸是一种重要的氨基酸,其结构如图所示,分子中第一电离能最大的原子价电子排布式是 ,其中碳原子的杂化方式有 。
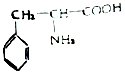
(4)已知CaF2晶体(如图,Ca2+处于面心)的密度为ρg/cm3,NA为阿伏加德常数,相邻的两个Ca2+的核间距为a cm,则CaF2的摩尔质量(M)可以表示为 g/mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依曲替酯是一种皮肤病用药,它可以由原料X经过多步反应合成。
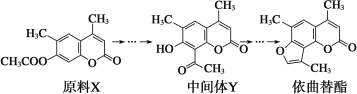
下列说法不正确的是( )
A.原料X与中间体Y互为同分异构体
B.原料X可以使酸性KMnO4溶液褪色
C.中间体Y能发生加成、取代、消去、氧化、还原反应
D.1 mol依曲替酯能与2 mol NaOH发生反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com