
【题目】下列叙述合理的是( )
A.金属材料都是导体,非金属材料都是绝缘体
B.合金的熔点比组成它的各种成分的熔点都高
C.水电站把机械能转化成电能,而核电站把化学能转化成电能
D.我国规定自2008年6月1日起,商家不得无偿提供塑料袋,目的是减少“白色污染”
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】原电池中, B极逐渐变粗,A极逐渐变细,C为电解质溶液,则A、B、C应是下列各组中的( )
A.A是Zn,B是Cu,C为稀硫酸
B.A是Cu,B是Zn,C为稀硫酸
C.A是Fe,B是Ag,C为稀AgNO3溶液
D.A是Ag,B是Fe,C为稀AgNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关甲烷分子结构的说法中,错误的是 ( )
A.甲烷分子中含有4个C—H共价健
B.甲烷分子中C—H共价键的夹角为109°28'
C.甲烷是正四面体结构
D.甲烷是一种直线型分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20mL 0.2mol/L H2A溶液中滴加0.2 mol/L NaOH 溶液。有关微粒的物质的量变化如下图(其中I代表H2A,II代表HA-,III代表A2-)根据图示判断,下列说法正确的是

A. 当V(NaOH)="20" mL时,溶液中离子浓度大小关系:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
B. 等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水大
C. 欲使NaHA溶液呈中性,可以向其中加入酸或碱
D. 向NaHA溶液加入水的过程中,pH可能增大也可能减少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的镁、铜合金加入到稀硝酸溶液中,两者恰好完全反应,假设反应过程中还原产物全部是NO,向所得溶液中加入物质的量浓度为3molL﹣1的NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1g,则下列有关叙述中正确的是( )
A.开始加入合金的质量可能为3.6g
B.参加反应的硝酸的物质的量为0.1mol
C.沉淀完全时消耗NaOH溶液的体积为100mL
D.溶解合金时产生NO的体积为2.24L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【改编题】不规范的实验操作都有安全隐患,进入高中后化学实验明显增多,作为高中生实验时要规范操作。请改正下列各操作中的错误(在下图对应的横线上用文字简要回答)。
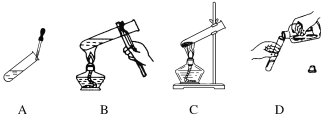
A.________________________________________________________________________
B.________________________________________________________________________
C.________________________________________________________________________
D.________________________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属在现代社会中发挥着巨大的作用,铝的化合物在工农业生产及人们的日常生活中也具有广泛地作用。
(1)若将铝溶解,下列试剂中最好选用________(填选项字母)。
A.浓硫酸B.稀硫酸C.稀硝酸
(2)以铝土矿(主要成分是Al2O3,杂质有SiO2、Fe2O3等)为原料,采用拜耳法生产Al2O3的流程如下图所示:
①Al2O3可用于电解制Al,电解时需加入冰晶石(Na3AlF6)作为助熔剂,用NaF和Al2(SO4)3反应制备冰晶石的化学方程式为________________;电解时用石墨作阳极,温度维持在950~970℃,阳极需定期更换,其原因为________________________。
②赤泥中铝硅酸钠的化学式可表示为:3Na2O·3Al2O3·5SiO2·5H2O,则滤液I的主要成分是________________;铝土矿的品位常用铝硅比(A/S,即矿石中Al2O3与SiO2的质量比)来衡量。某种铝土矿的A/S=10.2,则加入足量NaOH溶液后铝的理论溶出率为________________。
③该生产过程中,需向沉淀池中加入过量的X,该反应的离子方程式为________________。
(3)铍(Be)与铝元素相似,其氧化物及氢氧化物具有两性,请写出BeO与盐酸反应的离子方程式,Be(OH)2溶于NaOH溶液的化学方程式为:Be(OH)2+2NaOH=Na2BeO2+2H2O,往10.0mL1.00mol·L-1的Be(NO3)2溶液中逐滴加入等浓度的NaOH溶液,请在以下坐标图中画出沉淀量随NaOH溶液加入量的变化图:

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为周期表前四周期的一小部分,A、B、C、D、E的位置关系如图所示.其中B元素的最高价是负价绝对值的3倍,它的最高氧化物中含氧60%,回答下列问题:

(1)C位于第 周期,第 族.
(2)B的离子结构示意图 .A单质的电子式为 .
(3)D、B、E的三种元素形成的单质中,氧化性最强的是: (填化学式).A、B、的气态氢化物热稳定性最强的是 (填化学式).
(4)D的气态氢化物的结构式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com