
A、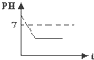 |
B、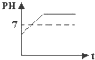 |
C、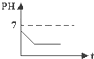 |
D、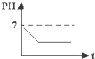 |
| ||
| ||


科目:高中化学 来源: 题型:
| A、①③⑤ | B、②④⑤ |
| C、②③ | D、③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、100 mL 2 mol/L的盐酸与锌反应时,加入适量的氯化钠溶液,生成氢气的速率不变 |
| B、用铁片和稀硫酸反应制取氢气,改用铁片和浓硫酸可以加快产生氢气的速率 |
| C、在做草酸与高锰酸钾的反应时,加入少量硫酸锰固体可加快溶液褪色速率 |
| D、汽车尾气中的CO和NO可以缓慢反应生成N2和CO2,为了加快反应速率,实际生活中使用了增大压强或升高温度的方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由pH=l的CH3COOH溶液与pH=13的NaOH溶液等体积混合而成 |
| B、由1mL0.1 mol?L-1CH3COOH溶液与10mL 1mol?L-1的NaOH溶液混合而成 |
| C、由0.1mol?L-1的CH3COOH溶液与0.1mol?L-1的NaOH溶液等体积混合而成 |
| D、由0.1mol?L-1的CH3COONa溶液与0.1mol?L-1的NaOH溶液等体积混合而成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、23g Na变为Na+时失去的电子数为NA |
| B、32g O2中含有的分子数为2NA |
| C、在标准状况下22.4L H2中含有的氢分子数为NA |
| D、1 L0.1 mol/LNa2CO3溶液中含有的钠离子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2CO3=Na++CO32- |
| B、Ba(OH)2=Ba2++OH2- |
| C、H2SO4=H2++SO42- |
| D、NaCl=Na++Cl- |
| E、NaCl=Na++Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、+(a+b)kJ?mol-1 |
| B、+(a-b)kJ?mol-1 |
| C、-(a-b)kJ?mol-1 |
| D、-(a+b)kJ?mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com