
����Ŀ��Ϊ�˳�ȥ�����е�Ca2����Mg2����SO![]() ����ɳ���ɽ���������ˮ��Ȼ������������������
����ɳ���ɽ���������ˮ��Ȼ������������������
�ٹ��ˡ��ڼӹ���NaOH��Һ���ۼ�����HCl���ܼӹ���Na2CO3��Һ���ݼӹ���BaCl2��Һ
ͨ���̲��������ε��ᴿ�����������ĸ�ʵ��ش��������⣺
(1)�����岽�����У������е���________��
(2)ʵ���ҽ���NaCl��Һ������ʱ��һ�������²������̣�
�ٹ̶���Ȧλ�á� �ڷ��þƾ��ơ� �۷���������(��������ʢ��NaCl��Һ)�� �ܼ��Ƚ��衡��ֹͣ����
��ȷ�IJ���˳��Ϊ___________________��
(3)�ڴ��ξ���һϵ�в��������Һ�еμӹ�������Na2CO3��Һ�������ⲽ������Ŀ����___________________________________________���ж�Na2CO3��Һ�Ѿ������ķ�����_________________________________________________________________��
(4)ʵ�����ォ�����Ƴɾ��εĹ����У����ܽ⡢���ˡ�������������IJ����ж�Ҫ�õ����������ֱ�˵���������������ʹ�ò�������Ŀ�ģ�
�ܽ�ʱ��_________________________________________��
����ʱ��_________________________________________��
����ʱ��_________________________________________��
���𰸡� �� �ڢ٢ۢܢ� ��ȥCa2���Լ�����Ĺ���Ba2�� ȡ�ϲ���Һֱ�ӵ���Na2CO3��Һ�����ٲ������� ���裬�����ܽ� ����(��ʹ����Һ���ز���������©������ֹ����) ���裬��ֹ��ֲ�����Һ�λ���ɽ�
�������������к��е�Ca2����Mg2����SO42-����ɳ�����ʣ�����������ˮ���������BaCl2��Һ�Գ�ȥSO42-����ͬʱ������������Ba2+�����������Na2CO3��Һ�Գ�ȥBa2+��Ca2��������BaCl2��Һһ������Na2CO3��Һǰ�棬����NaOH��Һ��Ŀ�ij�ȥMg2�������ˣ����õ��ij���ȫ���˳������õ�����Һ�Ǻ�NaCl��Na2CO3��NaOH�ȵĻ�������HCl���Խ�һ����ȥCO32-��OH-���������ӣ��õ���Ϊ������NaCl��Һ���������һ��Ϊ����
��2������NaCl��Һʱ�����մ��µ��ϵ�˳���ȷ��þƾ��ƣ��ٹ̶���Ȧλ�ã�����������ʼ���Ƚ��裬��ʣ������Һ��ʱֹͣ���ȣ�������ȷ�IJ���˳��Ϊ�ڢ٢ۢܢ�
��3���ڳ��Ӳ����м������BaCl2��Һ�Գ�ȥSO42-����ͬʱ������������Ba2+�����������Na2CO3��Һ�Գ�ȥCa2��������Ba2+���ж�Na2CO3��Һ�Ѿ������ķ�������ȡ�ϲ���Һֱ�ӵ���Na2CO3��Һ�����ٲ������� ��
��4�����ܽ�ʱ�ò��������Ͻ����Լӿ��ܽ����ʣ�����ʱʹ���˻����Һ�����Ų���������©����������������������ֹ����©������������������Ҫ�ò��������Ͻ��裬��ֹ��ֲ�������ɵ�Һ��ɽ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��C��N��S����Ҫ�ķǽ���Ԫ�أ���Ҫ��ش��������⣺
��1���̵����к��е�CO��SO2����Ҫ����Ⱦ����ڴ��������½�����ת��ΪS(s)��CO2���˷�Ӧ���Ȼ�ѧ����ʽΪ______________________________________________________��
��֪��CO(g)+1/2O2(g)=CO2(g) ��H=��283.0 kJ��mol��1
S(s)+O2(g)=SO2(g) ��H=��296.0 kJ��mol��1��
��2����ס���������Ϊ1 L���ܱ������У��ֱ����5 mol SO2��3 mol O2��������Ӧ��2SO2(g)+
O2(g)![]() 2SO3(g) ��H��0�����������¶�ΪT1�������·�Ӧ���ﵽƽ��ʱSO3�����ʵ���Ϊ4.5 mol�����������¶�ΪT2�������·�Ӧ���ﵽƽ��ʱSO3�����ʵ���Ϊ4.6 mol����T1___T2�����������������������������з�Ӧ��ƽ�ⳣ��K=_____________________��
2SO3(g) ��H��0�����������¶�ΪT1�������·�Ӧ���ﵽƽ��ʱSO3�����ʵ���Ϊ4.5 mol�����������¶�ΪT2�������·�Ӧ���ﵽƽ��ʱSO3�����ʵ���Ϊ4.6 mol����T1___T2�����������������������������з�Ӧ��ƽ�ⳣ��K=_____________________��
��3����ͼ��ʾ��A�Ǻ��ݵ��ܱ�������B��һ������ɱ�ij������ҡ����ֺ��£��ر�K2���ֱ�1 mol N2��3 mol H2ͨ��K1��K3����A��B�У������ķ�ӦΪ��N2(g)+3H2(g) ![]() 2NH3(g)����ʼʱA��B�������ͬ��Ϊa L��
2NH3(g)����ʼʱA��B�������ͬ��Ϊa L��

������ʾ��ͼ����˵��A�����з�Ӧ�ﵽƽ��״̬������˵��B�����з�Ӧ�ﵽƽ��״̬����______��

������A�з�Ӧ����ƽ��ʱ����ʱ��t s���ﵽƽ���������ѹǿ��Ϊԭ����5/6����ƽ����Ӧ������(H2)=___________________________��
��4����0.1 mol�����ֱ�ͨ��1 L pH=1�����ᡢ����ʹ�����Һ�У���ȫ��Ӧ������Һ��NH4+����Ũ�ȷֱ�Ϊc1��c2��c3��������Ũ�ȴ�С�Ĺ�ϵΪ____________������c1��c2��c3�ͣ�������=����ʾ������֪�������Һ�����ԣ�������CH3COOH��Ka=1��10��5 mol��L��1������¶���NH4Cl��ˮ�ⳣ��K h Ϊ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A.ʯ���ǻ��������Ǵ�����
B.�е�:����>ú��>����
C.ֱ�����ͺ��ѻ����ͳɷ���ȫ��ͬ
D.ʯ�ͷ������������̣�ʯ���ѻ��ǻ�ѧ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪723Kʱ��2SO2��g��+O2��g��![]() 2SO3��g����H=��QkJ/mol������ͬ�����£���һ�ܱ�������ͨ��2mol SO2��1mol O2���ﵽƽ��ʱ�ų�������ΪQ1kJ������һ�����ͬ���ܱ�������ͨ��1mol SO2��0.5mol O2���ﵽƽ��ʱ�ų�������ΪQ2kJ����Q1��Q2��Q����Ĺ�ϵ�ǣ� ��
2SO3��g����H=��QkJ/mol������ͬ�����£���һ�ܱ�������ͨ��2mol SO2��1mol O2���ﵽƽ��ʱ�ų�������ΪQ1kJ������һ�����ͬ���ܱ�������ͨ��1mol SO2��0.5mol O2���ﵽƽ��ʱ�ų�������ΪQ2kJ����Q1��Q2��Q����Ĺ�ϵ�ǣ� ��
A��Q2=![]() B��Q2��
B��Q2��![]() C��Q2��Q1��Q D��Q=Q1��Q2
C��Q2��Q1��Q D��Q=Q1��Q2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������±��е���Ϣ�жϣ�����˵���������

A. �ڢ��鷴Ӧ����������ΪO2
B. �ڢ��鷴Ӧ��C12��FeBr2�����ʵ���֮��С�ڻ����1��2
C. �ڢ��鷴Ӧ������3mol C12��ת��6mol����
D. ��������ǿ������˳��ΪC1O3- >C12>Fe3+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���NaOH��Һ�ֱ�μӵ�����һԪ����HA��HB�У����ֻ����Һ��pH������Ũ�ȱ仯�Ĺ�ϵ��ͼ��ʾ������������ȷ����

A. Ka(HA)��������Ϊ10-5
B. ��NaOH��Һ��HB���������ʱ��c(B-)<c(HB)
C. ��Ũ�ȵ�NaA��NaB��Һ�У�ˮ�ĵ���̶ȣ�NaA<NaB
D. ��Ũ�ȵ�HB��NaA�Ļ����Һ�У�c(Na+)>c(A-)>c(B-)>c(OH-)>c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������(Na2S2O8)������Ư�����������ȡ�ij�о�С��������ͼװ���Ʊ�Na2S2O8��̽��������(���ȼ��г�������ȥ)��
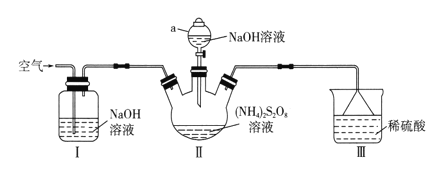
��֪����(NH4)2S2O8+2NaOH![]() Na2S2O8+2NH3+2H2O
Na2S2O8+2NH3+2H2O
��2NH3+3Na2S2O8+6NaOH![]() 6Na2SO4+N2+6H2O
6Na2SO4+N2+6H2O
(1)����a��������________________��װ��I��NaOH��Һ��������___________��
(2)װ��II������Ӧ��ͬʱ����Ҫ����ͨ�������Ŀ����_______________________��
(3)װ��III��������__________________________��
(4)Na2S2O8��Һ��ͭ��Ӧֻ���������Σ��ҷ�Ӧ������졣
�ٸ÷�Ӧ�Ļ�ѧ����ʽΪ___________________________��
��ijͬѧ�ƲⷴӦ��������ԭ����������ɵ�Cu2+�Է�Ӧ������á����ʵ�鷽����֤���Ʋ��Ƿ���ȷ___________��(��ѡ�Լ���Cu��Na2S2O8��Һ��CuSO4��Һ��Cu(NO3)2��Һ������ˮ)
(5)�ⶨ��Ʒ���ȣ���ȡ0.2500g��Ʒ��������ˮ�ܽ⣬�������KI����ַ�Ӧ���ٵμӼ���ָʾ������0.1000mol/LNa2S2O8����Һ�ζ����ﵽ�ζ��յ�ʱ�����ı���Һ�����Ϊ19.50mL��(��֪��I2+2S2O32-=S4O62-+2I-)
��ѡ�õ�ָʾ����____________���ﵽ�ζ��յ��������______________________��
����Ʒ�Ĵ���Ϊ___________%��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. �����£�1mLpH=1��������100mLNaOH��Һ��Ϻ���Һ��pH=7����NaOH��Һ��pH=11
B. 25��ʱ��0.1mol L-1��HA��Һ��![]() = 1��10-8�������Һ����ˮ�������c(H+)=l��10-3mol��L-1
= 1��10-8�������Һ����ˮ�������c(H+)=l��10-3mol��L-1
C. 25��ʱ������pH��ͬ������ROH��MOH(ǰ�ߵĵ���ƽ�ⳣ��Kb��С)����ˮϡ�ͺ���Һ��pH����ͬ�������ϡ�͵ı�������
D. 25��ʱ��BaSO4��ˮ���г������ܽ��ƽ�⣺BaSO4(s)![]() Ba2+(aq)+SO42-(aq)��˵��BaSO4���������
Ba2+(aq)+SO42-(aq)��˵��BaSO4���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������£���һ���������ܱ������г���2molA��1molB���������з�Ӧ��2A(g)+B(g)![]() 2C(g) ��H< 0���ﵽƽ�����t1ʱ�̸ı���������ѧ��Ӧ������ʱ��仯��ͼ�����ж�t1ʱ�̸ı��������Ʋ�����ȷ����
2C(g) ��H< 0���ﵽƽ�����t1ʱ�̸ı���������ѧ��Ӧ������ʱ��仯��ͼ�����ж�t1ʱ�̸ı��������Ʋ�����ȷ����
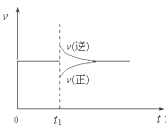
A������ѹǿ���䣬���߷�Ӧ�¶�
B�������¶Ȳ��䣬�����������
C�������¶Ⱥ�����������䣬����1molC(g)
D�������¶Ⱥ�ѹǿ���䣬����1molC(g)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com