
����Ŀ�������£��������Ϊ1 mL��Ũ�Ⱦ�Ϊ0.10 mol/L��XOH��X2CO3��Һ�ֱ��ˮϡ�������ΪV mL��pH��lg V�ı仯�����ͼ��ʾ��������������ȷ����

A. XOH������
B. pH=10��������Һ�е�c(X+):XOH>X2CO3
C. ��֪H2CO3�ĵ���ƽ�ⳣ��Ka1Զ����Ka2����Ka2ԼΪ1.0��1010.2
D. ��lg V=2ʱ����X2CO3��Һ���¶����ߣ���Һ������ǿ���� ��С
��С
���𰸡�C
��������
A������ͼ֪��0.1mol/L��XOH��pH=13��˵��XOH��Һ��c��OH-��=c��XOH����
B��XOH��ǿ����Һ��X2CO3��ǿ����������Һ��Ҫʹ������Һ��pH��ȣ���c��XOH����c��X2CO3�����ٽ�������غ��жϣ�
C.0.10mol/LX2CO3��Һ��pH=11.6�������Һ��c��OH-��=c��HCO3-��=![]() mol/L=10-2.4 mol/L��c��CO32-��=0.1mol/L��Kh1=
mol/L=10-2.4 mol/L��c��CO32-��=0.1mol/L��Kh1=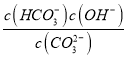 =
=![]() ����Ka2=
����Ka2=![]() =
=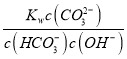 ��
��
D����lgV=2ʱ������Һ�������Ϊԭ����100���������¶ȣ��ٽ�ˮ�⣬��һ��ˮ��̶�ԶԶ���ڵڶ�����������Һ��c��CO32-����С��c��HCO3-������
A������ͼ֪��0.1mol/L��XOH��pH=13��˵��XOH��Һ��c��OH-��=c��XOH����XOH��ȫ���룬Ϊǿ����ʣ�ѡ��A����
B��XOH��ǿ����Һ��X2CO3��ǿ����������Һ��Ҫʹ������Һ��pH��ȣ���c��XOH����c��X2CO3�����ٽ�������غ��c��X+����XOHС��X2CO3��ѡ��B����
C.0.10mol/LX2CO3��Һ��pH=11.6�������Һ��c��OH-��=c��HCO3-��=![]() mol/L=10-2.4 mol/L��c��CO32-��=0.1mol/L��Kh1==
mol/L=10-2.4 mol/L��c��CO32-��=0.1mol/L��Kh1==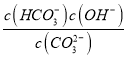 =
=![]() ����Ka2=
����Ka2=![]() =
=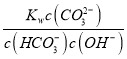 =
=![]() =1.0��10-10.2��ѡ��C��ȷ��
=1.0��10-10.2��ѡ��C��ȷ��
D����lgV=2ʱ������Һ�������Ϊԭ����100���������¶ȣ��ٽ�ˮ�⣬��һ��ˮ��̶�ԶԶ���ڵڶ�����������Һ��c��CO32-����С��c��HCO3-����������![]() ����ѡ��D����
����ѡ��D����
��ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ʵ������������ܵó���Ӧ���۵���(����)
ѡ�� | ʵ����� | ���� | ���� |
A | SO2����ͨ����з�̪��NaOH��Һ�� | ��Һ��ɫ��ȥ | SO2����Ư���� |
B | ������NO2���ܱղ������������ˮ�� | �������ɫ���� | 2NO2(g) |
C | ij��ɫ��ҺX�м�����ۣ�KI��Һ | ��Һ�����ɫ | ��ҺX�к���Br2 |
D | ��ˮ�Ҵ��м���Ũ���ᣬ���ȣ�����������Yͨ������KMnO4��Һ | ��Һ��ɫ��ȥ | ����Y�к�����ϩ |
A. AB. BC. CD. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��pH��1����������ҺA��B��1mL���ֱ��ˮϡ�͵�1000mL����pH����Һ����Ĺ�ϵ��ͼ������˵����ȷ���ǣ� ��
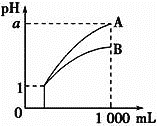
����a��4����A��B��������
��ϡ�ͺ�A����Һ�����Ա�B����Һǿ
����a��4����A��ǿ�ᣬB������
��A��B��������Һ�����ʵ���Ũ��һ�����
A. �٢�B. �ڢ�C. �ڢ�D. �٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������е�H2Sͨ�������ȷֽ����ȡ������2H2S(g)![]() 2H2(g)��S2(g)������3L�ܱ������У����Ʋ�ͬ�¶Ƚ���H2S�ֽ�ʵ�顣
2H2(g)��S2(g)������3L�ܱ������У����Ʋ�ͬ�¶Ƚ���H2S�ֽ�ʵ�顣
��1��ij�¶�ʱ����÷�Ӧ��ϵ��������1.3lmol����Ӧ1 min�������Ϊl.37mol,��tmin ��H2����������Ϊ___________��
��2��ij�¶�ʱ��H2S��ת���ʴﵽ���ֵ��������_____________(ѡ����)��
a�������ѹǿ�������仯 b��������ܶȲ������仯
c��![]() �������仯 d����λʱ����ֽ��H2S�����ɵ�H2һ����
�������仯 d����λʱ����ֽ��H2S�����ɵ�H2һ����
��3��ʵ��������ͼ��ͼ������a��ʾH2S��ƽ��ת�������¶ȹ�ϵ������b��ʾ��ͬ�¶��¡���Ӧ������ͬʱ����δ�ﵽ��ѧƽ��ʱH2S��ת���ʡ��÷�ӦΪ_____��Ӧ������ȡ������ȡ���������b���¶ȵ����ߣ�������aͨ����ԭ����_________��������������������£����Ҫ���H2������������ɲ�ȡ��һ�ִ�ʩ��________��

��4��ʹ1LH2S��20L������������O2�������Ϊ0.2����ȫ��Ӧ��ָ������£��������������______L ����2gH2S��ȫȼ�պ����ɶ��������ˮ������ͬʱ�ų�29.4 kJ���������÷�Ӧ���Ȼ�ѧ����ʽ��__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����t ��ʱ��AgBr��ˮ�еij����ܽ�ƽ��������ͼ��ʾ����֪t ��ʱAgCl��Ksp��4��10��10 mol2��L��2������˵������ȷ����

A.��t ��ʱ��AgBr��KspΪ4.9��10��13 mol2��L��2
B.��AgBr������Һ�м���NaBr���壬��ʹ��Һ��b�㵽c��
C.ͼ��a���Ӧ����AgBr�IJ�������Һ
D.��t ��ʱ��AgCl(s)��Br��(aq)![]() AgBr(s)��Cl��(aq)��ƽ�ⳣ��K��816
AgBr(s)��Cl��(aq)��ƽ�ⳣ��K��816
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ������X����ij�ܱ������У�������Ӧ��2X(g)![]() 3Y(g)+Z(g)�����������X�����ʵ����������¶ȹ�ϵ��ͼ��ʾ�������ƶ���ȷ����()��
3Y(g)+Z(g)�����������X�����ʵ����������¶ȹ�ϵ��ͼ��ʾ�������ƶ���ȷ����()��
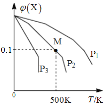
A. �����¶ȣ��÷�Ӧƽ�ⳣ��K��С
B. ѹǿ��С��P3��P2��P1
C. ƽ�������Ч����ʹƽ��Ħ����������
D. �ڸ�������M��Xƽ��ת����Ϊ9/11
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�ʵ����1.0mol/L NH4HCO3 ��ҺpH=8.0��ƽ��ʱ̼�ķֲ�ϵ��������̼����Ũ��ռ��̼������Ũ��֮�͵ķ�������pH�Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ�������
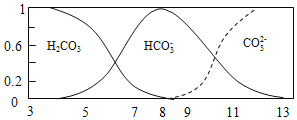
A. �����£�Kb(NH3H2O)>Ka1(H2CO3)>Ka2(H2CO3)
B. pH=13ʱ����Һ�в�����HCO3-��ˮ��ƽ��
C. pH��8��11 ʱ������pHֵ������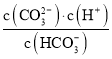 ����
����
D. pH=3ʱ����c(NH4+)+c(NH3H2O)=c(HCO3-)+c(H2CO3)+c(CO32-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ҵ��ˮ����Ҫ����Cr3����ͬʱ������������Fe3����Fe2����Al3����Ca2����Mg2���ȣ������Խ�ǿ��Ϊ�������ã�ͨ�������������̴�����
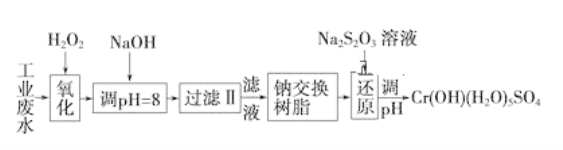
ע�����������ӳ�����������������ʽ��ȫ����ʱ��Һ��pH���±���
�������� | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 | Al(OH)3 | Cr(OH)3 |
pH | 3.7 | 9.6 | 11.1 | 8 | 9(>9�ܽ�) |
��1�����������пɴ���H2O2������Լ���________(�����)��
A��Na2O2 B��HNO3 C��FeCl3 D��KMnO4
��2������NaOH��Һ������ҺpH��8ʱ����ȥ��������________����֪�����ӽ�����֬��ԭ����Mn����nNaR��MRn��nNa�����˲�������������ȥ������������__________��
A��Fe3��B��Al3��C��Ca2��D��Mg2��
��3����ԭ�����У�ÿ����0.8 mol Cr2O72-ת��4.8 mol e�����÷�Ӧ���ӷ���ʽΪ____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
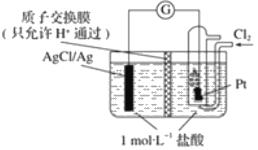
����Ŀ��ijԭ���װ����ͼ��ʾ������ܷ�ӦΪ 2Ag+Cl2�T2AgCl��
��1��д���õ�ع���ʱ��������Ӧ��������___��������___��
��2������·��ת��amole��ʱ������Ĥ�����Һ��Լ����___mol���ӣ�����Ĥ�Ҳ���Һc��HCl��___�������������������1molL-1��������Һ����仯����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com