
A、B、C、X是中学化学常见物质,均由短
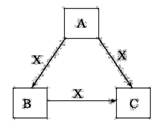 周期元素组成,转化关系如图。
周期元素组成,转化关系如图。
请针对以下三种不同情况回答:
(1)若A、B、C中均含同一种常见金属元素,该元素
在C中以阴离子形式存在,将A、C的水溶液混合可得B的白色胶状沉淀。
①A中含有的金属元素在元素周期表中的位置为__________,向水中加入X物质,X对水的电离平衡的影响是 (填“促进”、“抑制”或 “无影响”) 。
②A与C的水溶液混合后生成B反应的离子方程式为 。
(2)若A为固态非金属单质,A与X同周期,同时A在X中燃烧,产生白色烟雾,常温常压下C为白色固体,B分子中各原子最外层均为8电子结构。
①若A为该元素的白色固体单质,则1mol A单质中含共价键数目为 NA ,B的电子式为___________。
②X与水反应的离子方程式为 。
(3)若A、B、C的焰色反应呈黄色,水溶液均为碱性,常温下,X为气态酸性氧化物。
①A中所含有的化学键类型是_____________________。
②C溶液中离子浓度由小到大的顺序是__ _________________ 。
科目:高中化学 来源: 题型:
NiSO4•6H2O是一种绿色易溶于水的晶体,广泛用于化学镀镍、生产电池等,可由电镀废渣(除含镍外,还含有Cu、Fe、Cr等杂质)为原料获得。工艺流程如下图:


已知:25℃时,几种金属氢氧化物的溶度积常数和完全沉淀的pH范围如下表所示。
| Fe(OH)2 | Fe(OH)3 | Cr(OH)3 | Ni(OH)2 | |
| Ksp | 8.0×10—16 | 4.0×10—38 | 6.0×10—31 | 6.5×10—18 |
| 完全沉淀pH | ≥9.6 | ≥3.2 | ≥5.6 | ≥8.4 |
注:NiCO3是一种不溶于水易溶于强酸的沉淀。
请回答下列问题:
(1)下列措施可行,且能提高废渣浸出率的有 。
A.升高反应温度 B.增大压强 C.在反应过程中不断搅拌
(2)在滤液Ⅰ中加入6%的H2O2,其作用是 (用离子方程式表示);加入NaOH调节pH的范围是 ,为了除去溶液中的 离子。
(3)滤液Ⅱ的主要成分是 。
(4)检验Ni2+已完全沉淀的实验方法是 。
(5)操作Ⅰ的实验步骤依次为:
① ;
② ;
③蒸发浓缩、冷却结晶,过滤得NiSO4•6H2O晶体;
④用少量乙醇洗涤NiSO4•6H2O晶体并晾干。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、M、N、Q为元素周期表前四周期的五种元素。其中X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,M的内层电子数是最外层电子数的9倍, Q在元素周期表的各元素中电负性最大。元素N的气态原子逐个失去第1个至第4个电子所需能量(即电离能,用符号I1至I4表示)如下表所示:
| I1 | I2 | I3 | I4 | |
| 电离能(kJ/mol) | 578 | 1817 | 2745 | 11578 |
请回答下列问题:
(1)X元素的基态原子中电子占据 种能量不同的原子轨道,属于 区元素,它的外围电子排布图为 。
(2)XZ3分子的立体结构是 ,XZ2分子中中心原子的杂化类型为 ,两者中属于极性分子的是 (写分子式),请简述XZ3和XZ2对应水化物的酸性强弱差异的原因
。
(3)元素N的化合价最可能是________;
(4)M与Q形成的化合物的沸点远高于Y与Q形成的化合物的原因是: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
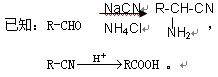
氯吡格雷(clopidogrel)是一种用于抑制血小板聚集的药物。以A(C7H5OCl)为原料合成氯吡格雷的路线如下:
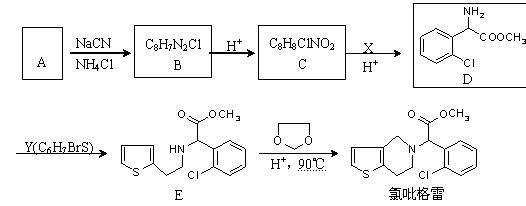
完成下列填空:
⑴C中含氧官能团的名称为 ,C→D的反应类型是 。
⑵Y的结构简式为 ,在一定条件下Y与BrCl(一氯化溴,与卤素单质性质相似)按物质的量1:1发生加成反应,生成的产物可能有 种。
⑶C可在一定条件下反应生成一种产物,该产物分子中含有3个六元环。该反应的化学
程式为 。
⑷由E转化为氯吡格雷时,生成的另一种产物的结构简式为 。
⑸写出A(芳香族化合物)的所有同分异构体的结构简式(包括A本身) 。
⑹
写出由乙烯、甲醇为有机原料制备化合物 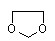 的合成路线流程图(无机试剂任选)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任选)。合成路线流程图示例如下:
CH3CH2OH 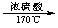 CH2=CH2
CH2=CH2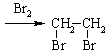
。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关热化学方程式的叙述正确的是
A.已知甲烷的燃烧热为890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为
CH4(g)+2O2(g) ====2CO2(g)+2H2O(g) ΔH = - 890.3 kJ·mol-1
B.已知C(石墨,s)====C(金刚石,s) ΔH >0, 则金刚石比石墨稳定
C.已知中和热为ΔH =-57.4 kJ·mol-1,则1mol稀硫酸和足量稀NaOH溶液反应的反应热就是中和热
D.已知S(g)+O2(g) ==== SO2(g) ΔH1; S(s)+O2(g) ==== SO2(g) ΔH2, 则ΔH1﹤ΔH2
查看答案和解析>>
科目:高中化学 来源: 题型:
反应4A(s)+3B(g) 2C(g)+D(g),经2 min,B的浓度减少0.6 mol·L-1。对此反应速率的表示正确的 是( )
A.在2 min内的反应速率,用C表示是0.3 mol·L-1·min-1
B.用A表示的反应速率是0.4 mol·L-1·min-1
C.在2 min末的反应速率,用B表示是0.3 mol·L-1·min-1
D.分别用B、C、D表示反应速率,其比值是3∶2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
新型净水剂—高铁酸钾(K2FeO4)为暗紫色固体,可溶于水。工业上制备K2FeO4的常用方法之一是次氯酸盐氧化法:①2FeCl3+10NaOH+3NaClO=2Na2FeO4+9NaCl+5H2O、②Na2FeO4+2KOH=K2FeO4+2NaOH。下列说法不正确的是
A.反应①为氧化还原反应,反应②为复分解反应
B.反应①中氧化产物与还原产物物质的量之比为2:9
C.反应②的产物K2FeO4中Fe为+6价,具有强氧化性,能杀菌消毒
D.若有2mol FeCl3发生反应,转移电子的物质的量为6 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com