


科目:高中化学 来源: 题型:
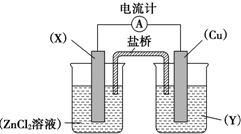 依据氧化还原反应Zn(s)+Cu2+(aq)═Zn2+(aq)+Cu(s)设计的原电池如图所示.
依据氧化还原反应Zn(s)+Cu2+(aq)═Zn2+(aq)+Cu(s)设计的原电池如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol/L |
| B、2mol/L |
| C、3mol/L |
| D、0.5mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,2g氢气所含有的氢原子的数目为NA |
| B、1molFe与足量的盐酸反应,失去的电子数为0.3NA |
| C、标准状况下,22.4L氯气与足量氢氧化钠溶液反应转移的电子数为NA |
| D、0.02 mol/L的NaCl溶液中含有Na+的数目是0.02 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、x=4 |
| B、每生成1 mol Fe3O4,反应共转移2 mol e- |
| C、Fe2+和S2O32-都是还原剂 |
| D、1 mol S2O32-被氧化时,被S2O32-还原的O2为0.25 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、爆鸣气、硫酸铜、硫酸 |
| B、水、空气、纯碱 |
| C、氧化铁、氨水、熟石灰 |
| D、硝酸、石灰石、烧碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
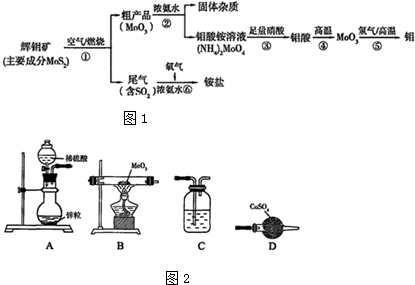
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
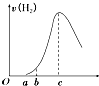 把在空气中久置的铝片5.0g投入盛有500mL 0.5mol?L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率v与反应时间t可用如图所示的坐标曲线来表示:
把在空气中久置的铝片5.0g投入盛有500mL 0.5mol?L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率v与反应时间t可用如图所示的坐标曲线来表示:| A、O→a段不产生氢气是因为表面的氧化物隔离了铝和硫酸溶液 |
| B、b→c段产生氢气的速率增加较快的主要原因之一是温度升高 |
| C、c点时反应处平衡状态 |
| D、t>c产生氢气的速率降低主要是因为溶液中c(H+)降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com