
 X+CH2═CH-R
X+CH2═CH-R| Pd |
| 碱 |
 CH═CH-R+HX (X为卤素原子,R为取代基)经由Heck反应合成M(一种防晒剂)的路线如下:
CH═CH-R+HX (X为卤素原子,R为取代基)经由Heck反应合成M(一种防晒剂)的路线如下:
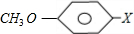 ,D为CH2═CHCOOCH2CH2CH(CH3)2.A(C3H4O)发生氧化生成B,B与C反应生成D,可知A为CH2═CH-CHO,B为CH2═CH-COOH,故C为HOCH2CH2CH(CH3)2.与浓H2SO4共热生成F,F能使酸性KMnO4溶液褪色,故C发生消去反应生成F,所以F为(CH3)2CHCH=CH2.D含有碳碳双键,发生加聚反应生成高分子化合物G,所以G的结构简式为
,D为CH2═CHCOOCH2CH2CH(CH3)2.A(C3H4O)发生氧化生成B,B与C反应生成D,可知A为CH2═CH-CHO,B为CH2═CH-COOH,故C为HOCH2CH2CH(CH3)2.与浓H2SO4共热生成F,F能使酸性KMnO4溶液褪色,故C发生消去反应生成F,所以F为(CH3)2CHCH=CH2.D含有碳碳双键,发生加聚反应生成高分子化合物G,所以G的结构简式为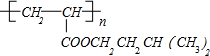 .E的一种同分异构体K苯环上有两个取代基且苯环上只有两种不同化学环境的氢,说明两个取代基处于苯环的对位位置,K与FeCl3溶液作用显紫色,则K中含有酚羟基.故K为
.E的一种同分异构体K苯环上有两个取代基且苯环上只有两种不同化学环境的氢,说明两个取代基处于苯环的对位位置,K与FeCl3溶液作用显紫色,则K中含有酚羟基.故K为 .
. ,D为CH2═CHCOOCH2CH2CH(CH3)2.A(C3H4O)发生氧化生成B,B与C反应生成D,可知A为CH2═CH-CHO,B为CH2═CH-COOH,故C为HOCH2CH2CH(CH3)2.与浓H2SO4共热生成F,F能使酸性KMnO4溶液褪色,故C发生消去反应生成F,所以F为(CH3)2CHCH=CH2.D含有碳碳双键,发生加聚反应生成高分子化合物G,所以G的结构简式为
,D为CH2═CHCOOCH2CH2CH(CH3)2.A(C3H4O)发生氧化生成B,B与C反应生成D,可知A为CH2═CH-CHO,B为CH2═CH-COOH,故C为HOCH2CH2CH(CH3)2.与浓H2SO4共热生成F,F能使酸性KMnO4溶液褪色,故C发生消去反应生成F,所以F为(CH3)2CHCH=CH2.D含有碳碳双键,发生加聚反应生成高分子化合物G,所以G的结构简式为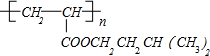 .E的一种同分异构体K苯环上有两个取代基且苯环上只有两种不同化学环境的氢,说明两个取代基处于苯环的对位位置,K与FeCl3溶液作用显紫色,则K中含有酚羟基.故K为
.E的一种同分异构体K苯环上有两个取代基且苯环上只有两种不同化学环境的氢,说明两个取代基处于苯环的对位位置,K与FeCl3溶液作用显紫色,则K中含有酚羟基.故K为 ,
,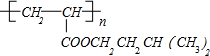 ,故答案为:(CH3)2CHCH=CH2;
,故答案为:(CH3)2CHCH=CH2;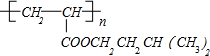 ;
; ,K与过量NaOH溶液共热,酚羟基与碱发生中和反应,-X原子在氢氧化钠水溶液、加热条件发生取代反应,发生反应的方程式为
,K与过量NaOH溶液共热,酚羟基与碱发生中和反应,-X原子在氢氧化钠水溶液、加热条件发生取代反应,发生反应的方程式为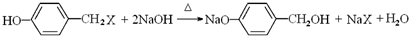 ,
,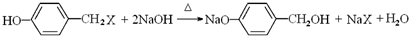 .
.


 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2个 | B、3个 | C、4个 | D、5个 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、υ(A)=0.2mol(L?s) |
| B、υ(B)=0.45 mol(L?s) |
| C、υ(C)=0.40 mol(L?min) |
| D、υ(D)=0.6 mol(L?min) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、与钠反应放出氢气 |
| B、与新制的Cu(OH)2悬浊液反应 |
| C、能与溴水发生取代反应 |
| D、发生相互加聚反应生成高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

| A、检验制得的香草醛中是否混有化合物3,可用氯化铁溶液 |
| B、化合物2在一定条件下可发生加聚反应 |
| C、理论上反应1→2中原子利用率100% |
| D、等物质的量的四种物质与足量NaOH溶液反应,消耗NaOH物质的量比为1:3:2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
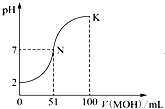 常温下向100mL 0.01mol?L-1 HA溶液中逐滴加入0.02mol?L-1 MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).回答下列问题:
常温下向100mL 0.01mol?L-1 HA溶液中逐滴加入0.02mol?L-1 MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com