
【题目】如图是可逆反应X2+3Y22Z2 在反应过程中的反应速率V与时间(t)的关系曲线,下列叙述正确的是( ) 
A.t1时,只有正方向反应
B.t2时,反应到达限度
C.t2﹣t3 , 反应不再发生
D.t2﹣t3 , 各物质的浓度不再发生变化
【答案】BD
【解析】解:A、t1时,既有正方向反应,又有逆反应,故A错误;
B、t2时,达平衡状态,反应到达限度,故B正确;
C、是动态平衡,v正═v逆>0,故C错误;
D、t2﹣t3 , 达平衡状态,各物质的浓度不再发生变化,故D正确;
故选BD.
【考点精析】根据题目的已知条件,利用化学平衡状态本质及特征的相关知识可以得到问题的答案,需要掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效).


 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源: 题型:
【题目】根据所学知识完成题目:
(1)西班牙的瑞奥汀托河是一条酸河,河水中含有硫酸亚铁和硫酸.经调查发现,这是由于上游河床含有黄铁矿(FeS2 , 铁为+2价),在水中氧的作用下,发生了反应:2FeS2+7O2+2H2O═2FeSO4+2H2SO4 . 反应中FeS2是剂,氧化产物是 , 当有1mol FeS2完全反应时,转移的电子数mol.
(2)某同学打算用稀硫酸与金属锌反应制备标准状况下的氢气224ml,为防止硫酸过量而造成浪费,实验中应需要硫酸mol.
(3)实验室现有一瓶稀硫酸如图A所示,B为空瓶,若利用A瓶中的稀硫酸配制B瓶上标签所示稀硫酸240ml,需要准备的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管和 , 所需A瓶中稀硫酸的体积 . 在配制溶液时若实验遇到下列情况,会造成所配硫酸溶液的物质的量浓度偏低的操作是(填序号) . 
①稀释的硫酸转移到容量瓶中后未洗涤烧杯
②趁热将溶液注入容量瓶中并定容
③摇匀后发现液面低于刻度线于是又加水
④容量瓶中原有少量蒸馏水.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设计如下装置探究稀盐酸中阴、阳离子在电场中的相对迁移速率(已知:Cd的金属活动性大于Cu)。恒温下,在垂直的玻璃细管内,先放CdCl2溶液及显色剂,然后小心放入HCl溶液,在aa'处形成清晰的界面。通电后,可观察到清晰界面缓缓向上移动。下列说法不正确的是( ) 
A.通电后,可观察到清晰界面缓缓向上移动的原因是Cd2+向Pt电极迁移的结果
B.装置中Pt电极附近的pH增大
C.一定时间内,如果通过HCl溶液某一界面的总电量为5.0 C,测得H+所迁移的电量为4.1 C,说明该HCl溶液中H+的迁移速率约是Cl-的4.6倍
D.如果电源正负极反接,则下端产生大量Cl2 , 使界面不再清晰,实验失败
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏伽德罗常数的值,下列说法正确的是( )
A.25℃时,pH=13的1.0L Ba(OH)2溶液中含有的Ba2+数目为0.05NA
B.标准状况下,2.24L CH2Cl2只含有的C﹣Cl键的数目为0.2NA
C.1.8g重水(D2O)只含有NA个中子
D.常温常压下,21g乙烯与环丁烷的混合物中含有原子数目为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种可再生能源,具有开发和应用的广阔前景,请回答下列问题:
一定温度下,在一恒容的密闭容器中,由CO和H2合成甲醇:CO(g)+2H2(g)CH3OH(g)△H<0
(1)下列情形不能说明该反应已达到平衡状态的是(填序号).
A.每消耗1mol CO的同时生成2molH2
B.混合气体总物质的量不变
C.生成CH3OH的速率与消耗CO的速率相等
D.CH3OH,CO,H2的浓度都不再发生变化
(2)CO的平衡转化率(α)与温度、压强的关系如图所示.B、C二点的平衡常数KB、KC的大小关系为 . 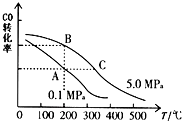
(3)某温度下,将2.0mol CO和6.0molH2充入2L的密闭容器中,达到平衡时测得c(CO)=0.25mol/L,CO的转化率= , 此温度下的平衡常数K=(保留二位有效数字).
(4)温度650℃的熔融盐燃料电池,用(CO、H2)作反应物,空气与CO2的混合气体为正极反应物,镍作电极,用Li2CO3和Na2CO3混合物作电解质.该电池的正极反应式为 .
(5)已知:CH3OH、H2的燃烧热(△H)分别为﹣726.5kJ/mol、﹣285.8kJ/mol,则常温下CO2和H2反应生成CH3OH和H2O的热化学方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意解答
(1)某实验小组设计了下列实验以探究影响化学反应速率的因素. 实验I:在甲、乙、丙三只相同的试管中分别加入5mL质量分数均为5%的过氧化氢溶液,各加入三滴洗涤剂,再分别放到如图所示的烧杯中水浴加热.实验发现,三支试管中产生气泡的速率不同.(洗涤剂起到将气体变为气泡的作用)
实验Ⅱ:在甲、乙、丙三只相同的试管中分别加入5mL质量分数均为5%的过氧化氢溶液,各加入三滴洗涤剂.在甲试管中加入MnO2少许,在乙试管中加入少许FeCl3 , 在丙中加入少许新鲜的鸡肝泥.观察到乙试管中产生气泡的速率最慢,而丙试管中产生气泡的速率最快.
实验Ⅲ:在甲、乙、丙三只相同的试管中分别加入5mL质量分数分别为5%,10%和15%的过氧化氢溶液,各加入三滴洗涤剂,再分别滴加三滴浓FeCl3溶液.观察并记录实验现象.
实验Ⅳ:在甲、乙、丙三只相同的试管中分别加入少许鸡肝泥,再分别放到如图所示的烧杯中水浴加热2分钟,再分别向三支试管中加入5mL质量分数均为5%的过氧化氢溶液和三滴洗涤剂.观察到丙中产生气泡速率最慢.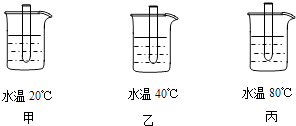
根据上述四个实验,回答下列问题:
①实验I的实验现象是 .
②实验Ⅱ的实验目的是 .
③实验Ⅲ的实验目的是;产生气泡速率最快的是试管(填“甲”“乙”或“丙”).
④实验Ⅳ中丙产生气泡速率最慢,该实验现象的原因可能是 .
(2)在一定温度下,将0.20 mol 的四氧化二氮气体充入1L的固定的密闭容器,每隔一段时间对该容器内的物质进行一次分析,得到如下数据:
时间 (s) | 0 | 20 | 40 | 60 | 80 | 100 |
C(N2O4) | 0.20 | C1 | 0.10 | C3 | C4 | C5 |
C(NO2) | 0.00 | 0.12 | C2 | 0.22 | 0.22 | 0.22 |
根据表格提供数据,请回答下列各小题:
①C1C2(填<,>或=).
②在0~20S内四氧化二氮的平均反应速度为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取三个干燥的烧瓶,分别装入标准状况下的干燥氨气、含有二分之一体积空气的氯化氢、二氧化氮和氧气(体积比为4:1)的混合气体;然后分别做溶解于水的喷泉实验.实验结束后三个烧瓶中所得溶液的物质的量浓度之比为( )
A.2:1:2
B.5:5:4
C.1:1:1
D.无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com