
【题目】25℃时,pH简单计算。
(1)0.05mol/L的硫酸溶液的pH=________________;0,01mol/L的NaOH溶液的pH=________________。
(2)1mlpH=2的硫酸加水稀释至100ml,pH=___________。
(3)常温下,由水电离出的C(H+)=1×10-12mol/L,则,该溶液的可能pH=___________。
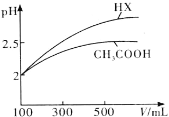
(4)体积均为100mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数________(填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数。
(5)常温下,常温下,pH=12的NaOH溶液与pH=1的HCl溶液按一定比例混合,所得溶液pH=2,则NaOH溶液与HCl溶液的体积比为_________________。
【答案】112412或2大于9:2
【解析】
(1)根据1个硫酸分子中有2个氢原子,可求出C(H+);根据Kw求出C(H+);
(2)1mL pH=2的H2SO4溶液加水稀释到100mL,c(H+)由0.01mol·L-1变为0.0001mol·L-1;
(3)常温下,由水电离出的C(H+)=1×10-12mol/L,如果是酸C(H+)=0.01mol/L,如果是碱C(OH-)=0.01mol/L;
(4)pH相等的酸中,加水稀释促进弱酸电离,稀释相同的倍数,pH变化大的为强酸,小的为弱酸。
(5)依据酸碱反应实质为H++OH-=H2O,常温下溶液中c(H+)c(OH-)=10-14,混合后溶液显酸性,说明氢离子过量,结合定量关系计算混合溶液中过量的氢离子浓度为10-2mol·L-1,得到酸碱溶液的体积比。
(1)0.05mol·L-1硫酸溶液中,C(H+)═2c(SO42-)=0.1mol·L-1,则pH=-lgC(H+)═1;
0.01mol·L-1,氢氧化钠为强碱,则溶液中氢氧根离子浓度c(OH-)=10-2mol·L-1,常温下Kw=10-14,依据Kw=c(H+)c(OH-),C(H+)=10-14/10-2=10-12mol·L-1,则溶液pH=-lg10-12=12;
(2)1mL pH=2的H2SO4溶液加水稀释到100mL,溶液中氢离子浓度c(H+)由0.01mol·L-1变为0.0001mol·L-1,则稀释后溶液的pH=-lg0.0001=4;
(3)如果是酸:c(H+)==0.01mol·L-1,溶液的pH=-lg0.01=2;
如果是碱c(OH-)=0.01mol·L-1,c(H+)=1×10-14/C(OH-)mol·L-1=1×10-14/0.01mol·L-1=1×10-12mol·L-1,该氢氧化钠溶液的pH=-lg1×10-12=12;
(4)pH相等的酸中,加水稀释促进弱酸电离,稀释相同的倍数,pH变化大的为强酸,小的为弱酸,所以HX的酸性大于醋酸,则HX的电离平衡常数大于醋酸;
(5)pH=12的NaOH溶液中c(OH-)=10-2mol·L-1,pH=1的HCl溶液c(H+)=0.1mol·L-1;设氢氧化钠溶液体积为V(碱),酸溶液体积为V(酸),依据溶液混合后pH=2,氢离子过量,混合溶液中氢离子浓度计算为:c(H+)=(0.1V(酸)-0.01V(碱))/(V(酸)+V(碱))=0.01,解得V(碱):V(酸)=9:2。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.通常,同周期元素的第一电离能ⅦA族的元素最大
B.主族元素的原子形成单原子离子时的化合价数都和它的族序数相等
C.第ⅠA、ⅡA族元素的原子,其半径越大,第一电离能越大
D.在同一主族中,自上而下第一电离能逐渐减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合理利用资源,降低碳的排放,实施低碳经济是今后经济生活主流。
(1)科学家致力于二氧化碳的“组合转化”技术研究,如将H2和CO2以4∶1比例混合通入反应器,适当条件下反应可获得一种能源。完成以下化学方程式:4H2+CO2 ![]() ________ +2H2O。
________ +2H2O。
(2)汽车尾气中的CO、NOx在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出NO被CO还原的化学方程式:_______________。
(3)工业尾气中氮的氧化物常采用碱液吸收法处理。NO与NO2按物质的量之比1∶1被足量KOH溶液完全吸收后只得到一种钾盐,该钾盐的化学式是______________。
(4)CO2合成生产燃料甲醇(CH3OH)是碳减排的新方向。进行如下实验:某温度下在1 L的密闭容器中,充2 mol CO2和6 mol H2,发生:CO2(g)+3H2(g )![]() CH3OH(g)+H2O(g)。
CH3OH(g)+H2O(g)。
①能判断该反应已达化学反应限度标志的是______________ (填字母)。
a.CO2百分含量保持不变
b.容器中H2浓度与CO2浓度之比为3:1
c.混合气体的平均相对分子质量保持不变
d.容器中混合气体的质量保持不变
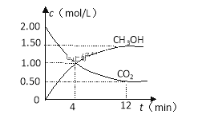
②现测得CO2和CH3OH(g)的浓度随时间变化如图所示。从反应开始到平衡,氢气的平均反应速率v (H2)=______ mol/(L min),容器中起始的压强与平衡时的压强之比为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烃A的产量能衡量一个国家石油化工发展水平,F的碳原子数为D的两倍,以A为原料合成F,其合成路线如图所示:
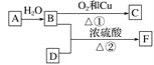
(1)写出决定B、D性质的重要原子团的名称:
B________、D________。
(2)A的结构式为____________。
(3)写出下列反应的化学方程式并注明反应类型:
①______________________,反应类型:_______;
②_________________,反应类型:________。
(4)实验室怎样区分B和D?___________。
(5)除去F中少量B和D的最好试剂是________(填字母)。
A 饱和碳酸钠溶液 B 氢氧化钠溶液 C 苯 D 水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有短周期元素R、X、Y、Z、T。R与T原子最外层电子数均是电子层数的2倍;Y元素能与大多数金属和非金属元素形成化合物;Z+与Y2-电子层结构相同。五种元素的原子半径与原子序数的关系如图所示,下列推断正确的是

A. Y、Z组成的化合物只含离子键
B. 氢化物的沸点:Y < X
C. T、R的最高价氧化物对应的水化物的酸性T比R的强
D. Y分别与T、X组成的二元化合物的水溶液一定是强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】滴定是一种重要的定量实验方法:
Ⅰ.酸碱中和滴定:常温下,用0.1000mol/L NaOH溶液分别滴定20.00mL 等浓度的盐酸和醋酸溶液,得到两条滴定曲线,如下图所示:
(1)滴定盐酸的曲线是图__________(填“1”或“2”)
(2)滴定前CH3COOH的电离度为__________
(3)达到B、D状态时,反应消耗的NaOH溶液的体积a__________b(填“>”“<”或“=”)
Ⅱ.氧化还原滴定原理与中和滴定原理相似,为了测定某NaHSO3固体的纯度,现用0.1000mol/L的酸性KMnO4溶液进行滴定,回答下列问题:
(1)准确量取一定体积的酸性KMnO4溶液需要使用的仪器是___________________。
(2)已知酸性KMnO4溶液的还原产物为MnSO4,写出此反应的离子方程式:_____
(3)若准确称取WgNaHSO3固体溶于水配成500mL溶液,取25.00mL置于锥形瓶中,用KMnO4溶液滴定至终点,消耗KMnO4溶液VmL。则滴定终点的现象为_______NaHSO3固体的纯度为_________。
(4)下列操作会导致测定结果偏低的是__________.
A 未用标准浓度的酸性KMnO4溶液润洗滴定管
B 滴定前锥形瓶未干燥
C 盛装酸性KMnO4溶液的滴定管,滴定前滴定管尖嘴部分有气泡, 滴定后无气泡
D 不小心将少量酸性KMnO4溶液滴在锥形瓶外
E 观察读数时,滴定前仰视,滴定后俯视
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【题目】已知:①H2(g)+ ![]() O2(g)=2H2O(g) △H1=akJ/mol
O2(g)=2H2O(g) △H1=akJ/mol
②2H2(g)+O2(g)=2H2O(g) △H2=b kJ/mol
③H2(g)+ ![]() O2(g)=H2O(l) △H3=ckJ/mol;
O2(g)=H2O(l) △H3=ckJ/mol;
④2H2(g)+O2(g)=2H2O(l) △H4=dkJ/mol。
下列关系正确的是
A. a<c<0 B. b>d>0 C. 2a=b<0 D. 2c=d>0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com