
【题目】下列叙述正确的是( )
A.通常,同周期元素的第一电离能ⅦA族的元素最大
B.主族元素的原子形成单原子离子时的化合价数都和它的族序数相等
C.第ⅠA、ⅡA族元素的原子,其半径越大,第一电离能越大
D.在同一主族中,自上而下第一电离能逐渐减小
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】工业上消除氮氧化物的污染,可用如下反应:
CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g) ΔH=a kJ/mol
N2(g)+CO2(g)+2H2O(g) ΔH=a kJ/mol
在温度T1和T2时,分别将0.50 mol CH4和1.2 mol NO2充入体积为1 L的密闭容器中,测得n(CH4)随时间变化数据如下表:
温度 | 时间/min n/mol | 0 | 10 | 20 | 40 | 50 |
T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | n(CH4) | 0.50 | 0.30 | 0.18 | …… | 0.15 |
下列说法不正确的是
A. 10 min内,T1时v(CH4)T2时小 B. 温度:T1<T2
C. ΔH:a < 0 D. 平衡常数:K(T1)<K(T2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验能达到预期目的的是
A.  制溴苯
制溴苯
B.  从 a 处移到 b 处,观察到铜丝由黑变红
从 a 处移到 b 处,观察到铜丝由黑变红
C.  检验无水乙醇中是否有水
检验无水乙醇中是否有水
D.  分离含碘的四氯化碳液体,最终在锥形瓶中可获得碘
分离含碘的四氯化碳液体,最终在锥形瓶中可获得碘
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(12分)二氧化碳是用途非常广泛的化工基础原料,回答下列问题:
(1)工业上可以用CO2来生产燃料甲醇。
已知:CO2(g)+3H2(g)![]() CH3OH(l)+H2O(l) △H=-130kJ·mol-1
CH3OH(l)+H2O(l) △H=-130kJ·mol-1
2H2(g)+O2(g)=2H2O(l) △H=-572kJ·mol-1
CH3OH(l)的燃烧热△H=___________。
(2)在催化剂作用下,CO2和CH4可直接转化为乙酸:CO2(g)+CH4(g)=CH3COOH(g) △H>0在不同温度下乙酸的生成速率变化如图所示。
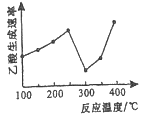
①当温度在250℃—300℃范围时,乙酸的生成速率减慢的主要原因是_________。
②欲使乙酸的平衡产率提高,应采取的措施是_____________(任写一条措施即可)。
(3)一定条件下,在密闭容器中发生反应:2CO(g)![]() C(s)+CO2(g)。
C(s)+CO2(g)。
①下列能说明该反应达到平衡的是___________。
A.容器内混合物的质量不变
B.CO和CO2的物质的量之比不再变化
C.混合气体的平均摩尔质量不再变化
D.形成amolC=O键的同时断裂amolC![]() O键
O键
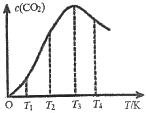
②向某恒容容器中通入一定量的CO发生上述反应,在不同温度下CO2的物质的量浓度c(CO2)随温度的变化如上图所示,则该反应为________(填“放热”或“吸热”)反应。
③向容积可变的某恒压容器中通入amolCO,TC时反应经过10min达平衡,CO的体积分数为75%。CO的平衡转化率为_______。在容积改变的条件下,反应速率可用单位时间内反应物或生成物的物质的量变化来表示,则0-10min内平均反应速率v(CO2)=__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】部分弱酸的电离常数如下表:

下列有关说法正确的是( )
A. 恰好中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者大于后者
B. 等体积、等浓度的HCOONa和NaCN两溶液中所含离子总数目HCOONa大于NaCN
C. NaHS溶液中加入适量 KOH后:c(Na+)=c(H2S)+c(HS-)+2c(S2-)
D. HCOO-、CN-、HS-在溶液中不可以大量共存
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在无色透明的溶液中,下列各组离子能大量共存的是( )
A. K+、H+、SO42- 、C1- B. Na+、CO32-、NO3-、Ca2+
C. Na+、NH4+、OH-、Cl- D. Na+、SO42-、Cu2+、C1-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】奈必洛尔是已知用于血管扩张的降血压药物。合成中间体I是合成奈必洛尔的重要步骤,以下是合成中间体I的已知工业流程:
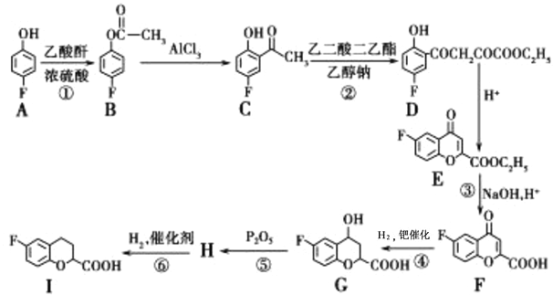
已知:乙酸酐的结构简式![]()
请回答下列问题:
(1)I物质中的含氧官能团的名称是____________________________。
(2)反应①的化学方程式为__________________;反应⑤的化学方程式为______________(填序号)
(3)上述①⑥中属于取代反应的是____________________________。(填序号)
(4)写出满足下列条件的C的同分异构体的结构简式:____________________________。
Ⅰ.苯环上只有两种取代基
Ⅱ.分子中核磁共振氢谱有4组峰
Ⅲ.能与NaHCO3反应生成CO2
(5)根据已有知识并结合相关信息,写出以![]() 和乙酸酐为原料制备
和乙酸酐为原料制备 的合成路线流程图(无机试剂任选)__________。合成路线流程图示例如下:
的合成路线流程图(无机试剂任选)__________。合成路线流程图示例如下:
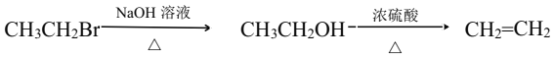
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右下表为元素周期表的一部分,其中X、Y、Z、W为短周期元素,W元素的核电荷数为X元素的2倍。下列说法正确的是( )
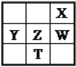
A. X、W、Z元素的原子半径及它们的气态氢化物的热稳定性均依次递增
B. Y、Z、W元素在自然界中均不能以游离态存在,它们的最高价氧化物的水化物的酸性依次递增
C. YX2晶体熔化、液态WX3气化均需克服分子间作用力
D. 根据元素周期律,可以推测T元素的单质具有半导体特性,T2X3具有氧化性和还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,pH简单计算。
(1)0.05mol/L的硫酸溶液的pH=________________;0,01mol/L的NaOH溶液的pH=________________。
(2)1mlpH=2的硫酸加水稀释至100ml,pH=___________。
(3)常温下,由水电离出的C(H+)=1×10-12mol/L,则,该溶液的可能pH=___________。
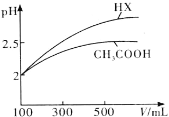
(4)体积均为100mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数________(填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数。
(5)常温下,常温下,pH=12的NaOH溶液与pH=1的HCl溶液按一定比例混合,所得溶液pH=2,则NaOH溶液与HCl溶液的体积比为_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com