
【题目】有机物A、B、C、D、E之间发生如下的转化:
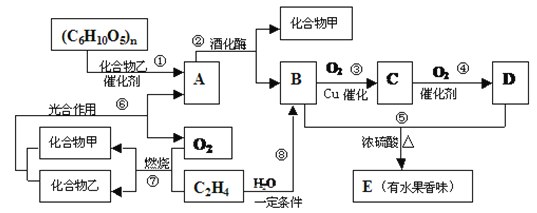
(1)写出C物质的结构简式:__________.
(2)上述②~⑧转化反应中,属于加成反应的有__________.(用反应序号填写);
(3)向A的水溶液中加入新制的Cu(OH)2并加热时产生的实验现象是__________.
(4)请写出反应的化学反应方程式:__________。
【答案】 CH3CHO ⑧ 有(砖)红色沉淀产生 2CH3CH2OH + O2 ![]() 2CH3CHO + 2H2O
2CH3CHO + 2H2O
【解析】试题分析:乙烯燃烧生成二氧化碳和水,化合物甲是二氧化碳、化合物乙水;二氧化碳、水通过光合作用生成葡萄糖和氧气,化合物A是葡萄糖;葡萄糖在酒化酶作用下生成乙醇和二氧化碳,B是乙醇;乙醇催化氧化生成乙醛C,乙醛可氧化为乙酸D;乙醇、乙酸发生酯化反应生成E,E是乙酸乙酯;乙烯与水在一定条件下发生加成反应生成乙醇。
解析:根据以上分析,(1)C是乙醛,乙醛结构简式:CH3CHO。
(2)乙烯与水在一定条件下生成乙醇属于加成反应,属于加成反应的是⑧;
(3)葡萄糖中含有醛基,与新制的Cu(OH)2加热产生葡萄糖酸和砖红色氧化亚铜沉淀,实验现象是有(砖)红色沉淀产生.
(4)乙醇催化氧化生成乙醛的方程式是2CH3CH2OH + O2 ![]() 2CH3CHO + 2H2O。
2CH3CHO + 2H2O。


科目:高中化学 来源: 题型:
【题目】燃煤技术的改进,有助于合理控制温室效应、环境污染,并能进行资源化利用,还可重新获得燃料或重要工业产品。工业上以煤和水为原料通过一系列转化变为清洁能源氢气和工业原料甲醇。
(1)若碳的燃烧热为393.5kJ·mol-1,氢气的燃烧热为285.8kJ·mol-1。已知反应
C(s)+2H2O(g) ![]() CO2(g)+2H2(g) △H>0,能否求出该反应的△H_______(填“能”或“不能”)。若能则求出其△H(若不能请说明理由):_____________________。
CO2(g)+2H2(g) △H>0,能否求出该反应的△H_______(填“能”或“不能”)。若能则求出其△H(若不能请说明理由):_____________________。
(2)工业上也可以仅利用上述反应得到的CO2和H2进一步合成甲醇,反应方程式为:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H<0
CH3OH(g)+H2O(g) △H<0
①工业生产过程中CO2和H2的转化率________(填“前者大”、“后者大”、“一样大”或“无法判断”),为了提高甲醇的产率可以采取的措施是____________、____________(填两点)。
②在一恒温恒容密闭容器中充入1 mol CO2和3 mol H2进行上述反应。测得CO2和CH3OH(g)浓度随时间变化如图所示。
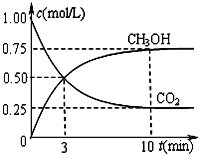
i.用H2表示0-3min内该反应的平均反应速率______________。
ii.该温度下的平衡常数为__________________。10 min后,保持温度不变,向该密闭容器中再充入1 mol CO2(g)和1 mol H2O(g),此时V正 _________V逆(填“>”、“<”或“=”)。
iii.对于基元反应aA+bB![]() cC+dD而言,其某一时刻的瞬时速率计算公式如下:正反应速率为V正=k正·c(A)a·c(B)b ;逆反应速率为V逆=k逆·c(C)c·c(D)d,其中k正、k逆为速率常数。若将上述反应视为基元反应则在上述条件下k逆∶k正=_________。反应进行到第3 min时V正 :V逆 =________。
cC+dD而言,其某一时刻的瞬时速率计算公式如下:正反应速率为V正=k正·c(A)a·c(B)b ;逆反应速率为V逆=k逆·c(C)c·c(D)d,其中k正、k逆为速率常数。若将上述反应视为基元反应则在上述条件下k逆∶k正=_________。反应进行到第3 min时V正 :V逆 =________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一化学平衡状态体系中,发生下列量的变化,其中一定会使平衡发生移动的是( )
A. 反应物的转化率 B. 反应物的浓度
C. 正、逆反应速率 D. 体系的压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将10mL单质气体X2和20mL单质气体Y2完全反应后,恰好生成20mL气体Z,若上述三种气体的体积都是在同温、同压下测定的,则气体Z的分子式是( )
A. XY2 B. X2Y C. XY D. X2Y4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知室温下0.01 mol·L-1 CH3COOH溶液中c(H+)=4.32×10-4 mol·L-1,则该CH3COOH溶液中水的离子积常数
A. <1×10-14B. >1×10-14
C. =1×10-14D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可用甲烷和氧气按9:1的体积比混合,在200℃和10MPa的条件下,通过铜制管道反应制得甲醇:2CH4+O2=2CH3COH。
(1)已知一定条件下,CH4和CH3COH燃烧的热化学方程式分别为:
CH4(g)+SO2(g)=CO2(g)+2H2(g) △H=-802kJ/lmol
CH3OH(g)+l.5O2(g)=CO2(g)+2H2O(g) △H=-677kJ/mol
则2CH4(g)+O2(g)=2CH3OH(g) △H=__________
(2)甲烷固体氧化物燃料电池属于第三代燃料电池,是一种在中高温下直接将储存在燃料和氧化剂中的化学能高效、环境友好地转化成电能的全固态化学发电装置。其工作原理如下图所示。a是电池的____极(填“正”或“负”) ,b极的电极反应式为__________。

(3)工业上合成甲醇的另一种方法为:
CO(g)+2H2(g) ![]() CH3OH(g) △H=-90kJ/mol
CH3OH(g) △H=-90kJ/mol
T℃时,将2mol CO 和4molH2充入1L 的密闭容器中,测得H2的物质的量随时间变化如下图实线所示。
① 能用于判断反应已达化学平衡状态的是____________。
A.气体的总压强不再改变
B. H2与CH3OH的体积比不再改变
C.气体的密度不再改变
D.单位时间内消耗1mol CO,同时生成1mol CH3OH
② 请计算出T℃ 时反应的平衡常数K=_________________。
③ 仅改变某一实验条件再进行两次实验测得H2的物质的量随时间变化如图中虚线所示。曲线Ⅰ对应的实验条件改变是:________;曲线Ⅱ对应的实验条件改变是_________0。

④ a、b、c三点逆反应速率由大到小排列的顺序是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuCl广泛应用于化工和印染等行业。某研究性学习小组拟热分解CuCl2·2H2O制备CuCl,并进行相关探究。
已知:

该小组用下图所示装置进行实验(夹持仪器略)。

请回答下列问题:
(1)仪器X的名称是__________。
(2)实验操作的先后顺序是① →_____→ → → ⑤。
①检查装置的气密性后加入药品 ②熄灭酒精灯,冷却
③在“气体入口”处通干燥HCl ④点燃酒精灯,加热
⑤停止通入HCl,然后通入N2
(3)在实验过程中,观察到B中物质由白色变为蓝色,C中试纸的颜色变化是_________。
(4)装置D中发生反应的离子方程式是___________________________________。
(5)反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl2或CuO杂质,根据资料信息分析:
①若杂质是CuCl2,则产生的原因是____________________________________________。
②若杂质是CuO,则产生的原因是________________________________________________。
(6)若m克CuCl2·2H2O全部转化为CuO(铜元素无损耗),则固体质量减少_____________克(用含m的式子表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2014新课标1】〔化学—选修5:有机化学基础〕(15分)
席夫碱类化合物G在催化、药物、新材料等方面有广泛应用。合成G的一种路线如下:
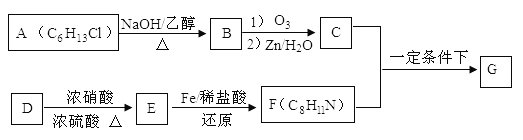
已知以下信息:
①
②一摩尔B经上述反应可生居二摩尔C,且C不能发生银镜反应。
③D属于单取代芳烃,其相对分子质量为106。
④核磁共振氢谱显示F苯环上有两种化学环境的
⑤
回答下列问题:
(1)由A生成B的化学方程式为 ,反应类型为
(2)D的化学名称是 ,由D生成E的化学方程式为:
(3)G的结构简式为
(4)F的同分异构体中含有苯环的还有____种(不考虑立体异构)。其中核磁共振氢谱中有4组峰,且面积比为6:2:2:1的是_______。(写出其中的一种的结构简式)。
(5)由苯和化合物C经如下步骤可合成N-异丙基苯胺。

反应条件1所选择的试剂为____________;反应条件2所选择的试剂为________;I的结构简式为_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com