
| A�� | ����������������Fe��OH��3+3H+�TFe3++3H2O | |
| B�� | AlƬ������NaOH��Һ��Ӧ���������壺2Al+2OH-+2H2O�T2Al��OH��3+3H2�� | |
| C�� | ��̼�������Һ�мӹ���ʯ��ˮ�����ȣ�NH4++OH-�TNH3•H2O | |
| D�� | ���ữ�ĸ��������Һ����˫��ˮ��2MnO4-+6H++5H2O�T2Mn2++5O2��+8H2O |
���� A�������������ܹ��������������ɵ��ʵ⣻
B�������Ϸ�Ӧ����ʵ��
C�����߷�Ӧ����̼��ơ�������ˮ��
D�����߷���������ԭ��Ӧ������������ӱ���ԭ���������ⱻ������
��� �⣺A�����������������������ӷ�ӦΪ2Fe��OH��3+2I-+6H+�T2Fe2++I2+6H2O����A����
B����������������Һ��Ӧ�����ӷ���ʽ��2Al+2OH-+2H2O=+2AlO2-+3H2������B����
C����̼�������Һ�мӹ���ʯ��ˮ�����ȵ����ӷ�ӦΪCa2++HCO3-+NH4++2OH-$\frac{\underline{\;\;��\;\;}}{\;}$NH3��+2H2O+CaCO3������C����
D�����ữ�ĸ��������Һ����˫��ˮ��2MnO4-+6H++5H2O�T2Mn2++5O2��+8H2O����D��ȷ��
��ѡ��D��
���� ���⿼�����ӷ�Ӧ����ʽ����д����ȷ�����Ļ�ѧ��Ӧ�ǽ����Ĺؼ���ע��������ԭ��ӦΪ�����״��㣬��Ŀ�ѶȲ���


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���³�ѹ�£�78gNa2O2�к��е�����������NA | |
| B�� | m g ${\;}_{Z}^{A}$Xn-��������������Z-n��mNA/A | |
| C�� | 1L0.1mol/LFe��OH��3�����к���Fe��OH��3������Ϊ0.1NA | |
| D�� | H2SO4��Ħ������Ϊ98 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ư�ۡ����ᡢ��ƺ�Һ�ȶ����ڻ���� | |
| B�� | ����е�1 mol/L NaOH��Һ�еμ�FeCl3������Һ�����Ʊ�Fe��OH��3���� | |
| C�� | �����Ȼ��ƣ������ͭ���ܵ��磬���Զ����ڵ���� | |
| D�� | һ��ƽ�й������䵰������Һʱ���Ӳ�����Կ���һ��������ͨ· |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaB��Һ��pH=8��c��Na+��-c��B-��=9.9��10-6mol•L-1 | |
| B�� | pH��ȵĢ�NH4C1���ڣ�NH4��2SO4����NH4HSO4������Һ�У�c��NH4+����С˳��Ϊ����=�ڣ��� | |
| C�� | Na2CO3��Һ�У�2c��Na+��=c��CO32-��+c��HCO3-��+c��H2CO3�� | |
| D�� | 10mLpH=12������������Һ�м���pH=2��HA��pH�պõ���7��������Һ���V���ܣ���20mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SO3 | B�� | BaSO4 | C�� | Cl2 | D�� | CH3COOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | X/m mol | B�� | 2X/3mol | C�� | ��X+Y��mol | D�� | 2��X+Y��/3mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
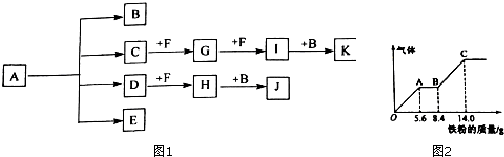
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SiC | B�� | SiO2 | C�� | Si | D�� | Si3N4 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com