
【题目】锌银电池的负极为锌,正极为氧化银,电解质是KOH,电池反应为Zn+Ag2O+H2O=Zn(OH)2+2Ag。以锌银电池为电源,电解硫酸镍溶液冶炼纯镍,装置如图所示。下列说法正确的是( )
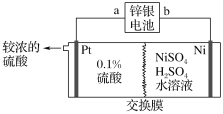
A.装置中使用阳离子交换膜
B.锌银电池a极反应式为Ag2O+H2O+2e-=2Ag+2OH-
C.左侧若加入稀盐酸,电解后得到比较浓的盐酸
D.若锌银电池溶解13 g锌,则镍极净增质量最多为5.9 g
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】X、Y、Z、Q、R是原子序数依次增大的短周期主族元素。已知:气体YX3能使润湿的紫色石蕊试纸变蓝,Z和X在同一主族,Q原子的最外层电子数是其周期序数的2倍。回答下列问题:
(1)![]() 原子的结构示意图为 _____,YX3的化学式为 _____。
原子的结构示意图为 _____,YX3的化学式为 _____。
(2)![]() 、Q、R原子的半径从大到小的顺序是 ___________。
、Q、R原子的半径从大到小的顺序是 ___________。![]() 用原子符号表示
用原子符号表示![]() 。
。
(3)![]() 分别与X、Z形成的化合物分别是__________(填化学式),___________(填电子式)。Q与Z形成的化合物类型是_________(填离子化合物或共价化合物)。
分别与X、Z形成的化合物分别是__________(填化学式),___________(填电子式)。Q与Z形成的化合物类型是_________(填离子化合物或共价化合物)。
(4)能证明R的非金属性比Q强的实验事实是______![]() 填字母序号
填字母序号![]() 。
。
A HR的水溶液酸性比H2Q的水溶液酸性强 B R2与H2化合比Q与H2化合容易。
C R的最高价氧化物的水化物的酸性比Q的强 D HR的稳定性比H2Q强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在四个不同的密闭容器中,采用不同条件进行反应N2(g)+3H2(g)![]() 2NH3(g),根据下列在相同时间内测定的结果判断,生成氨的速率最快的是
2NH3(g),根据下列在相同时间内测定的结果判断,生成氨的速率最快的是
A. v(N2)=0.2mol/(Lmin)B. v(NH3)=0.3mol/(Lmin)
C. v(H2)=0.1mol/(Lmin)D. v(H2)=0.3mol/(Lmin)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定质量的镁、铝合金与硝酸恰好完全反应,得到硝酸盐溶液和NO2、N2O4、NO的混合气体,将这些气体与标准状况下3.36 L O2混合后通入水中,所有气体恰好完全被水吸收生成硝酸。若向所得硝酸盐溶液中加入2 mol/L NaOH溶液至沉淀最多时停止加入,将沉淀滤出,向滤液中加水稀释至500 mL,此时所得溶液的物质的量浓度为( )
A. 0.5 mol/LB. 1 mol/L
C. 1.2 mol/LD. 2 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应![]()
![]() ,若在恒压绝热容器中发生,下列选项表明反应一定已达平衡状态的是( )
,若在恒压绝热容器中发生,下列选项表明反应一定已达平衡状态的是( )
A.容器内的温度不再变化
B.容器内的压强不再变化
C.相同时间内,断开![]() 键的数目和生成
键的数目和生成![]() 键的数目相等
键的数目相等
D.容器内气体的浓度![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物在工业生产等方面有重要的应用。工业合成氨是煤化工产业链中非常重要的一部分,发射卫星时可用肼(N2H4)作燃料。
(1)已知:17g NH3(g)在一定条件下分解生成N2(g)和H2(g),吸收46.1kJ的热量。则反应N2(g)+3H2(g)=2NH3(g) △H=_______________kJ·mol-1
(2)在一定条件下,向容积为5L的恒容密闭容器中充入1mol N2、3molH2,10min后,测得容器内NH3为1mol,则用N2表示的平均反应速率为______________________。
(3)已知在298K时1g肼气体燃烧生成N2和水蒸气,放出16.7kJ的热量。下列热化学方程式书写正确的是__________(填字母序号)
A.N2H4+O2=N2+2H2O △H=-534.4kJ·mol—1
B.N2H4(g)+O2(g)=N2(g)+2H2O(l) △H=-534.4kJ·mol—1
C.N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=-534.4kJ·mol—1
D.N2H4(g)+O2(g)= N2(g)+2H2O(g) △H=-16.7kJ·mol—1
(4)N2H4、O2和KOH溶液组成的燃料电池生成水和氮气。
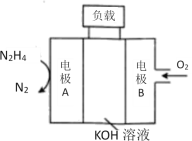
①负极反应式为_____________。
②放电时,溶液中的阴离子向_______极移动(填“正”或“负”)。
③放电时,正极区溶液的碱性___________(填“增强”、“减弱”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,反应H2(g)+ I2(g) 2HI(g) △H<0在一密闭体系中达到化学平衡。在448℃时,该反应的化学平衡常数为49。
(1)请写出该反应的平衡常数的表达式__________。
(2)下列说法中能说明该反应已达平衡状态的是______________(用字母序号填空)
A.压强不再改变
B.速率之比 v(H2):v(I2):v(HI)=1:1:2
C.混合气体的颜色不再改变
D.混合气体的密度不再改变
(3)只改变下列条件,该化学平衡如何移动?①向正反应方向移动;②向逆反应方向移动;③不移动。升高温度__________;(用数字序号填空,下同)缩小容器的体积___________;保持体积不变,通入氢气___________;保持压强不变,通入氩气____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC为离子化合物,D的二价阳离子与C的阴离子具有相同的电子层结构。化合物AC2为一种常见的温室气体。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)基态E原子的核外电子排布式是________,在第四周期中,与基态E原子最外层电子数相同还有_______(填元素符号)。
(2)A、B、C的第一电离能由小到大的顺序为____________。
(3)写出化合物AC2的电子式_____________。
(4)D的单质在AC2中点燃可生成A的单质与一种熔点较高的固体产物,写出其化学反应方程式:__________。
(5)1919年,Langmuir提出等电子原理:原子数相同、电子数相同的分子,互称为等电子体。等电子体的结构相似、物理性质相近。此后,等电子原理又有发展,例如,由短周期元素组成的微粒,只要其原子数相同,各原子最外层电子数之和相同,也可互称为等电子体。一种由B、C组成的化合物与AC2互为等电子体,其化学式为_____。
(6)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() (次磷酸钠)易溶于水,水溶液近中性,具有强还原性,可用于化学镀银、镍、铬等.一种利用泥磷(含
(次磷酸钠)易溶于水,水溶液近中性,具有强还原性,可用于化学镀银、镍、铬等.一种利用泥磷(含![]() 和少量
和少量![]() 、
、![]() 、
、![]() 、
、![]() 等)为原料制备
等)为原料制备![]() 的工艺流程如下:
的工艺流程如下:
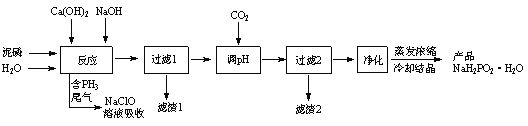
已知:①![]() 与两种碱的反应主要有:
与两种碱的反应主要有:
I.![]()
II.![]()
III.![]()
②2.实验温度下,![]()
![]()
(1)已知![]() 是一元中强酸,写出
是一元中强酸,写出![]() 溶液中存在的所有平衡方程式:_________。
溶液中存在的所有平衡方程式:_________。
(2)通![]() “调
“调![]() ”时,写出除去溶液中
”时,写出除去溶液中![]() 杂质的离子方程式是_________。
杂质的离子方程式是_________。
(3)“过滤2”的滤渣2主要成分为_________(填化学式),“净化”除去![]() 及
及![]() 等时还须用到
等时还须用到![]() 、
、![]() 及
及![]() 溶液,当加入一定量的
溶液,当加入一定量的![]() 溶液后,静置,溶液中
溶液后,静置,溶液中![]() ,则此时溶液中
,则此时溶液中![]() 的浓度为_________
的浓度为_________![]() 。
。
(4)尾气中的![]() 被
被![]() 溶液吸收生成
溶液吸收生成![]() ,则该吸收反应中氧化产物与还原产物的物质的量之比为_________。从吸收液中经结晶、过滤、洗涤、干燥,也可获得产品
,则该吸收反应中氧化产物与还原产物的物质的量之比为_________。从吸收液中经结晶、过滤、洗涤、干燥,也可获得产品![]() ,洗涤该产品常用乙醇,其原因是_________。
,洗涤该产品常用乙醇,其原因是_________。
(5)次磷酸钠的磷元素易被强氧化剂氧化成最高价。实验室可用滴定法测定产品纯度。
甲同学准确称取![]() 产品配成
产品配成![]() 溶液准确量取
溶液准确量取![]() 溶液于锥形瓶中,用
溶液于锥形瓶中,用![]() 酸性
酸性![]() 标准溶液经规范、严密的多次平行滴定,平均消耗酸性
标准溶液经规范、严密的多次平行滴定,平均消耗酸性![]() 溶液
溶液![]() ,则测得产品的纯度为_________,乙同学认为甲同学的测定结果不科学,分析导致甲同学得出如此测定结果的最可能原因是_________。
,则测得产品的纯度为_________,乙同学认为甲同学的测定结果不科学,分析导致甲同学得出如此测定结果的最可能原因是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com