
【题目】已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC为离子化合物,D的二价阳离子与C的阴离子具有相同的电子层结构。化合物AC2为一种常见的温室气体。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)基态E原子的核外电子排布式是________,在第四周期中,与基态E原子最外层电子数相同还有_______(填元素符号)。
(2)A、B、C的第一电离能由小到大的顺序为____________。
(3)写出化合物AC2的电子式_____________。
(4)D的单质在AC2中点燃可生成A的单质与一种熔点较高的固体产物,写出其化学反应方程式:__________。
(5)1919年,Langmuir提出等电子原理:原子数相同、电子数相同的分子,互称为等电子体。等电子体的结构相似、物理性质相近。此后,等电子原理又有发展,例如,由短周期元素组成的微粒,只要其原子数相同,各原子最外层电子数之和相同,也可互称为等电子体。一种由B、C组成的化合物与AC2互为等电子体,其化学式为_____。
(6)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是____________。
【答案】1s22s22p63s23p63d54s1(或[Ar] 3d54s1) K、Cu C<O<N ![]() 2Mg+ CO2
2Mg+ CO2 ![]() 2MgO +C N2O 4Mg+10HNO3 = 4Mg(NO3)2+NH4NO3+3H2O
2MgO +C N2O 4Mg+10HNO3 = 4Mg(NO3)2+NH4NO3+3H2O
【解析】
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC为离子化合物,D的二价阳离子与C的阴离子具有相同的电子层结构,化合物AC2为一种常见的温室气体,则A为C,C为O,B为N,D为Mg。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24,E为Cr。
(1)基态E原子的核外电子排布式是1s22s22p63s23p63d54s1(或[Ar] 3d54s1),在第四周期中,与基态E原子最外层电子数相同即最外层电子数只有一个,还有K、Cu;故答案为:1s22s22p63s23p63d54s1(或[Ar] 3d54s1);K、Cu;
(2)同周期从左到右电离能有增大趋势,但第IIA族元素电离能大于第IIIA族元素电离能,第VA族元素电离能大于第VIA族元素电离能,因此A、B、C的第一电离能由小到大的顺序为C<O<N;故答案为:C<O<N;
(3)化合物AC2为CO2,其电子式![]() ;故答案为:
;故答案为:![]() ;
;
(4)Mg的单质在CO2中点燃可生成碳和一种熔点较高的固体产物MgO,其化学反应方程式:2Mg+ CO2 ![]() 2MgO +C;故答案为:2Mg+ CO2
2MgO +C;故答案为:2Mg+ CO2 ![]() 2MgO +C;
2MgO +C;
(5)根据CO与N2互为等电子体,一种由N、O组成的化合物与CO2互为等电子体,其化学式为N2O;故答案为:N2O;
(6)B的最高价氧化物对应的水化物的稀溶液为HNO3与Mg的单质反应时,NHO3被还原到最低价即NH4NO3,其反应的化学方程式是4Mg+10HNO3 = 4Mg(NO3)2+NH4NO3+3H2O;故答案为:4Mg+10HNO3=4Mg(NO3)2+NH4NO3+3H2O。


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:
【题目】分离提纯时常用的仪器如图所示,请回答下列问题:
A.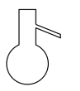 B.
B.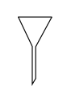 C.
C.![]() D.
D.![]() E.
E.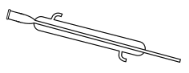
(1)仪器![]() 的名称分别为____、____。
的名称分别为____、____。
(2)分离以下混合物应主要选用上述哪种仪器(填字母符号)
a.除去澄清石灰水中悬浮的![]() 颗粒____;
颗粒____;
b.提取食盐水中的![]() 固体____;
固体____;
c.除去油水中的水:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌银电池的负极为锌,正极为氧化银,电解质是KOH,电池反应为Zn+Ag2O+H2O=Zn(OH)2+2Ag。以锌银电池为电源,电解硫酸镍溶液冶炼纯镍,装置如图所示。下列说法正确的是( )
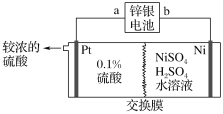
A.装置中使用阳离子交换膜
B.锌银电池a极反应式为Ag2O+H2O+2e-=2Ag+2OH-
C.左侧若加入稀盐酸,电解后得到比较浓的盐酸
D.若锌银电池溶解13 g锌,则镍极净增质量最多为5.9 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①2H2S(g)+SO2(g)═3S(s)+2H2O(l)△H1=﹣154 kJmol﹣1
②S(s)+O2(g)═SO2(g)△H2=﹣297 kJmol﹣1
③2H2S(g)+O2(g)═2S(s)+2H2O(l)△H3
④2H2S(g)+3O2(g)═2SO2(g)+2H2O(l)△H4
下列说法正确的是
A.△H3>△H4B.△H3=+143 kJmol﹣1
C.无法计算△H4的值D.H2S 燃烧热为 1045 kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以SO2为原料,通过下列工艺可制备化工原料H2SO4和清洁能源H2。下列说法中不正确的是
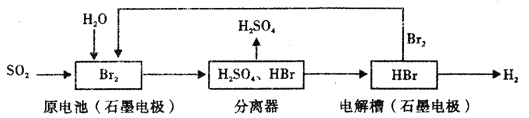
A. 该生产工艺中Br2被循环利用
B. 在电解过程中,电解槽阴极附近溶液的pH变大
C. 原电池中负极发生的反应为SO2+2H2O-2e-=SO42-+4H+
D. 该工艺总反应的化学方程式表示为SO2+Br2+2H20=2HBr+H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在体积为10 L的密闭容器中,1 mol A和1 mol B进行反应:2A(g)+B(g)![]() 2C(g),经60 s达到平衡,生成0.6 mol C。下列说法正确的是
2C(g),经60 s达到平衡,生成0.6 mol C。下列说法正确的是
A. 以A浓度变化表示的反应速率为0.001 mol·L-1·s-1
B. 其他条件不变,将容器体积变为5 L,C的平衡浓度变为原来的2倍
C. 其他条件不变,若增大压强,则物质A的转化率减小
D. 达到平衡时,C的体积百分含量为0.353
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素R、X、Y、Z在元素周期表中的相对位置如图所示,X原子最外层电子数比次外层电子数少3,下列说法正确的是
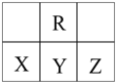
A.X的气态氢化物比R的气态氢化物稳定
B.原子半径大小顺序是:r(Z)> r( Y) > r( X)
C.Y、R形成的化合物YR2能使酸性KMnO4溶液褪色
D.X、Z形成的化合物XZ5中各原子均满足最外层8电子结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中的有害气体主要有NO、碳氢化合物及CO,某校同学设计实验将模拟汽车尾气转化为无害气体。回答下列问题;

(1)为了配制模拟尾气,甲组同学用上图所示装置分别制备NO、乙烯及CO三袋气体。
①用装置A制取NO,分液漏斗中盛放的是___(填试剂名称)。
②用 (乙烯利)与NaOH溶液并用装置B制取乙烯,反应生成乙烯的化学方程式为______(磷转化为Na3 PO4)。
(乙烯利)与NaOH溶液并用装置B制取乙烯,反应生成乙烯的化学方程式为______(磷转化为Na3 PO4)。
③用H2 C2 O4与浓硫酸制取CO(化学方程式为H2C2O4 ![]() CO+CO2+H2O并提纯,选用上图装置预制一袋干燥纯净的CO,各接口连接的顺序为___→g(气流从左至右),其中装置D中盛放的药品是___
CO+CO2+H2O并提纯,选用上图装置预制一袋干燥纯净的CO,各接口连接的顺序为___→g(气流从左至右),其中装置D中盛放的药品是___
(2)乙组同学将甲组制得的气体与空气按适当比例混合形成模拟尾气(NO,CO,C2 H4及空气),按如图所示 装置进行尾气转化并检验。

①为检验催化反应后的气体中是否有CO2生成和乙烯的残留,G、H中盛放的试剂依次是_________(填标号)。
a. NaOH溶液 b.酸性KMnO4溶液
c.澄清石灰水 d. Br2/CCl4溶液
②通“模拟尾气”前,需先将催化剂加热到反应所需的温度,其目的是___;写出其中CO与NO完全转化为无害气体的化学方程式:___
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)标准状况下,1.92 g某气体的体积为672 mL,则此气体的相对分子质量为_____。
(2)在25 ℃、101 kPa的条件下,同质量的CH4和A气体的体积之比是15∶8,则A的摩尔质量为________________。
(3)两个相同容积的密闭容器X、Y,在25 ℃下,X中充入a g A气体,Y中充入a g CH4气体,X与Y内的压强之比是4∶11,则A的摩尔质量为_____________。
(4)19 g某二价金属的氯化物RCl2中含有0.4 mol的Cl-,则R的相对原子质量为__________。
(5)V L Fe2(SO4)3溶液中含Fe3+ m g,则溶液中SO42-的物质的量浓度为___________mol·L-1。
(6)在无土栽培中,配制1 L含5 mol NH4Cl、1.6 mol KCl、2.4 mol K2SO4的某营养液,若用KCl、NH4Cl、(NH4)2SO4配制,则需KCl、NH4Cl的物质的量分别为________、________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com