
【题目】下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
族 周期 | IA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)④、⑤、⑥的原子半径由大到小的顺序为_____________________(填化学式)。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是___________。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:_______。
(4)由表中两种元素的原子按1:1组成的常见液态化合物的溶液易被催化分解,写出其化学方程式____。
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:

X溶液与Y溶液反应的离子方程式为_____________,N→⑥的单质的化学方程式为_____________。
【答案】Na>Al>O HNO3>H2CO3>H2SiO3 ![]() 或
或![]() 2H2O2====2H2O+O2↑ Al3++3NH3H2O═Al(OH)3↓+3NH4+ 2Al2O3(熔融)
2H2O2====2H2O+O2↑ Al3++3NH3H2O═Al(OH)3↓+3NH4+ 2Al2O3(熔融)![]() 4Al+3O2↑
4Al+3O2↑
【解析】
本题本题主要考查元素的性质。①②③④⑤⑥⑦⑧分别是H、C、N、O、Na、Al、Si、Cl。
(1)同周期元素的原子半径随着原子序数的增大而减小,所以原子半径Na>Al>Si。同主族元素原子半径随着电子层数增大而增大,所以原子半径O<Si。总之,④、⑤、⑥的原子半径由大到小的顺序为Na>Al>O。
(2)非金属性N>C>Si,所以最高价含氧酸的酸性由强到弱的顺序是HNO3>H2CO3>H2SiO3。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物氢氧化钠和次氯酸钠,其中一种化合物的电子式:![]() 。
。
(4)由表中两种元素的原子按1:1组成的常见液态化合物的溶液易被催化分解,其化学方程式为2H2O2![]() 2H2O+O2↑ 。
2H2O+O2↑ 。
(5)X溶液与Y溶液反应的离子方程式为![]() 。
。
N→⑥的单质的化学方程式为![]() 。
。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
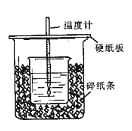
(1)从实验装置上看,图中尚缺少的一种玻璃仪器是 。
(2)烧杯间填满碎纸条的作用是 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大、偏小、无影响”)
(4)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等、不相等”),所求中和热 (填“相等、不相等”),简述理由
(5)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会 ;(填“偏大”、“偏小”、“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列信息判断氢气燃烧生成水时的热量变化,其中一定正确的是( )

A. H2O分解为H2与O2时放出热量
B. 生成1mol H2O时吸收热量245 kJ
C. 甲、乙、丙中物质所具有的总能量大小关系为乙>甲>丙
D. 氢气和氧气的总能量小于水的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一小块钠投入到盛有氯化镁溶液的试管里,不可能观察到的现象是 ( )
A.熔成小球并在液面上游动
B.有气体生成
C.溶液底部有银白色物质生成
D.溶液变浑浊
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一小块钠投入CuSO4溶液中,观察到的现象是__________(填序号)。
①钠浮于液面上;②熔化成小球;③发出嘶嘶的响声,放出气体;④有蓝色沉淀产生;⑤析出大量红色的铜。用离子方程式解释实验现象__________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人们应用原电池原理制作了多种电池以满足不同的需要。电池发挥着越来越重要的作用,如在宇宙飞船、人造卫星、电脑、照相机等,都离不开各式各样的电池,同时废弃的电池随便丢弃也会对环境造成污染。请根据题中提供的信息,回答下列问题:
(1)研究人员最近发明了一种“水”电池,这种电池能利用淡水与海水之间含盐量的差别进行发电,在海水中电池反应可表示为:5MnO2 +2Ag+2NaCl=Na2Mn5O10 +2AgCl。
①该电池的负极反应式是______________;
②在电池中,Na + 不断移动到“水”电池的_______极(填“正“或“负”);
③外电路每通过4mol电子时,生成Na2 Mn5 O10 的物质的量是_______。
(2)中国科学院应用化学研究所在甲烷(CH4是一种可燃物)燃料电池技术方面获得新突破。甲烷燃料电池的工作原理如下图所示:
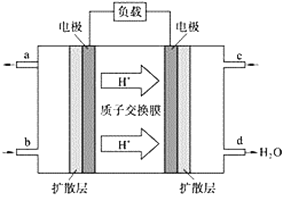
①该电池工作时,b口通入的物质为____________。
②该电池负极的电极反应式_________________________。
③工作一段时间后,当3.2 g甲烷完全反应生成CO2时,有__________NA个电子转移。
(3)Ag2O是银锌碱性电池的正极活性物质,当银锌碱性电池的电解质溶液为KOH溶液时,电池放电时正极的Ag2O转化为Ag,负极的Zn转化为Zn(OH)2,写出该电池反应方程式:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】部分氧化的 Fe-Cu 合金样品(氧化物为 Fe2O3、CuO)共5.76 g,经如下处理:

下列说法正确的是( )
A. 滤液A中的阳离子为Fe2+、Fe3+、H+ B. 溶解样品消耗的硫酸共为 0.04 mol
C. 样品中氧元素的质量为 0.48 g D. V=336 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将 4 mol A 气体和 2 mol B 气体在 2 L 的密闭容器中混合并在一定条件下发生如下反应:2A(g)+B(g)![]() XC(g),经 2 s后反应达平衡,测得 C 的浓度为 0.6 mol·L-1 ,B的物质的量为1.4 mol,现有下列几种说法:
XC(g),经 2 s后反应达平衡,测得 C 的浓度为 0.6 mol·L-1 ,B的物质的量为1.4 mol,现有下列几种说法:
①用物质 A 表示的反应的平均速率为 0.3 mol/(L·s)
②反应前容器内的压强与平衡后容器内的压强之比为1:1
③ 2 s 时物质A的转化率为30% ④ X="2"
其中正确的是
A. ①③④B. ①④C. ②③D. ③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com