
| A. | MgO固体(Al2O3) | B. | Na2CO3固体(NaHCO3) | ||
| C. | FeCl2溶液(CuCl2) | D. | Fe2O3固体(SiO2) |
分析 A.氧化铝与NaOH反应,而MgO不能;
B.碳酸氢钠与NaOH反应生成碳酸钠;
C.二者均与NaOH反应;
D.二氧化硅与NaOH反应,而氧化铁不能.
解答 解:A.氧化铝与NaOH反应,而MgO不能,则选择NaOH溶液反应后,过滤可除杂,故A正确;
B.碳酸氢钠与NaOH反应生成碳酸钠,则加碳酸钠溶液、蒸发结晶可除杂,故B正确;
C.二者均与NaOH反应,不能除杂,应选铁粉、过滤除杂,故C错误;
D.二氧化硅与NaOH反应,而氧化铁不能,则选择NaOH溶液反应后,过滤可除杂,故D正确;
故选C.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、发生的反应、混合物分离方法为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | ①⑤ | B. | ③④ | C. | ② | D. | 全都不行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol H+含有的电子数 | |
| B. | 标准状况下,22.4L酒精所含的分子数 | |
| C. | 1.6 g CH4 含有的质子数 | |
| D. | 1L 1mol/L的硫酸钠溶液所含的Na+ 数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Cu2+、Cl-、SO42- | B. | Na+、HCO3-、Cl-、NO3- | ||
| C. | Na+、SO32-、NO3-、K+ | D. | K+、SO42-、Mg2+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | P-P键的键能大于P-Cl键的键能 | |
| B. | 可求Cl2(g)+PCl3(g)═PCl5(s)的反应热△H | |
| C. | Cl-Cl键的键能$\frac{b-a+5.6c}{4}$ kJ•mol-1 | |
| D. | 1molP4含4molp-p键 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
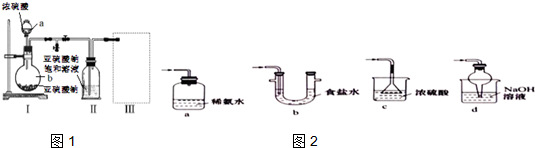
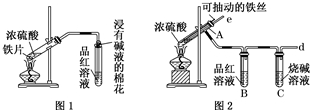 某校化学兴趣小组为探究铁与浓硫酸反应,设计了图1、图2所示装置进行实验.
某校化学兴趣小组为探究铁与浓硫酸反应,设计了图1、图2所示装置进行实验.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
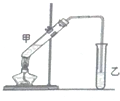 俗话说,“陈酒老醋特别香”,其原因是酒在储存过程中生成了有香味的乙酸乙酯,在实验室里我们也可以用如图所示的装置来模拟该过程.请回答下列问题:
俗话说,“陈酒老醋特别香”,其原因是酒在储存过程中生成了有香味的乙酸乙酯,在实验室里我们也可以用如图所示的装置来模拟该过程.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
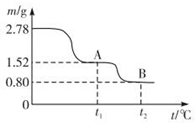
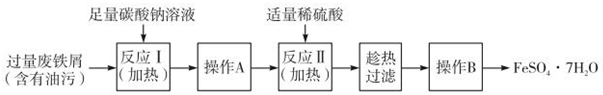
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com