
����Ŀ����Cl2����ijЩ�����л���ʱ�����������HCl�����÷�ӦA����ʵ���ȵ�ѭ�����ã���ӦA�� 4HCl+O2 ![]() 2Cl2+2H2O
2Cl2+2H2O
��֪��������ӦA�У�4mol HCl���������ų�115.6kJ��������
���� 
��1����ӦA���Ȼ�ѧ����ʽ�� ��
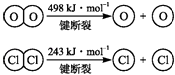
��2���Ͽ�1mol H��O����Ͽ�1mol H��Cl�������������ԼΪkJ��H2O��H��O����HCl��H��Cl�����ǿ���������� ��
���𰸡�
��1��4HCl��g��+O2��g��?2Cl2��g��+2H2O��g����H=��115.6 KJ/mol
��2��32��ǿ
���������⣺��1�����ݷ�ӦA�У�4mol HCl���������ų�115.6kJ����������Ӧ���Ȼ�ѧ����ʽΪ��4HCl��g��+O2��g��2Cl2��g��+2H2O��g����H=��115.6 KJ/mol���ʴ�Ϊ��4HCl��g��+O2��g��2Cl2��g��+2H2O��g����H=��115.6 KJ/mol����2���ʱ�=��Ӧ��ϼ������������������γɻ�ѧ���ų�������4HCl��g��+O2��g��2Cl2��g��+2H2O��g����H=��115.6 KJ/mol��4��E��H��Cl��+498��[243��2+4��E��H��O��]=��115.6���õ�4��E��H��O����4��E��H��Cl��=498��486+115.6=127.6E��H��O����E��H��Cl��=31.9��32��H2O��H��O����HCl��H��Cl��ǿ���ʴ�Ϊ��32��ǿ�� ��1����ӦA�У�4mol HCl���������ų�115.6kJ�������������Ȼ�ѧ����ʽ��д��������ע���ʾۼ�״̬�Ͷ�Ӧ�ʱ�д������2�����ݷ�ӦA�У�4mol HCl���������ų�115.6kJ���������ʱ�=��Ӧ��ϼ������������������γɻ�ѧ���ų��������㣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ���ܴﵽĿ�ĵ���
A. ���ȳ�ȥNa2CO3�����е�NaHCO3
B. ��NaOH��Һ��ȥCO2�е�SO2����
C. ����ˮ��ȥFe2(SO4)3��Һ�е�����FeSO4
D. ��BaCl2��Һ��ȥNaCl��Һ�е�K2SO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ��������Ҫ����2 mol/L��NaCl��Һ950 mL������ʱӦѡ�õ�����ƿ�Ĺ��ͳ�����NaCl�������ֱ��ǣ�������
A. 950mL��111.2g B. 500mL��117g
C. 1000mL��l17g D. ������117g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ������ˮ��Һ��ֻ���ܺ������������е�������:K+��NH4+��Cl-��Mg2+��Ba2+��CO32-��SO42-����ȡ����100mL����Һ��������ʵ��:(1)��һ�ݼ���AgNO3��Һ�г���������(2)�ڶ��ݼ�����NaOH��Һ���Ⱥ��ռ�������0.04 mol��(3)�����ݼ�����BaCl2��Һ���������õ�����6.27g������������ϴ�ӡ����������������Ϊ2.33g����������ʵ�飬�����Ʋ���ȷ����
��K+һ����������100mL��Һ�к�0.01molCO32-����Cl-���ܴ������� Ba2+һ������������Mg2+���ܴ���
A. �ڢۢ� B. �ۢܢ� C. �٢ڢ� D. �٢ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ��ʾ�ش��й����⣺ 
��1���׳�Ϊ��ѡ�ԭ��ء����ء�����
��2���ҳ���Zn���Ϸ�����Ӧ�ĵ缫��ӦʽΪ�� ��
��3��ʯīA���ռ���1.12L���壨����£�����Ӧ������ת�Ƶĵ�����Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ϡ��֮����������ڡ���ѧ���ӹ������н������������ʣ������й�˵������ȷ����
A. ��̬CO2 �׳Ƹɱ��������ŷ����������ЧӦ
B. �ⵥ��������������ָ���ⵥ�������绯ΪI-��IO3-,��������гɵⵥ��
C. CO������ú���ж���������ú����ȡůʱ�������ڷ���һ��ˮ���Ϳ�����Ч��ֹ�ж�
D. NO����������������Ļ�������ǿ����������������ָ:��ѹ�ŵ��������N2��O2����NO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ʵ����ʺ���;���������
A. Na2O2 ����ɫ���塢������ B. Fe2O3����ɫ��ĩ������ԭ��
C. Cl2 dz��ɫ���塢����ˮ���� D. SO2 ��ɫ���塢��ҵ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ��Һ�д��ڷ�Ӧ��Ag����Fe2��Ag(s)��Fe3��+Q���ﵽƽ���Ϊʹƽ����ϵ����������������ɲ�ȡ�Ĵ�ʩ�ǣ� ��
A.�����¶�B.��ˮϡ��C.����Fe2����Ũ��D.�����¼�ѹ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����С��ľ̿�ھƾ������������ȣ�Ѹ��Ͷ���ȵ�Ũ�����У��������ҷ�Ӧ��ͬʱ�д�������ɫ���������Һ����ľ̿Ѹ��ȼ�շ���������
��1��д������ľ̿���ȵ�Ũ��������ΪCO2�Ļ�ѧ����ʽ ��
��2��ľ̿��Ũ���ᷴӦ�����л�������Ũ����ķֽ⣬���˲��������⣬Ҳ��������ɫ���壮��ͬ�����¸÷ֽⷴӦ���������������ɫ��������֮��Ϊ ��
��3��ij�о���ѧϰС���ͬѧ�ԡ�ľ̿��Һ����Ѹ��ȼ�շ�����������ԭ������3�����룺 ����һ����ͬѧ��Ϊ������O2֧��ľ̿ȼ��
���������ͬѧ��ΪŨ����ֽ������O2֧��ľ̿ȼ��
����������ͬѧ��Ϊ��Ӧ������NO2֧��ľ̿ȼ��
�ٸ���ľ̿�ڿ�����ȼ�յ�����ͬѧ�IJ������Բ������������� ��
�����۷�����ͬѧ�IJ���Ҳ����ȷ��ԭ���� ��
��Ҫ֤ʵ��ͬѧ�IJ��룬���貹���ʵ�鷽��������д��ʵ�����������ͽ��ۣ���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com