
����Ŀ��I��������ͼװ�ÿ���֤ͬ����Ԫ�طǽ����Եı仯����
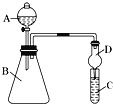
(1)����A������Ϊ______________�������D��������______________��
(2)��Ҫ֤���ǽ����ԣ�Cl��I����A�м�Ũ���ᣬB�м�KMnO4��(KMnO4��Ũ���᳣���·�Ӧ��������)��C�мӵ��۵⻯�ػ����Һ��װ��C�е�ʵ������Ϊ������Һ������д��ʹ������Һ���������ӷ���ʽ__________________________________________��
(3)ʵ����������ҩƷ����ϡ���� ��ϡ���� ��Na2SiO3��Һ ��Na2CO3 ��CaCO3���壬��ѡ�����ҩƷ���ʵ����֤C��Si��S�ķǽ����Եı仯���ɣ�װ��A��B����װҩƷ�ֱ�Ϊ_______��____________��(�����)
������Zn��Cu2��===Zn2����Cu�ķ�Ӧ���ԭ��ء�
(1)ԭ�����ʹ�õĵ������Һ��__________________��
(2)д���缫��Ӧʽ��������___________________________������______________________________��
(3) ����������6.02��1023������ͨ��ʱ����ظ�����������____________g��
���𰸡���Һ©�� ������ Cl2 +2I- = I2 + 2Cl- �� �� CuSO4 /CuCl2/Cu(NO3)2 Zn - 2e- = Zn2+ Cu2+ +2e- =Cu 32.5g
��������
I����1�����������Ĺ���д������A�����ƣ����θ���ܾ��з�ֹ���������ã�
��2�����ʵ����֤�ǽ����ԣ�Cl>I������������KI������ԭ��Ӧ����֤��
��3��Ҫ֤���ǽ����ԣ�S>C>Si������ǿ��������ԭ��֤����
������ʧ�������Ը�����Zn������ѡ���п�����Ͳ�Ľ�����ʯī���������Һ���ݷ���ʽ��֪��ѡ�������ͭ�Ρ�
I����1������AΪ��Һ©�������θ����D�ܹ���ֹ���������Ա���C��Һ�������ƿ�У�
�𰸣���Һ©�� ������
��2�����ʵ����֤�ǽ����ԣ�Cl>I������������KI������ԭ��Ӧ����֤����װ��A��B��C����װҩƷӦ�ֱ�ΪŨ���ᡢKMnO4�����۵⻯�أ�װ��C�е�ʵ������Ϊ��Һ������װ��C�з�����Ӧ�����ӷ���ʽΪCl2 +2I- = I2 + 2Cl-��
�𰸣�Cl2 +2I- = I2 + 2Cl-
��3���ǽ�����Խǿ�����������ˮ��������Խǿ��Ҫ֤���ǽ����ԣ�S>C>Si������ǿ��������ԭ��֤����A�п��Լ����ᣬB�м�Na2CO3��H2SO4+Na2CO3=Na2SO4+H2O+CO2����Ȼ���CO2ͨ��C�е�Na2SiO3�У����Է�����Ӧ��Na2SiO3+CO2+H2O=H2SiO3��+Na2CO3��������ɫ��״�������Ӷ�����֤�����ԣ�H2SO4>H2CO3>H2SiO3���ʷǽ����ԣ�S>C>Si��
�𰸣� �� ��
�������Ϸ�����֪
(1)ԭ�����ʹ�õĵ������Һѡ�������ͭ�Σ�
�𰸣�CuSO4 /CuCl2/Cu(NO3)2
(2)д���缫��Ӧʽ��������Zn - 2e- = Zn2+��������Cu2+ +2e- =Cu��
�𰸣�Zn - 2e- = Zn2+ Cu2+ +2e- =Cu
(3) ����������6.02��1023������ͨ��ʱ������п0.5mol������0.5mol��65g/mol=32.5g��
�𰸣�32.5


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������һ�ֹ�ҵ��������Ҫ�ɷ�ΪMgCO3��MgSO4����������Fe��Al����������Ϊԭ���Ʊ�MgCO3��3H2O��ʵ���������:

��1��Ϊ�ӿ���������,�ɲ�ȡ�İ취��______,д������ʱ��������Ҫ�ɷַ�����Ӧ�Ļ�ѧ����ʽΪ_________________��
��2������H2O2����ʱ������Ӧ�����ӷ���ʽΪ_________________��
��3������ȡ��Һ�ķ�����ȥ��Һ�е�Fe3+��
�ټ�����Һ���Ƿ���Fe3+������Լ���_________________��
��ΪʹFe3+ �����ܶ�ش�ˮ��ת�����л���,��ȡ�IJ���:��ˮ��Һ�м���һ��������ȡ����_______�����á���Һ,���ظ���Ρ�
����ȡʱ,������Һ����Fe2+��Al3+��Mg2+���м�����������,ʹFe2+ ��Cl-����[FeCl4]-,��������������(Et2O)������ȡ,������H+���,����������Et2O��H+,����[FeCl4]-��Et2O��H+���������γɵ���Et2O��H+��[FeCl4]-���õ�����,Cl-��Et2O�ֱ�ȡ����Fe2+��H+����λˮ����,�����к��˵��,������ˮ��,�ܹ����������С����,�ʹ�ˮ��ת�Ƶ��л����С�����ȡ��������ȡAl3+��Mg2+��ԭ����_________��
��4����֪:Ksp[Al(OH)3]=1.0��10-33,Ksp[(Mg(OH)2)=1.0��10-12.pH=8.5ʱMg(OH)2��ʼ������������,��ȥMgSO4��Һ�е�Al3+��ʹ��Ũ��С��1��10-6mol��L-1��,����백ˮ������ҺpH�ķ�ΧΪ____________��
��5������Һ�м���Na2CO3��Һ����MgCO3 ������������ˮϴ��,��������Ƿ�ϴ���IJ�����________________��
��6������ʱ����¸���¶Ƚϸ�ʱ��������Ӧ,д��MgCO3��3H2O��323K�¶�ʱ����ת���Ļ�ѧ����ʽ________________��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������G�Ǻϳɿ�����ҩ������������м��壬��ͨ�����·����ϳɣ�

��������E�еĺ�������������Ϊ___________��
��B��C�ķ�Ӧ����Ϊ___________��
��D����ԭ�õ�E��D�ķ���ʽΪC14H9O5N��д��D�Ľṹ��ʽ___________��
��д��ͬʱ��������������F��һ��ͬ���칹��Ľṹ��ʽ��___________��
�������к����������������ܷ���ˮ�ⷴӦ�����������ʣ�����һ������FeCl3��Һ������ɫ��Ӧ����һ���ܷ���������Ӧ����������ֻ��3�ֲ�ͬ��ѧ�������⡣
����֪��Na2Cr2O7��������![]() ����RΪ��������
����R��������
���� ��CH3OHΪԭ���Ʊ�
��CH3OHΪԭ���Ʊ�![]() ��д���ϳ�·������ͼ(���Լ�����ѡ)��________�ϳ�·������ͼʾ�����£�
��д���ϳ�·������ͼ(���Լ�����ѡ)��________�ϳ�·������ͼʾ�����£�
![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ�ص����ӣ�![]() ������ͬ�ĵ��Ӳ�ṹ�����й�ϵ�в���ȷ����( )
������ͬ�ĵ��Ӳ�ṹ�����й�ϵ�в���ȷ����( )
A. ��������![]() B. ��ԭ�ԣ�
B. ��ԭ�ԣ�![]()
C. �����ԣ�![]() D. �뾶��
D. �뾶��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܱ���Ϊ21������߷�չDZ���������Դ���俪�������ǿ�ѧ�����о�����Ҫ���⡣�Իش��������⣺
(1)�뻯ʯȼ����ȣ�������Ϊȼ�ϵ��ŵ���_________(���ٴ������)��
(2)������ֱ��ȼ����Ƚϣ���Ƴ������ؿ��Դ�����������ת���ʣ��������س������д���Ͻ�M������ת��ΪMH2���ܷ�ӦΪ��xNi(OH)2+M![]() xNiOOH+MHx����д���ŵ�����и���
xNiOOH+MHx����д���ŵ�����и���
��Ӧʽ____________��
(3)ʩ������Sehlesinger�������������NaBH4��ˮ��Ӧ��������BH4-+2H2O=BO2-+4H2������֪NaBH4��ˮ��Ӧ��������Һ�Լ��ԣ���Һ�и�����Ũ�ȴ�С��ϵΪ__________�������ӷ���ʽ��ʾ����Һ�Լ��Ե�ԭ��_______________��
(4)���ݻ���ΪVL�Ģ�������ͬ�ܱ������У��ֱ����ag�Ĵ���Ͻ�M����bmol�����������·�Ӧ��2M(s)+xH2(g)![]() 2MHx(s) ��H<0�����������ķ�Ӧ�¶ȷֱ�ΪT1��T2��T3�Һ㶨���䣬������������ͬ������£�ʵ���÷�Ӧ�����е�1minʱM��������ͼ1��ʾ����ʱ������������һ���ﵽ��ѧƽ��״̬����___________��������������Ӧ���ﵽ��ѧƽ��ʱ��H2ת�������ķ�Ӧ�¶���______��
2MHx(s) ��H<0�����������ķ�Ӧ�¶ȷֱ�ΪT1��T2��T3�Һ㶨���䣬������������ͬ������£�ʵ���÷�Ӧ�����е�1minʱM��������ͼ1��ʾ����ʱ������������һ���ﵽ��ѧƽ��״̬����___________��������������Ӧ���ﵽ��ѧƽ��ʱ��H2ת�������ķ�Ӧ�¶���______��

(5)������Խ����л���������ұ��뱽��ϩ֮��Ŀ��淴Ӧ��ʵ������ͼ��⣻

���ں����ܱ������У����Ʋ�ͬ�¶Ƚ����ұ�������ʵ�顣���ұ���ʼŨ�Ⱦ�Ϊc mol/L�ⶨ�ұ���ת���ʣ������ͼ2��ʾ��ͼ��AΪ�ұ���ƽ��ת�������¶ȹ�ϵ���ߣ�B���߱�ʾ��ͬ�¶��·�Ӧ������ͬʱ����Ϊ�ﵽ��ѧƽ��ʱ�ұ���ת���ʡ���˵�����¶ȵ����ߣ�����B������A�ƽ���ԭ��__________��
��ά����ϵ��ѹ�㶨�����¶�Tʱ�����ʵ���Ϊn�����ΪV���ұ��������������⡣��֪�ұ���ƽ��ת����Ϊa�����ڸ��¶��·�Ӧ��ƽ�ⳣ��K=__________����a�ȷ��ű�ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�����ӷ���ʽ��д��ȷ����(����)
A.�ƺ���ˮ��Ӧ��Na��2H2O=Na����2OH����H2��
B.��������������������Һ��Al��2OH��=AlO2-��H2��
C.����������������2Al��6H��=2Al3����3H2��
D.����ϡ���ᷴӦ��2Fe��6H��=2Fe3����3H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����(����)
A. CO2�����鶼������������
B. �ø���������ȼ���Ҵ�����������Դ�������Ҵ�ȼ�ϲ��������������
C. ̫���ܡ����ܺ�����������������Դ
D. ̫���ܵ�ؿɽ�̫����ֱ��ת��Ϊ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ģ���һ����Fe��Fe2O3�Ļ�����м���120mLһ��Ũ�ȵ�ϡ����ǡ��ʹ������ܽ⣬ͬʱ�ɵõ���״����1.344L NO���壮�����õ�����Һ���ټ���KSCN��Һ����ɫ���֣�����������H2�ڼ��������»�ԭ��ͬ�����Ļ����õ�11.76g�����ʣ���ԭϡ��������ʵ���Ũ��Ϊ��������
A. 2molL-1 B. 4molL-1
C. 5.75molL-1 D. ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ����ʾ��Mg2����Al3����NH4��������Һ�еμ�NaOH��Һʱ������������NaOH������Ĺ�ϵͼ��

���и�������ʾ��ͼһ�µ���
A. ͼ���������ӵ����ʵ���֮��Ϊ:n(Mg2��):n(Al3��):n(NH4��)��2:3:2
B. ͼ����ʹ�õ�NaOH��Ũ��Ϊ2mol/L
C. ͼ��������A��Ӧ��������C����H>0
D. ͼ�������߱�ʾij��Ӧ���̵������仯�� ��ʹ�ô�����B��ή��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com