
【题目】乙酰水杨酸,俗称阿司匹林(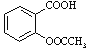 ),是常用的解热镇痛药。实验室合成流程如下:
),是常用的解热镇痛药。实验室合成流程如下:
![]()
查阅资料:
阿司匹林:受热易分解,溶于乙醇、难溶于水
水杨酸(邻羟基苯甲酸):溶于乙醇、微溶于水
醋酸酐[(CH3CO)2O]:无色透明液体,溶于水形成乙酸
请根据以上信息回答下列问题:
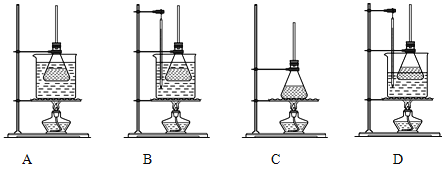
(1)①合成阿司匹林时,下列几种加热方式最合适的_____________。
②合成阿司匹林使用的锥形瓶必须干燥的原因是______________。
③如右图所示装置,通过抽滤可使粗产品与母液分离。下列说法不正确的是____________。
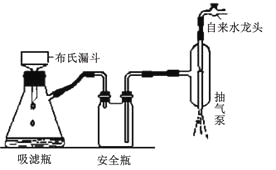
A.抽滤能加快过滤速率,得到相对干燥的沉淀,但颗粒太小的沉淀不能用此装置
B.当溶液具有强酸性、强氧化性时,可用玻璃砂漏斗代替布氏漏斗
C.抽滤时,当吸滤瓶内液面快到支管口时,先拔掉吸滤瓶上橡皮管,再从吸滤瓶支管口倒出溶液
D.洗涤晶体时,先关闭水龙头,用洗涤剂缓慢淋洗,再打开水龙头抽滤
(2)提纯粗产物中加入饱和NaHCO3溶液至没有CO2产生为止,再抽滤。加入饱和NaHCO3溶液的目的是(用化学反应方程式表示)__________________。
(3)另一种改进的提纯方法,称为重结晶提纯法。
![]()
①最后步骤中洗涤剂最好选择_______________。
A.15%的乙醇溶液 B.NaOH溶液 C.冷水 D.滤液
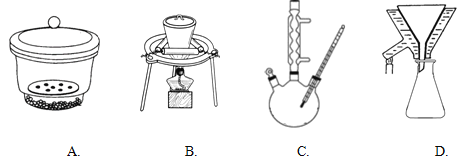
②下列装置在上述流程中肯定用不到的是_______________。
③重结晶时为了获得较大颗粒的晶体产品,查阅资料得到如下信息:
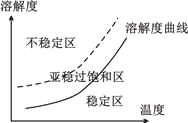
1.不稳定区出现大量微小晶核,产生较多颗粒的小晶体
2.亚稳过饱和区,加入晶种,晶体生长
3.稳定区晶体不可能生长
由信息和已有的知识分析,从温度较高浓溶液中获得较大晶体颗粒的操作为______________。
【答案】B 防止乙酸酐水解(或与水反应) CD 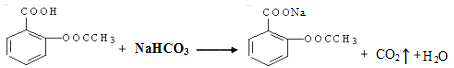 C B (在亚稳过饱和区)加入晶种,缓慢降温
C B (在亚稳过饱和区)加入晶种,缓慢降温
【解析】
(1)①控制温度在85℃~90℃,温度低于100℃,应采取水浴加热,故选B;
②乙酸酐容易发生水解生成乙酸,故仪器应干燥防止乙酸酐水解,故答案为防止乙酸酐水解;
③A、抽滤能加快过滤速率,得到相对干燥的沉淀,颗粒太小的沉淀会穿过滤纸,不能用此装置,故A正确;B、当溶液具有强酸性、强氧化性时会腐蚀滤纸,可用玻璃砂漏斗代替布氏漏斗,故B正确;C、当吸滤瓶中液面快达到支管口位置时,应拔掉吸滤瓶上的橡皮管,从吸滤瓶上口倒出溶液,故C错误;D、洗涤晶体时,先关小水龙头,不是关闭水龙头,然后蒸馏水缓缓淋洗,再打开水龙头抽滤,故D错误;故选CD;
(2)乙酰水杨酸能和碳酸氢钠反应生成二氧化碳气体,所以判断该过程结束的现象是没有气体(CO2)产生;使乙酰水杨酸转化为易溶于水的乙酰水杨酸钠,乙酰水杨酸钠易溶于水,从而除去杂质,且便于分离,反应的化学方程式为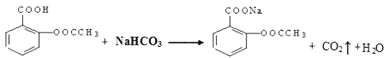
(3)①阿司匹林:受热易分解,溶于乙醇、难溶于水,最后步骤中洗涤剂最好冷水,故选C;
②根据流程图,冷凝回流需要C,趁热过滤需要D,干燥时需要A,不需使用的装置是B,故选B;
③根据信息,重结晶时为了获得较大颗粒的晶体产品,操作为在亚稳过饱和区加入晶种,缓慢降温,故答案为在亚稳过饱和区加入晶种,缓慢降温。


科目:高中化学 来源: 题型:
【题目】A、B、C、D是四种短周期元素,E是过渡元素,A、B、C同周期,C、D同主族,A原子M层电子数是L层的一半,B是同周期第一电离能最小的元素,C在同周期中未成对电子数最多,E的外围电子排布式为3d64s2。回答下列问题:
(1)写出下列元素的名称:A __ B___ C ___ D ___
(2)上述五种元素中最高价氧化物对应水化物酸性最强的是(用化学式表示,下同)____,碱性最强的是______ 。
(3)D所在周期第一电离能最小的元素是_____,电负性最大的元素是_____。(填元素符号)
(4)D的氢化物比C的氢化物的沸点__(填“高”或“低”),原因是 ___________。
(5)E元素原子的核电荷数是____,E元素在周期表的位置是 _____,E元素处于周期表分区中的____区。
(6)画出D的核外电子排布图________,E的外围电子排布图_________。
(7)用电子式表示B的硫化物的形成过程:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题
(1)立方烷 ![]() 的六氯代物有_________种。
的六氯代物有_________种。
(2)甲基的电子式 ________________________。
(3)![]() 的系统命名________________________________________。
的系统命名________________________________________。
(4)下列物质的沸点按由高到低的顺序排列的是______________。
①CH3(CH2)2CH3 ②CH3(CH2)3CH3 ③ (CH3)3CH ④ (CH3)2CHCH2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某硫酸厂用以下几种方法处理SO2尾气。
(1)活性炭还原法
反应原理:恒温恒容2C(s)+2SO2(g)![]() S2(g)+2CO2(g)。
S2(g)+2CO2(g)。
反应进行到不同时间测得各物质的浓度如图:
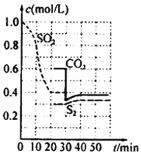
①第一次出现平衡的时间是第__min;
②0~20min反应速率表示为v(SO2)=__;
③30min时,改变某一条件平衡移动,则改变的条件最有可能是__;40min时,平衡常数值为__。
(2)亚硫酸钠吸收法
常温下,Na2SO3溶液吸收SO2生成NaHSO3,当吸收至pH=6时,吸收液中相关离子浓度关系一定正确的是__(填序号)。
a.c(Na+)+c(H+)>c(SO![]() )+c(HSO
)+c(HSO![]() )+c(OH-)
)+c(OH-)
b.c(Na+)=c(SO![]() )+c(HSO
)+c(HSO![]() )+c(H2SO3)
)+c(H2SO3)
c.水电离出的c(OH-)=1×10-8mol·L-1
d.c(Na+)>c(SO![]() )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
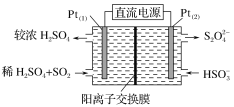
(3)电化学处理法
如图所示,Pt(1)电极的反应式为__;碱性条件下,用Pt(2)电极排出的S2O![]() 溶液吸收NO2,使其转化为N2,同时有SO
溶液吸收NO2,使其转化为N2,同时有SO![]() 生成。若阳极转移电子6mol,则理论上处理NO2气体__g。
生成。若阳极转移电子6mol,则理论上处理NO2气体__g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今有甲、乙、丙、丁、戊5种物质,在一定条件下,它们能按下图方式进行转化:
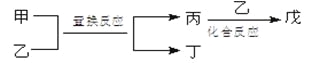
其推断正确的是
选项 | 甲 | 乙 | 丙 | 丁 | 戊 |
A | NH3 | O2 | NO | H2O | NO2 |
B | Mg | CO2 | C | MgO | CO |
C | C | H2O | CO | H2 | HCOOH |
D | FeBr2 | Cl2 | FeCl2 | Br2 | FeCl3 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的叙述正确的是
A.乙醇是良好的有机溶剂, 75 % 的酒精还可以灭活新冠病毒
B.苯酚有毒,沾到皮肤上可用 65 ℃的以上热水洗涤
C.乙烯、聚氯乙烯和苯分子中碳原子的杂化方式相同
D.有机物![]() 的名称是2-甲基-2-丁烯
的名称是2-甲基-2-丁烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,浓度都是1mol·L-1的两种气体X2和Y2在密闭容器中反应,经过tmin后,测得物质的浓度分别为:c(X2)=0.4mol·L-1,c(Y2)=0.8mol·L-1,则该反应的方程式可表示为()
A. X2+2Y2![]() 2XY2B. 2X2+Y2
2XY2B. 2X2+Y2![]() 2X2Y
2X2Y
C. X2+3Y2![]() 2XY3D. 3X2+Y2
2XY3D. 3X2+Y2![]() 2X3Y
2X3Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼酸三甲酯用作柠檬类水果的熏蒸剂。实验室合成硼酸三甲酯的原理及装置如下:Na2B4O710H2O+2H2SO4+12CH3OH![]() 2NaHSO4+4(CH3O)3B+17H2O
2NaHSO4+4(CH3O)3B+17H2O
已知:
硼酸三甲酯 | 甲醇 | |
溶解性 | 与乙醚、甲醇混溶,能水解 | 与水混溶 |
沸点/℃ | 68 | 64 |
硼酸三甲酯与甲醇混合物的共沸点为54℃ | ||
实验步骤如下:
①在圆底烧瓶中加入44.8g甲醇和191.gNa2B4O710H2O(硼砂,式量为382),然后缓慢加入浓H2SO4并振荡;加热烧瓶中的液体;通过分馏柱回流一段时间。
②先接收51~55℃的馏分,再接收55~60℃的馏分。
③将两次馏分合并,加入氯化钙进行盐析分层,上层为硼酸三甲酯,分离。
④精馏得高纯硼酸三甲酯19.2g。
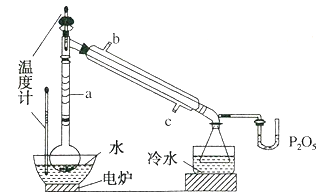
回答下列问题:
(1)图中仪器a的名称为__;直形冷凝管冷却水应从__(填“b”或“c”)接口进入。
(2)本实验加热方式为__,优点是__。
(3)加入氯化钙盐析分层的主要目的是__。
(4)U型管中P2O3的作用是__。
(5)图中,步骤④的仪器选择及安装都正确的是__,应收集__℃的馏分。
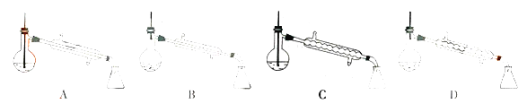
(6)本次实验的产率是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各溶液中微粒的物质的量浓度关系正确的是
①c(NH![]() )相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液中:c(NH4HSO4)>c[(NH4)2SO4]>c(NH4Cl)
)相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液中:c(NH4HSO4)>c[(NH4)2SO4]>c(NH4Cl)
②向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
③1.0mol/LNa2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3)
④某二元弱酸的酸式盐NaHA溶液中:c(H+)+c(Na+)=c(OH-)+c(HA-)+c(A2-)
⑤将pH=6的H2SO4稀释1000倍后,c(H+)=200c(SO![]() )
)
A.①②B.③⑤C.④⑤D.②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com