
(8分)某强酸性溶液X含有Ba2+、Al3+、NH4+、Fe2+、Fe3+、CO32-、SO32-、SO42-、Cl-、NO3-中的一种或几种,取该溶液进行实验,实验内容如下:
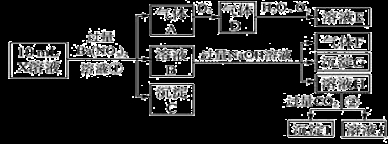
根据以上信息,回答下列问题:
(1)溶液X中除H+外还肯定含有的离子是___________;
(2)写出有关离子方程式:
步骤①中生成A:____________;步骤②生成沉淀I:__________。
(3)假设测定A、F、I均为0.01 mol,10 mL X溶液中n(H+)=0.04 mol,而沉淀C物质的量0.07 mol,能说明该溶液不能确定的阴离子存在的理由是___________________。
 名题金卷系列答案
名题金卷系列答案科目:高中化学 来源:2015-2016学年河北省高二上学期第一次月考化学试卷(解析版) 题型:选择题
已知①CH3COOH(l)+2O2(g)===2CO2(g)+2H2O(l) ΔH1=-870.3 kJ/mol
②C(s)+O2(g)===CO2(g) ΔH2=-393.5 kJ/mol
③H2(g)+ O2(g)===H2O(l) ΔH3=-285.8 kJ/mol
O2(g)===H2O(l) ΔH3=-285.8 kJ/mol
则2C(s)+2H2(g)+O2(g)===CH3COOH(l)的反应热为
A.-870.3 kJ/mol B.-571.6 kJ/mol
C.+787.0 kJ/mol D.-488.3 kJ/mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高一9月检测化学试卷(解析版) 题型:填空题
氧化还原反应的实质是___________;元素的化合价降低,发生的是__________反应;氧化还原反应中,还原剂_____________电子(填“得”或“失”);试写出Na 2 O 2 与H 2 O反应的化学方程式,并用双线桥标出电子转移的方向和数目: _____________。
查看答案和解析>>
科目:高中化学 来源:2016届重庆市高三上学期开学考试化学试卷(解析版) 题型:推断题
[化学-选修2:有机化学基础](12分)化合物G是一种医药中间体,常用于制备抗凝血药。可以通过下图所示的路线合成:

已知:RCOOH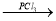 RCOCl;D与FeCl3溶液能发生显色。
RCOCl;D与FeCl3溶液能发生显色。
请回答下列问题:
(1)B→C的转化所加的试剂可能是___________,CH3COCl+E→F的反应类型是_________。
(2)有关G的下列说法正确的是________。
A.属于芳香烃
B.能与FeCl3溶液发生显色反应
C.可以发生水解、加成、氧化、酯化等反应
D.1mol G最多可以跟4mol H2反应
(3)E的结构简式为__________。
(4)F与足量NaOH溶液充分反应的化学方程式为________。
(5)写出同时满足下列条件的E 的所有同分异构体的结构简式___________。
的所有同分异构体的结构简式___________。
①能发生水解反应
②与FeCl3溶液能发生显色反应
③苯环上有两种不同化学环境的氢原子
查看答案和解析>>
科目:高中化学 来源:2016届云南省高三第一次月考试卷化学试卷(解析版) 题型:选择题
用丙醛(CH3-CH2-CHO)制聚丙烯 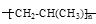 过程中发生的反应类型为
过程中发生的反应类型为
①取代 ②消去 ③加聚 ④缩聚 ⑤氧化 ⑥还原
A.①④⑥ B.⑤②③ C.⑥②③ D.②④⑤
查看答案和解析>>
科目:高中化学 来源:2016届四川省高三9月月考化学试卷(解析版) 题型:选择题
下列各组离子一定能在指定环境中大量共存的是
A.在c(HCO3-)=0.1 mol·L-1的溶液中:NH4+、AlO2-、Cl-、NO3-
B.常温下,在由水电离出的c(H+)=1×10-12 mol·L-1的溶液中:Fe2+、ClO-、Na+、SO42?
C.在加入铝粉产生H2的溶液中:SO42-、NO3-、Na+、NH4+
D.在使红色石蕊试纸变蓝的溶液中:SO32-、CO32-、Na+、K+
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省高三上学期一模化学试卷(解析版) 题型:选择题
下面是溶解性表中的部分内容(室温下测定):
阳离子 | 阴离子 | ||
OH- | SO42- | SO32- | |
Ca2+ | ① | 微 | 不 |
Fe3+ | 不 | 溶 | ② |
Cu2+ | 不 | ③ | 不 |
下列有关说法中正确的是
A.①处物质属于可溶性碱
B.②处物质组成为Fe2(SO3)3
C.③处物质为硫酸盐或者铜盐
D.①、③处物质在溶液中发生的反应一定是Cu2++2OH-===Cu(OH)2↓
查看答案和解析>>
科目:高中化学 来源:2016届广东省等六校高三第一次联考化学试卷(解析版) 题型:填空题
(15分)孔雀石主要含Cu2(OH)2CO3,还含少量FeO、SiO2。以孔雀石为原料可制备CuSO4·5H2O步骤如下:
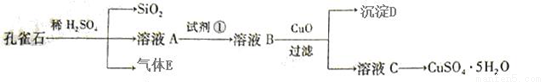
(1)写出孔雀石与稀硫酸反应的化学方程式:___________,
为了提高原料浸出速率,可采取的措施有____________(写出两条)。
(2)溶液A的金属离子有Cu2+、Fe2+。实验步骤中试剂①最佳选 (填代号)。
a.KMnO4 b.Cl2 c.H2O2 d.HNO3
(3)溶液B中加入CuO作用是_________________ ____ 。
(4)常温下Fe(OH)3的Ksp=1×10-39,若要将溶液中的Fe3+转化为Fe(OH)3沉淀,使溶液中c(Fe3+)降低至1×10—3mol/L,必需将溶液pH调节至 。
(5)由溶液C获得CuSO4·5H2O晶体,需要经____________、___________和过滤。
(6)可用KMnO4标准溶液测定溶液A中Fe2+的浓度,量取A溶液20.00ml,用0.010mol/L酸性KMnO4标准溶液滴定,消耗KMnO4 10.00ml, A溶液中Fe2+的物质的量浓度_________mol/L.
(反应原理:MnO4- + 5Fe2++8H+=Mn2++5Fe3++4H2O)
查看答案和解析>>
科目:高中化学 来源:2016届山西省忻州市高三上学期第一次月考化学试卷(解析版) 题型:选择题
烃A分子式为C4H10,分子结构中含有一个次甲基(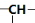 ),则此物质A的二溴代物的种数为
),则此物质A的二溴代物的种数为
A、3种 B、4种 C、5种 D、以上都不对
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com