
【题目】NA表示阿伏加德罗常数,下列有关叙述正确的是( )
①1mol苯乙烯中含有的碳碳双键数为4NA
②6.2g氧化钠和7.8g过氧化钠的混合物中含有的离子总数为0.6NA
③3.4gNH3中含N—H键数目为0.2NA
④常温下1L 0.5mol/L NH4Cl溶液与2L 0.25mol/L NH4Cl溶液所含NH4+的数目相同
⑤常温下4.6gNO2和N2O4混合气体中所含原子总数为3NA
⑥等体积、浓度均为1mol/L的磷酸和盐酸,电离出的氢离子数之比为3:1
⑦1mol铁粉在1mol氯气中充分燃烧,失去的电子数为3NA
⑧高温下,16.8 g Fe与足量水蒸气完全反应失去0.8NA个电子
A. ①④⑦ B. ②⑤⑧ C. ②③④⑥ D. ①②④⑤⑦
【答案】B
【解析】
试题①1mol苯乙烯中含有的碳碳双键数为1NA,故错误;②6.2g氧化钠的物质的量为0.1mol,含有0.2mol钠离子、0.1mol阴离子,总共含有0.3mol离子;7.8g过氧化钠的物质的量为0.1mol,含有0.2mol钠离子、0.1mol过氧根离子,总共含有0.3mol离子,二者的混合物中含有0.6mol离子,含有的离子总数为0.6NA,故正确;③3.4gNH3物质的量=![]() =0.2mol,含N-H键数目为0.6NA,故错误;④浓度越大水解程度越小,1L 0.50molL-1 NH4Cl溶液与2L 0.25molL-1 NH4Cl溶液含NH4+物质的量后者小,故错误;⑤NO2和N2O4的最简式均为NO2,故4.6g混合物中含有的NO2的物质的量为0.1mol,故含0.1mol氮原子和0.2mol氧原子,共含有原子数为0.3NA个,故正确;⑥盐酸为强电解质,溶液中完全电离,1mol/L的盐酸中含有氢离子浓度为1mol/L,而磷酸为弱电解质,1mol/L的磷酸溶液中氢离子浓度小于3mol/L,所以电离出的氢离子数之比小于3:1,故B误;⑦1mol氯气与1mol铁粉反应,氯气不足,完全反应只能得2mol电子,故错误;⑧n=
=0.2mol,含N-H键数目为0.6NA,故错误;④浓度越大水解程度越小,1L 0.50molL-1 NH4Cl溶液与2L 0.25molL-1 NH4Cl溶液含NH4+物质的量后者小,故错误;⑤NO2和N2O4的最简式均为NO2,故4.6g混合物中含有的NO2的物质的量为0.1mol,故含0.1mol氮原子和0.2mol氧原子,共含有原子数为0.3NA个,故正确;⑥盐酸为强电解质,溶液中完全电离,1mol/L的盐酸中含有氢离子浓度为1mol/L,而磷酸为弱电解质,1mol/L的磷酸溶液中氢离子浓度小于3mol/L,所以电离出的氢离子数之比小于3:1,故B误;⑦1mol氯气与1mol铁粉反应,氯气不足,完全反应只能得2mol电子,故错误;⑧n=![]() 计算得到物质的量=
计算得到物质的量=![]() =0.3mol,结合铁和水蒸气反应生成四氧化三铁和氢气计算电子转移数,3Fe~Fe3O4~8e-,则Fe与足量水蒸气完全反应失去0.8NA个电子,故正确;故选B。
=0.3mol,结合铁和水蒸气反应生成四氧化三铁和氢气计算电子转移数,3Fe~Fe3O4~8e-,则Fe与足量水蒸气完全反应失去0.8NA个电子,故正确;故选B。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某无色稀溶液X中,可能含有下表所列离子中的某几种。现取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂的体积(V)的关系如图所示。

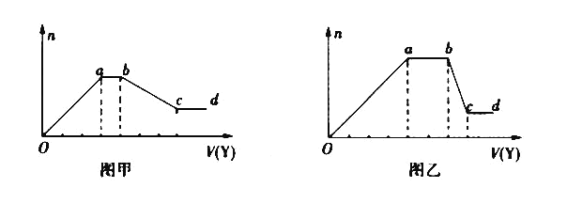
(1)若Y是盐酸,所得到的关系图如图甲所示,则oa段转化为沉淀的离子(指来源于X溶液的,下同)是_____,ab段发生反应的离子是_________,bc段发生反应的离子方程式是_________。
(2)若Y是NaOH溶液,所得到的关系图如图乙所示,则X中一定含有的离子是__________,假设X溶液中只含这几种离子,则溶液中各离子物质的量之比为_____,ab段反应的离子方程式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃,用0.1000mol/L的NaOH溶液滴定40.00mL0.1mol/L的某二元弱酸H2R溶液,所得滴定曲线如图所示(设所得溶液体积等于两种溶液体积之和)。下列说法正确的是
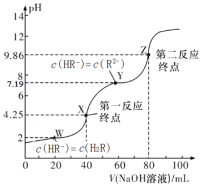
A.若只滴定到第一反应终点,可用酚酞做指示剂
B.图中Y点对应的溶液中:c(Na+)+c(H+)=2c(HR-)+c(OH-)
C.图中Z点对应的溶液中c(Na+)约为0.067mol/L,R2-的水解率大于1%
D.若pK=-lgK,2HR-![]() R2-+H2R达平衡时pK=5.19
R2-+H2R达平衡时pK=5.19
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】B、N、F、Ga、As是新一代太阳能电池、半导体材料中含有的主要元素。回答下列问题:
(1)基态Ga原子的核外电子排布式是__________,基态Ga原子核外电子占据最高能级的电子云轮廓图为________。
(2)在第四周期中,与基态As原子核外未成对电子数目相同的元素为__________。
(3)NF3的立体构型为_______。N2F2分子中各原子都满足8电子结构,分子中σ键和π键的个数比为______,氮原子的杂化轨道类型为__________。
(4)B、Al、Ga单质的熔点依次为2300°C,660°C,29.8°C,解释熔点产生差异的原因______。
(5)由B、N、F组成的某离子化合物中,B、N、F的原子个数比为1:1:8,其阴、阳离子互为等电子体,该化合物中的阳离子、阴离子符号分别为__________。
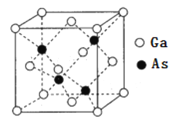
(6)GaAs晶体结构如图所示。
①图中As原子的坐标参数为![]() ,_______。
,_______。
②已知晶胞中相邻且最近的Ga、As原子的核间距为acm,NA为阿伏加德罗常数的值,晶体的密度为___________g/cm3(填写表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁烯是一种重要的化工原料,可由丁烷催化脱氢制备。回答下列问题:
(1)正丁烷(C4H10)脱氢制1-丁烯(C4H8)的热化学方程式如下:
①C4H10(g)= C4H8(g)+H2(g) ΔH1
已知:②C4H10(g)+ ![]() O2(g)= C4H8(g)+H2O(g) ΔH2=-119 kJ·mol-1
O2(g)= C4H8(g)+H2O(g) ΔH2=-119 kJ·mol-1
③H2(g)+ ![]() O2(g)= H2O(g) ΔH3=-242 kJ·mol-1
O2(g)= H2O(g) ΔH3=-242 kJ·mol-1
反应①的ΔH1为________ kJ·mol-1。图(a)是反应①平衡转化率与反应温度及压强的关系图,x_____________0.1(填“大于”或“小于”);欲使丁烯的平衡产率提高,应采取的措施是__________(填标号)。
A.升高温度 B.降低温度 C.增大压强 D.降低压强
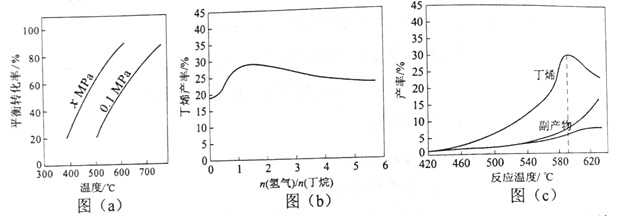
(2)丁烷和氢气的混合气体以一定流速通过填充有催化剂的反应器(氢气的作用是活化催化剂),出口气中含有丁烯、丁烷、氢气等。图(b)为丁烯产率与进料气中n(氢气)/n(丁烷)的关系。图中曲线呈现先升高后降低的变化趋势,其降低的原因是___________。
(3)图(c)为反应产率和反应温度的关系曲线,副产物主要是高温裂解生成的短碳链烃类化合物。丁烯产率在590℃之前随温度升高而增大的原因可能是___________、____________;590℃之后,丁烯产率快速降低的主要原因可能是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(10分)化合物X是一种香料,可采用乙烯与甲苯为主要原料,按下列路线合成:
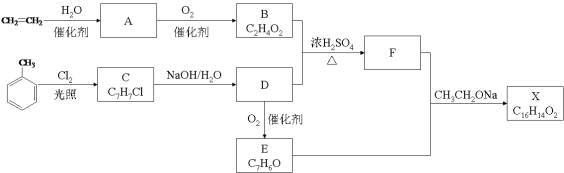
已知:RX![]() ROH;RCHO+CH3COOR’
ROH;RCHO+CH3COOR’![]() RCH=CHCOOR’
RCH=CHCOOR’
请回答:
(1)E中官能团的名称是 。
(2)B+D→F的化学方程式 。
(3)X的结构简式 。
(4)对于化合物X,下列说法正确的是 。
A.能发生水解反应 B.不与浓硝酸发生取代反应
C.能使Br2/CCl4溶液褪色 D.能发生银镜反应
(5)下列化合物中属于F的同分异构体的是 。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾更强,实验室制取高铁酸钠的化学方程式如下 :
(1)请用双线桥法表达出此反应的电子转移情况:__________
2Fe( NO3 )3+16NaOH+3Cl2=2Na2FeO4+6NaNO3 +6NaCl+8H2O
(2)若要制取8.3g高铁酸钠需要标准下Cl2的体积为多少?______若所用氢氧化钠溶液体积为200mL,则氢氧化钠溶液的物质的量浓度是多少?(写出计算过程)_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,下列溶液的离子浓度关系式正确的是
A.稀释氨水溶液 10 倍后,其 c(OH-)为原来的![]()
B.pH 之和为 14 的 H2C2O4与 NaOH 溶液混合:c(Na+)+c(H+)=c(OH-)+ c(HC2O4-)
C.pH=5 的 H2S 溶液中,c(H+)=c(HS-)=1×10-5mol/L
D.将等物质的量的Na2CO3 和 NaHCO3 混合溶于水中![]() <1
<1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三个密闭容器中分别充入N2、H2、O2三种气体,以下各种情况下排序正确的是( )
A. 当它们的温度和压强均相同时,三种气体的密度:ρ(H2)>ρ(N2)>ρ(O2)
B. 当它们的温度和密度都相同时,三种气体的压强:p(H2)>p(N2)>p(O2)
C. 当它们的质量和温度、压强均相同时,三种气体的体积:V(O2)>V(N2)>V(H2)
D. 当它们的压强和体积、温度均相同时,三种气体的质量:m(H2)>m(N2)>m(O2)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com