
【题目】下列离子方程式与所述事实相符且正确的是( )
A. 向明矾溶液中加入过量的氢氧化钡溶液:Al3++2 SO42-+2Ba2++4OH-![]() 2BaSO4↓+ AlO2-+2H2O
2BaSO4↓+ AlO2-+2H2O
B. 稀HNO3 与难溶于水的FeS固体反应:FeS+2H+![]() Fe2++H2S↑
Fe2++H2S↑
C. 向氯化钙溶液中通入CO2气体:Ca2++CO2+H2O![]() CaCO3↓+2H+
CaCO3↓+2H+
D. 强碱溶液中次氯酸钠与Fe(OH)3反应:3ClO-+2Fe(OH)3![]() 2 FeO42-+3Cl-+H2O+4H+
2 FeO42-+3Cl-+H2O+4H+
 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:
【题目】NO是一种性质活泼的大气污染物,它能与很多物质发生反应。
Ⅰ、在2L密闭容器内,800℃时反应:2NO(g)+O2(g)![]() 2NO2 (g)体系中,n(NO)随时间的变化如表:
2NO2 (g)体系中,n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K=_____。已知:![]() >
>![]() ,则该反应是___热反应。
,则该反应是___热反应。
(2)下图中表示NO2的变化的曲线是___________。用O2表示从0-2 s内该反应的平均速率
v =___________。

(3)为使该反应的反应速率增大,且平衡向正反应方向移动的是__________。
a.及时分离除NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
Ⅱ、超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,其反应为:2NO+2CO![]() 2CO2+N2。为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
2CO2+N2。为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)(mol/L) | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
c(CO)(mol/L) | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)上述条件下反应能够自发进行,则该反应的△H_____0(填写“>”、“<”、“=”)。
(2)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是________。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
(3)某同学设计了三组实验,实验条件已经填在下面实验设计表中,分析表格我们可以看出该同学的实验目的主要是研究_______________和_____________________对化学反应速率的影响。
实验编号 | T(℃) | NO初始浓(mol/L) | CO初始浓度(mol/L) | 催化剂的比表面积(m2/g) |
Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
Ⅱ | 280 | 1.20×10-3 | 5.80×10-3 | 124 |
Ⅲ | 350 | 1.20×10-3 | 5.80×10-3 | 124 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废旧光盘金属层中的少量Ag,某科研小组采用如下方案进行回收(金属层中其他金属含量过低,对实验的影响可忽略)。
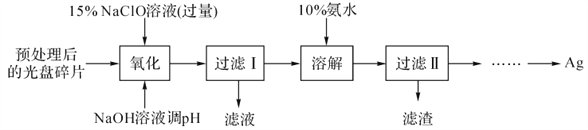
已知:①NaClO溶液在受热或酸性条件下易分解,如:3NaClO =2NaCl+NaClO3
②AgCl可溶于氨水:AgCl+2NH3·H2O =Ag(NH3)2++Cl-+2H2O
③常温时N2H4·H2O(水合肼)能还原Ag(NH3)2+:
4 Ag(NH3)2++N2H4·H2O=4Ag↓+N2↑+4NH4++4NH3↑+H2O
(1)“氧化”阶段需在80℃条件下进行,适宜的加热方式为___________。
(2)NaClO溶液与Ag反应的产物为AgCl、NaOH和O2,该反应的化学方程式为___________。HNO3也能氧化Ag,从反应产物的角度分析,以HNO3代替NaClO的缺点是________________。
(3)为提高Ag的回收率,需对“过滤Ⅱ”的滤渣进行洗涤,并________________。
(4)从“过滤Ⅱ”后的滤液中获取单质Ag的过程中,在加入2 mol/L水合肼溶液后,后续还需选用的试剂有________________(①1 mol/LH2SO4、②10%氨水、③1 mol/LNaOH溶液,填序号)。反应完全后获取纯净的单质银再进行的实验操作过程简述为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是工业上以有机物A、E为基本原料制备有机物M的一种合成路线.A能与Na2CO3溶液及溴水反应,且1molA最多可与2molBr2反应;B的苯环上有四种不同化学环境的氢原子;E、F均是芳香烃;M是一种具有特殊香气的物质。

已知: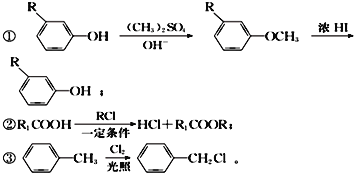
④酚羟基易被高锰酸钾酸性溶液、浓硝酸等氧化
回答下列问题:
(1)在F的同系物中,相对分子质量最小的物质是______(填名称);C中含氧官能团的名称为____________;
(2)A的结构简式为___________;E→F的反应类型为________;
(3)D+G→M的化学方程式为_____________________________;
(4)C的同分异构体中能同时满足下列条件的共有______种(不含立体异构);
①遇FeCl3溶液发生显色反应 ②能发生水解反应
其中核磁共振氢谱显示为5组峰,且峰面积比为2:2:2:1:1的是_____(写结构简式)。
(5)参照有机物M的上述合成路线,设计一条由![]() 和(CH3)3CCl为起始原料制备
和(CH3)3CCl为起始原料制备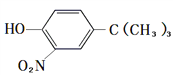 的合成路线:___________________________。
的合成路线:___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质或应用正确的是
A.实验室常用铝盐溶液与氢氧化钠溶液制备Al(OH)3沉淀
B.浓硫酸能干燥SO2、NO2等气体,说明浓硫酸具有吸水性
C.SO2具有漂白性,通入紫色石蕊溶液中能使溶液先变红后褪色
D.30%的H2O2溶液中加入MnO2可制得O2,MnO2做氧化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向0.1 mol·L-1NaOH溶液中通入过量的CO2后,溶液中存在的主要离子是下列的
A. Na+和CO32- B. Na+和HCO3- C. HCO3-和CO32- D. Na+和OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,几种弱酸的电离平衡常数如下表所示,下列说法正确的是
化学式 | HCOOH | H2CO3 | HCN |
电离平衡常数 | K=1.8×10-4 | K1=4.3×10-7 K2=5.6×10-11 | K=4.9×10-10 |
A. 酸性强弱顺序是HCOOH>HCN> H2CO3
B. HCOOH的电离平衡常数表达式为
C. Na2CO3溶液显碱性,NaHCO3溶液显酸性
D. H2CO3溶液和NaCN溶液反应的离子方程式为H2CO3+CN-=HCO3-+HCN
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题
(1)相同质量的CO和CO2的物质的量之比为 , 所含的电子个数之比为 , 在标准状况下的体积之比为 .
(2)19g某二价金属氯化物(ACl2)中含有0.4mol Cl﹣ , 则A的相对分子质量是
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“朴雪”乳酸亚铁口服液可以有效地治疗人类缺铁性贫血症,这是因为其中的 Fe2+进入人体后能
A. 调节血液的酸碱平衡
B. 调节血液的渗透压
C. 参与红细胞血红蛋白的形成
D. 促进更多红细胞的产生
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com