
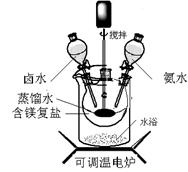
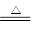 MgCO3·3H2O↓+ CO2↑+2NH3↑
MgCO3·3H2O↓+ CO2↑+2NH3↑  MgCO3·3H2O↓+ CO2↑+2NH3↑。
MgCO3·3H2O↓+ CO2↑+2NH3↑。

科目:高中化学 来源:不详 题型:填空题
 TiCl4
TiCl4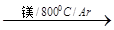 Ti
Ti 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.金属在自然界的存在形式 | B.金属熔点的高低 |
| C.金属离子得电子的能力 | D.金属元素在地壳中的含量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

| 物质 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe(OH)3 | 2.2 | 3.2 |
| Fe(OH)2 | 7.6 | 9.6 |
| Cu(OH)2 | 4.7 | 6.4 |
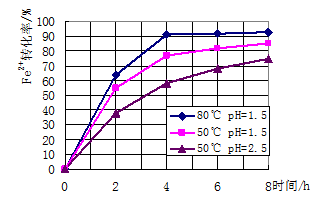
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.②③ | B.①③ | C.①②③ | D.②③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.改变金属内部组成结构,可以增强金属耐腐蚀的能力 | B.涂油漆 |
| C.外加电流阴极保护法 | D.在金属表面覆盖一层保护层 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 ,含
,含 、
、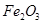 、MgO等杂质)中提取Al2O3的两种工艺品流程如下:
、MgO等杂质)中提取Al2O3的两种工艺品流程如下: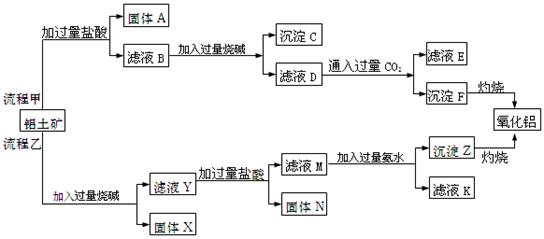
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 上由铝土矿(A12O3、Fe2O3)为原料制备无水AlCl3的工艺流程如下。
上由铝土矿(A12O3、Fe2O3)为原料制备无水AlCl3的工艺流程如下。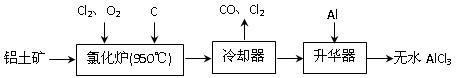
 的纯度,称取16.25 g无水AlCl3样品,溶于过量的NaOH溶液,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,残留固体质量为0.32 g。
的纯度,称取16.25 g无水AlCl3样品,溶于过量的NaOH溶液,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,残留固体质量为0.32 g。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com