
【题目】[化学——选修3:物质结构与性质]
已知A、B、C、D四种短周期元素,它们的核电荷数依次增大。A原子,C原子的L能层中,都有两个未成对的电子,C、D同主族。E、F都是第四周期元素,E原子核外有4个未成对电子,F原子除最外能层只有1个电子外,其余各能层均为全充满。根据以上信息填空:
(1)基态D原子中,电子占据的最高能层符号 ,该能层具有的原子轨道数为 ;
(2)E2+离子的价层电子轨道表示式是 ,F原子的电子排布式是 ;
(3)A元素的最高价氧化物对应的水化物中心原子采取的轨道杂化方式为 ,B元素的气态氢化物的分子模型为 ;
(4)化合物AC2、B2C和阴离子DAB-互为等电子体,它们结构相似,DAB-的电子式为 ;
(5)配合物甲的焰色反应呈紫色,其内界由中心离子E3+与配位体AB-构成,配位数为6,甲的水溶液可以用于实验室中E2+离子的定性检验,检验E2+离子的离子方程式为 ;
(6)某种化合物由D,E,F三种元素组成,其晶胞 如图所示,则其化学式为 ,该晶胞上下底面为正方形,侧面与底面垂直,根据图中所示的数据列式计算该晶体的密度:d= g/cm3。

【答案】(1)M;9;(2)![]() ;1s22s22p63s23p63d104s1;(3)sp2;四面体;(4)
;1s22s22p63s23p63d104s1;(3)sp2;四面体;(4)![]() (5)3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓;(6)CuFeS2;4.32
(5)3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓;(6)CuFeS2;4.32
【解析】
A、B、C、D都是周期表中的短周期元素,它们的核电荷数依次增大,A原子、C原子的L能层中都有两个未成对的电子,则A原子核外电子排布为1s22s22p2,C原子核外电子排布为1s22s22p4,故A为碳元素、C为氧元素;B原子序数介于C、O之间,则B为氮元素;C、D同主族,则D为S元素;E、F都是第四周期元素,E原子核外有4个未成对电子,原子核外电子排布为1s22s22p63s23p63d64s2,则E为Fe;F原子除最外能层只有1个电子外,其余各能层均为全充满,F原子核外电子数=2+8+18+1=29,则F为Cu元素,据以上分析回答题中的问题。
(1)基态S原子中电子占据的最高能层为第3能层,符号M,该能层有1个s轨道、3个p轨道、5个d轨道,共有9个原子轨道;
(2)Fe2+离子的价层电子排布3d6,其价层电子排布图是![]() ,F为Cu元素,原子核外有29个电子,原子的电子排布式是1s22s22p63s23p63d104s1;
,F为Cu元素,原子核外有29个电子,原子的电子排布式是1s22s22p63s23p63d104s1;
(3)碳元素的最高价氧化物对应的水化物为H2CO3,中心C原子成3个σ键、没有孤电子对,C原子 采取sp2杂化方式;B的气态氢化物为NH3,NH3分子中N原子价层电子对数=3+![]() =4,其VSEPR模型为四面体;
=4,其VSEPR模型为四面体;
(4)与CO2互为等电子体,可知SCN-电子式与CO2相同,参照CO2的电子式写出电子式为:![]() ;
;
(5)配合物甲的焰色反应呈紫色,为K元素,其内界由中心离子Fe3+与配位体CN-构成,配位数为6,甲为K3[Fe(CN)6],甲的水溶液可以用于实验室中Fe2+离子的定性检验,检验Fe2+离子的离子方程式为:3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓;
(6)晶胞中D(S)原子位于晶胞内部,原子数目为8个,E(Fe)原子6个位于面上、4个位于棱上,E(Fe)原子数目=6×![]() +4×
+4×![]() =4,F(Cu)原子位于4个位于面上、1个内部、8个顶点上,原子数目=4×
=4,F(Cu)原子位于4个位于面上、1个内部、8个顶点上,原子数目=4×![]() +1+8×
+1+8×![]() =4,晶体中Cu、Fe、S原子数目之比=4:4:8=1:1:2,故该晶体化学式为:CuFeS2;
=4,晶体中Cu、Fe、S原子数目之比=4:4:8=1:1:2,故该晶体化学式为:CuFeS2;
晶胞质量=![]() g,晶胞体积=(524×10-10 cm)2×103×10-10cm,该晶胞的密度d=
g,晶胞体积=(524×10-10 cm)2×103×10-10cm,该晶胞的密度d= ![]() =[
=[![]() ]÷[(524×10-10 cm)2×1030×10-10 cm]= 4.32g/cm3;
]÷[(524×10-10 cm)2×1030×10-10 cm]= 4.32g/cm3;
故答案为:CuFeS2;4.32。


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:
【题目】某工程师为了从腐蚀废液(含有Cu2+、Fe2+、Fe3+)中回收铜,并重新获得FeCl3溶液,准备采用下列步骤:

(1)请写出上述实验中加入或生成的有关物质的化学式。
①=__________,② __________,③__________,④__________,⑤__________,⑥__________。
(2)请写出相关反应的化学方程式:______,_____________,__________,_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以钒钛磁铁矿为原料,在炼铁的同时还可以制备钒的最高价氧化物V2O5,其主要流程如图:

已知:①![]() +2H+
+2H+![]()
![]() +H2O ②NH4VO3微溶于冷水,易溶于热水,不溶于乙醇
+H2O ②NH4VO3微溶于冷水,易溶于热水,不溶于乙醇
(l)浸取过程中提高浸取率的方法______(任写一种)
(2)钒渣中的V2O3与CaCO3混合后在空气中焙烧时转化为Ca(VO3)2同时释放出一种温室气体,写出该反应的化学方程式_____。
(3)Ca(VO3)2难溶于水但能溶于稀硫酸,试用平衡移动原理分析其原因_____,浸出液中含钒物质的化学式为_________。
(4)过滤后用乙醇代替水来洗涤沉淀的原因是______。
(5)“沉钒”得到偏钒酸铵(NH4VO3),若浸出液中c(![]() )=0.1molL-1,为使钒元素的沉降率达到98%,至少应调节c(
)=0.1molL-1,为使钒元素的沉降率达到98%,至少应调节c(![]() )为_____molL-1[已知Ksp(NH4VO3)=1.6×10-3]
)为_____molL-1[已知Ksp(NH4VO3)=1.6×10-3]
(6)煅烧NH4VO3时,固体质量随温度变化的曲线如图所示。加热到200℃时,得到的固体物质化学式为_____。
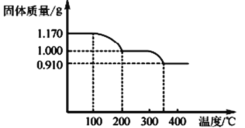
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备硝基苯的实验装置如图所示(夹持装置已略去)。下列说法不正确的是( )

A.水浴加热的优点为使反应物受热均匀、容易控制温度
B.仪器a的作用是冷凝回流,提高原料的利用率
C.浓硫酸、浓硝酸和苯混合时,应先向浓硫酸中缓缓加入浓硝酸,待冷却至室温后,再将所得混合物加入苯中
D.反应完全后,可用蒸馏的方法分离苯和硝基苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Zn、Fe及其化合物在生产生活中应用比较广泛。工业上利用锌焙砂(主要含ZnO、ZnFe2O4,还含有少量FeO和CuO等杂质)制取金属锌的工艺流程如下:

(1)为了提高酸浸效率,可采用的措施有___________________________________(任答两条);
写出ZnFe2O4溶于酸的离子方程式____________________________________
(2)向净化Ⅰ操作中加入ZnO的目的___________________________________
(3)若净化后的溶液中Cu2+浓度为1×10-12mol/L,则净化后溶液中Zn2+浓度为__________(已知:室温下Ksp(ZnS)=1.6×10-24, Ksp(CuS)=6.4×10-36)
(4)“电解”工艺制锌时Zn2+利用率较低,废液中有大 量的Zn2+ 残留。某化工厂拟采用改变酸锌比净化废液的方式来提高原料的利用率,降低成本。如图是工业生产中不同酸锌比时净化液利用率对电解时直流电耗能影响关系图。根据图分析,该工厂净化废液时的最佳酸锌比为______。

A. 5:1 B.6:1 C.7:1 D.10:1
(5)ZnFe2O4是一种性能优良的软磁材料,工业上常利用ZnFe2(C2O4)3·6H2O隔绝空气加热分解制备,该晶体的热分解化学方程式为_______________________________________。测热分解后产品中ZnFe2O4的质量分数方法如下:取a克产品用H2SO4溶解后加入足量KI溶液充分反应,调溶液至弱酸性,再加入淀粉指示剂,用c mol/L Na2S2O3标准溶液滴定,用去此标准溶液v mL时,刚好到达滴定终点,则此产品中ZnFe2O4的质量分数为____________(用a、c、v表示)。(已知:I2+2S2O32-=2I-+S4O62-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,某反应达到了化学平衡,其反应过程对应的能量变化如图。
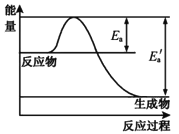
下列说法正确的是( )
A.Ea为逆反应活化能,Ea′为正反应活化能
B.温度升高,逆反应速率加快幅度大于正反应加快幅度,使平衡逆移
C.所有活化分子的平均能量高于或等于所有分子的平均能量
D.该反应为放热反应,ΔH=Ea′-Ea
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物M是有机合成的重要中间体,制备M的一种合成路线如图(部分反应条件和试剂略去):
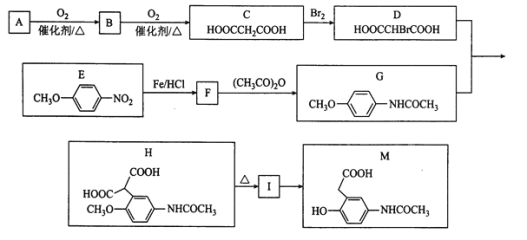
已知:①A的密度是相同条件下H2密度的38倍;其分子的核磁共振氢谱中有3组峰;
②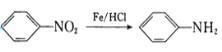 (-NH2容易被氧化);
(-NH2容易被氧化);
③ R-CH2COOH
R-CH2COOH
请回答下列问题:
(1)B的化学名称为___;D中官能团的名称为___。
(2)C→D的反应类型是___,I的结构简式为___。
(3)F→G的化学方程式为___。
(4)M不可能发生的反应为___(填选项字母)。
a.加成反应 b.氧化反应 c.取代反应 d.消去反应
(5)请写出任意两种满足下列条件的E的同分异构体有___。
①能与FeCl3溶液发生显色反应②能与NaHCO3反应③含有—NH2
(6)参照上述合成路线,以![]() 为原料(无机试剂任选),设计制备
为原料(无机试剂任选),设计制备![]() 的合成路线:___。
的合成路线:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】探究Na2O2与水的反应,实验如图:
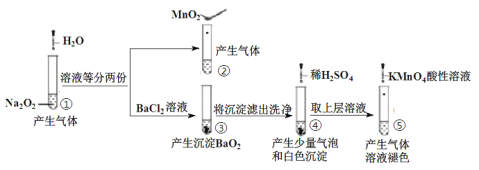
已知:H2O2H++![]() ;
;![]() H++
H++![]() 。下列分析不正确的是
。下列分析不正确的是
A.①、④实验中均发生了氧化还原反应和复分解反应
B.①、⑤中产生的气体能使带火星的木条复燃,说明存在H2O2
C.③和④不能说明溶解性:BaO2> BaSO4
D.⑤中说明H2O2具有还原性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com