
| n |
| V |
| m |
| M |
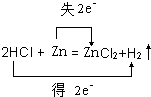 ,
, ,HCl是氧化剂,ZnCl2是氧化产物;
,HCl是氧化剂,ZnCl2是氧化产物;| 0.2mol |
| 0.2L |
| 6.5g |
| 65g/mol |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、c(NH4+)相等的(NH4)2SO4、(NH4)2Fe(SO4)2和NH4Cl溶液中,溶质浓度大小关系是:c[(NH4)2Fe(SO4)2]<c[(NH4)2SO4]<c(NH4Cl) |
| B、pH相同的盐酸和醋酸稀释相同倍数后,盐酸的pH小于醋酸的pH |
| C、中和体积与pH都相同的盐酸和醋酸所消耗的NaOH物质的量相同 |
| D、CH3COONa溶液中:c(Na+)=c(CH3COO-)+c(OH-)-c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、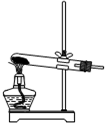 在如图所示装置中制氨气 |
| B、利用铝热反应焊接铁轨 |
| C、通过合成氨实现人工固氮 |
| D、过氧化钠用作呼吸面具的供氧剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、P既是氯化剂又是还原剂 |
| B、Cu3P既是氧化产物又是还原产物 |
| C、CuSO4发生了还原反应 |
| D、当生成lmol Cu3P时,转移电子的物质的量为6 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、溶液中c(Na+)=2c(SO42-) | ||
B、沉淀的物质的量等于
| ||
| C、标况下,生成SO2的体积<11.2aL | ||
D、原浓硫酸中H2SO4的物质的量>
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、a>b>c>d |
| B、b>a>d>c |
| C、c>d>b>a |
| D、d>c>a>b |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、PH<7的雨水称为酸雨 |
| B、二氧化硫的大量排放是造成光化学烟雾的主要原因 |
| C、PM2.5是指大气中直径小于或等于2.5微米的颗粒物,与肺癌等疾病的发生相关 |
| D、SO2、CO2、NO2均属于大气污染物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com