
【题目】有关晶体的结构如图所示,下列说法中不正确的是
A.  在NaCl晶体中,距Na+最近的Cl-形成正八面体
在NaCl晶体中,距Na+最近的Cl-形成正八面体
B.  在CaF2晶体中,每个晶胞平均占有4个Ca2+
在CaF2晶体中,每个晶胞平均占有4个Ca2+
C.  在金刚石晶体中,碳原子与碳碳键数目比为1∶2
在金刚石晶体中,碳原子与碳碳键数目比为1∶2
D.  由E原子和F原子构成的气态团簇分子的分子式为EF或FE
由E原子和F原子构成的气态团簇分子的分子式为EF或FE
【答案】D
【解析】
A、在NaCl晶体中,每个Na+周围距离最近的Cl是6个(上、下、左、右、前、后各1个),构成正八面体;
B、根据“均摊法”,1个CaF2晶胞中含有的Ca2+数为8×![]() 1/8+6×
1/8+6×![]() 1/2=4;
1/2=4;
C、金刚石晶体中,每个碳原子以4个碳碳键与相邻的4个碳原子结合,每个碳碳键为2个碳原子所共用,故碳原子与碳碳键数之比为1∶2;
D、气态团簇分子的分子式应为E4F4或F4E4,不能写成实验式。
A、在NaCl晶体中,每个Na+周围距离最近的Cl是6个(上、下、左、右、前、后各1个),构成正八面体,故A正确;
B、根据“均摊法”,1个CaF2晶胞中含有的Ca2+数为8×![]() 1/8+6×
1/8+6×![]() 1/2=4,故B正确;
1/2=4,故B正确;
C、金刚石晶体中,每个碳原子以4个碳碳键与相邻的4个碳原子结合,每个碳碳键为2个碳原子所共用,故碳原子与碳碳键数之比为1∶2,故C正确;
D、由E原子和F原子构成的气态团簇分子的分子式应为E4F4或F4E4,故D错误。
故选D。


科目:高中化学 来源: 题型:
【题目】已知(b)![]() 、(d)
、(d)![]() 、(p)
、(p)![]() 的分子式均为C6H6,下列说法正确的是
的分子式均为C6H6,下列说法正确的是
A. b的同分异构体只有d和p两种B. b、d、p的二氯代物均只有三种
C. b、d、p均可与酸性高锰酸钾溶液反应D. b、d、p中只有b的所有原子处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解物质的量浓度相同、体积比为2∶3的CuSO4和NaCl的混合溶液,可能发生的反应有( )
①2Cu2++2H2O![]() 2Cu+4H++O2↑
2Cu+4H++O2↑
②Cu2++2Cl-![]() Cu+Cl2↑
Cu+Cl2↑
③2Cl-+2H+![]() H2↑+Cl2↑
H2↑+Cl2↑
④2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
A.①②③B.①②④C.②③④D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家研制出一种催化剂,能在室温下高效催化空气中甲醛的氧化,其反应为HCHO+O2![]() CO2+H2O。下列有关说法正确的是( )
CO2+H2O。下列有关说法正确的是( )
A.反应物和生成物都是非极性分子
B.0.5 mol HCHO含有1 mol σ键
C.HCHO、CO2分子中中心原子杂化类型相同
D.HCHO能溶解在H2O中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用太阳能光解水,制备的H2用于还原CO2合成有机物,可实现资源的再利用。回答下列问题:
Ⅰ.半导体光催化剂浸入水或电解质溶液中,光照时可在其表面得到产物
(1)下图为该催化剂在水中发生光催化反应的原理示意图。光解水能量转化形式为___________。
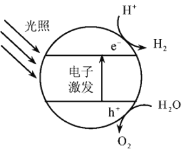
(2)若将该催化剂置于Na2SO3溶液中,产物之一为![]() ,另一产物为__________。若将该催化剂置于AgNO3溶液中,产物之一为O2,写出生成另一产物的离子反应式__________。
,另一产物为__________。若将该催化剂置于AgNO3溶液中,产物之一为O2,写出生成另一产物的离子反应式__________。
Ⅱ.用H2还原CO2可以在一定条下合成CH3OH(不考虑副反应):![]()
(3)某温度下,恒容密闭容器中,CO2和H2的起始浓度分别为 a molL-1和3 a molL-1,反应平衡时,CH3OH的产率为b,该温度下反应平衡常数的值为___________。
(4)恒压下,CO2和H2的起始物质的量比为1:3时,该反应在无分子筛膜时甲醇的平衡产率和有分子筛膜时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出H2O。
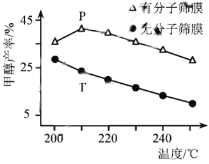
①甲醇平衡产率随温度升高而降低的原因为____________。
②P点甲醇产率高于T点的原因为___________。
③根据上图,在此条件下采用该分子筛膜时的最佳反应温度为___________°C。
Ⅲ.调节溶液pH可实现工业废气CO2的捕获和释放
(5) ![]() 的空间构型为__________。已知25℃碳酸电离常数为Ka1、Ka2,当溶液pH=12时,
的空间构型为__________。已知25℃碳酸电离常数为Ka1、Ka2,当溶液pH=12时,![]() =1:_______:__________。
=1:_______:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示分别为氯化钠、氯化铯、氟化钙的晶胞模型,请认真观察后完成表格。___________

离子晶体 | 晶体结构粒子 | 晶胞所含粒子数 | 配位数 | 阴阳离子个数之比 | ||
阴离子 | 阳离子 | 阴离子 | 阳离子 | |||
氯化钠 | ||||||
氯化铯 | ||||||
氟化钙 | ||||||
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由以下粒子结构示意图得出的结论正确的是( )

A.④表示的是阳离子
B.①③属于同种元素,②④属于同种元素
C.②④形成的化合物是Al2O3
D.①③的化学性质相似
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一白色粉末X,对X检验时,所做实验和现象为:

(1)写出X的化学式___。
(2)在①步反应中H2SO4的作用是___。
①在水溶液中电离,并呈强酸性 ②具有高沸点、难挥发性 ③浓硫酸具有吸水性 ④浓硫酸具有脱水性 ⑤浓硫酸具有强氧化性
(3)写出④、⑤两步反应的离子方程式:___、___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(![]() )是一种新型、高效、多功能水处理剂,且不会造成二次污染。
)是一种新型、高效、多功能水处理剂,且不会造成二次污染。
查阅资料:
①![]() 为紫色固体,微溶于
为紫色固体,微溶于![]() 溶液,具有强氧化性,在酸性或中性溶液中快速产生
溶液,具有强氧化性,在酸性或中性溶液中快速产生![]() ,在碱性溶液中较稳定。
,在碱性溶液中较稳定。
②![]() 与
与![]() 溶液在20℃以下反应生成
溶液在20℃以下反应生成![]() ,在较高温度下则生成
,在较高温度下则生成![]() 。
。
(1)实验室常利用氯气制备![]() 后与
后与![]() 、
、![]() 反应制备
反应制备![]() 。根据下列仪器,请你组装合理、简洁的实验装置,所用装置的接口连接顺序是________。
。根据下列仪器,请你组装合理、简洁的实验装置,所用装置的接口连接顺序是________。



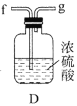


(2)写出装置A中发生反应的离子方程式________。
(3)三颈烧瓶用冰水浴的原因是________,A处盛放![]() 的仪器名称是________。
的仪器名称是________。
(4)将实验得到的![]() 再加入饱和
再加入饱和![]() 溶液中,可析出紫黑色的
溶液中,可析出紫黑色的![]() 粗晶体,其原因是________。
粗晶体,其原因是________。
(5)用滴定法测定所制粗![]() 的纯度(杂质与
的纯度(杂质与![]() 不反应):取
不反应):取![]() 粗
粗![]() 样品,加入足量硫酸酸化的
样品,加入足量硫酸酸化的![]() 溶液,充分反应后,用
溶液,充分反应后,用![]() 标准溶液滴定生成的I2,滴定消耗标准溶液的体积为
标准溶液滴定生成的I2,滴定消耗标准溶液的体积为![]() 。涉及的反应有:
。涉及的反应有:![]() ,
,![]() 。
。
①滴定时选用的指示剂是________,滴定终点的现象是________。
②制得粗![]() 的纯度是________。
的纯度是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com