
【题目】在配制 100 mL 1.0 mol·L-1 的 NaCl 溶液时,下列操作会导致结果偏低的是
(1)用托盘天平称量时砝码放在左盘,1g 以下使用游码
(2)溶解 NaCl 固体的烧杯上挂着水珠,直接使用
(3)将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外
(4)定容时俯视刻度线
(5)定容时仰视刻度线
(6)容量瓶未经干燥就用于配制溶液
A. (1)(3)(5) B. (1)(3)(4)
C. (2)(4)(6) D. (2)(3)(4)
【答案】A
【解析】
(1) 100 mL 1.0 mol·L-1的 NaCl溶液中所含NaCl的质量=0.1L×1.0mol/L×58.5g/mol=5.85g≈5.9g,用托盘天平称量时砝码放在左盘,此时称得的NaCl的质量只有5g-0.9g=4.1g,根据浓度公式c=![]() 可知,n减小,所以所配NaCl溶液的浓度偏低,(1)项正确;
可知,n减小,所以所配NaCl溶液的浓度偏低,(1)项正确;
(2)溶解 NaCl 固体的烧杯上挂着水珠,不影响NaCl的物质的量(n)和容量瓶中溶液体积(V),由公式c=![]() 可知,对NaCl溶液的浓度无影响,(2)项错误;
可知,对NaCl溶液的浓度无影响,(2)项错误;
(3)将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外,使NaCl物质的量(n)减小,根据公式c=![]() 可知,NaCl溶液的浓度将减小,(3)项正确;
可知,NaCl溶液的浓度将减小,(3)项正确;
(4)定容时俯视刻度线,使容量瓶中溶液体积(V)减小,根据公式c=![]() 可知,NaCl的浓度将增大,(4)项错误;
可知,NaCl的浓度将增大,(4)项错误;
(5)定容时仰视刻度线,使容量瓶中溶液体积(V)增大,根据公式c=![]() 可知,NaCl的浓度将减小,(5)项正确;
可知,NaCl的浓度将减小,(5)项正确;
(6)容量瓶未经干燥就用于配制溶液,NaCl的物质的量(n)和溶液体积(V)不受影响,根据公式c=![]() 可知,不影响NaCl的浓度,(6)项错误;答案选A。
可知,不影响NaCl的浓度,(6)项错误;答案选A。


 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )。
A.酯化反应也属于加成反应
B.酯化反应中羧酸脱去羧基中的羟基,醇脱去羟基中的氢原子生成水
C.浓硫酸在酯化反应中只起催化剂的作用
D.欲使酯化反应生成的酯分离并提纯,可以将酯蒸气通过导管伸入饱和碳酸钠溶液的液面下,再用分液漏斗分离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业废料和废水的处理离不开化学。
I. 某工业废料含SiO2、FeS和CuS等物质,采用如下实验方案进行回收利用。请回答下列问题:
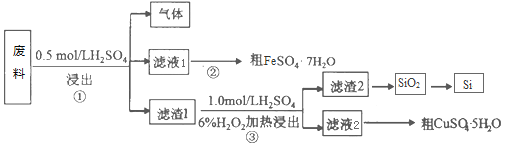
(1)已知步骤①中发生的化学反应为非氧化还原反应,写出产生气体的电子式_______,该气体可用足量的NaOH溶液吸收,该反应的离子方程式是_______________________________
(2)Si原子在周期表中的位置____________,写出晶体Si的一种主要用途___________。步骤②的操作依次为____________________、过滤、洗涤、干燥。滤渣2的主要成分是SiO2和S,写出步骤③涉及的化学方程式_________________________________。
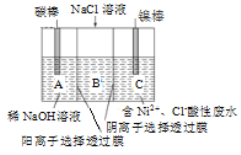
II.用一种阴、阳离子双隔膜三室电解槽处理含镍酸性废水并获得金属镍的模拟装置如图。
镍棒与外接电源____极相连。A极区电极反应式是__________________________。 电解一段时间后,B中NaCl溶液的浓度_________填“增大”、“减少”);若将图中阳离子膜去掉,将A、B两室合并,则A极区电极产物是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从元素化合价变化的角度分析,下列反应中,画线的物质发生氧化反应的是
A. SO2 + 2NaOH = Na2SO3 + H2O B. 2CuO + C![]() 2Cu + CO2↑
2Cu + CO2↑
C. 2FeCl3 + Fe = 3FeCl2 D. Zn+2HCl = ZnCl2+ H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石墨烯锂硫电池放电时的工作原理示意图如图,电池反应为:2Li + nS=Li2Sn,有关该电池说法正确的是( )
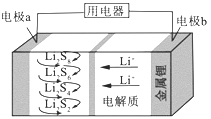
A. 放电时,Li+ 向负极迁移
B. 电池工作时,正极可发生反应:2Li2S6+2Li++2e-=3Li2S4
C. 当外电路有2mol电子通过时,有1mol Li+通过阳离子交换膜
D. 该电池可以选用盐酸作为电解质增强溶液导电性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PbO(溶于酸,微溶于强碱溶液)在工业上用途广泛,可制作颜料铅白、杀虫剂等。某再生能源企业以含铅废料(主要含Pb、PbO、PbSO4和极少量的PbO2)和稀H2SO4为原料制备高纯PbO的工艺流程如下:

(1)含铅废料中的PbO2和PbSO4中,铅的化合价分别为____________、____________。
(2)酸溶过程中为了加快溶解速率,除了加入FeSO4作催化剂外,还可采取的措施有____________________(任写一种)。
(3)滤液A中含有的主要阳离子是____________________(填离子符号)。
(4)脱硫过程发生的主要反应的离子方程式为________________________________。
(5)冷却、过滤后对所得的固体进行洗涤操作,在实验室洗涤时,所用到的玻璃仪器有烧杯、_________和_________,检验沉淀是否洗涤干净的方法是________________________________。
(6)PbO溶解在NaOH溶液中,存在平衡:PbO(s)+NaOH(aq)![]() NaHPbO2(aq)。PbO的溶解度曲线如图所示。结合该曲线,简述由粗品PbO得到高纯PbO的操作:_______________________________。
NaHPbO2(aq)。PbO的溶解度曲线如图所示。结合该曲线,简述由粗品PbO得到高纯PbO的操作:_______________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.分子晶体中一定存在分子间作用力和共价键
B.HF比HCl沸点高是因为HF分子间存在氢键
C.全部由非金属元素形成的化合物中可能含有离子键
D.溶于水能导电的化合物一定是离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝(AlN,Al和N的相对原子质量分别为27和14)广泛应用于电子、陶瓷等工业领域。在一定条件下,AlN可通过反应Al2O3+N2+3C![]() 2AlN+3CO合成。下列叙述不正确的是
2AlN+3CO合成。下列叙述不正确的是
A. 上述反应中, C是还原剂,AlN是还原产物
B. 上述反应中,每生成1 mol AlN需转移3 mol电子
C. AlN中氮元素的化合价为-3
D. AlN的摩尔质量为41
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分枝酸可用于生化研究.其结构简式如图.下列关于分枝酸的叙述正确的是
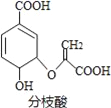
A. 分子中含有2种官能团
B. 可与乙醇、乙酸反应,且反应类型相同
C. 1mol分枝酸最多可与3molNaOH发生中和反应
D. 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com