
�����й��Ȼ�ѧ����ʽ�ı�ʾ��˵����ȷ����(����)
A����֪2H2(g)+O2(g)��2H2O(g)�� ��H=��483.6kJ/mol����������ȼ����Ϊ241.8kJ/mol
B����֪C(ʯī��s)��C(���ʯ��s) ��H>0������ʯ��ʯī�ȶ�
C����20.0g NaOH��ϡ��Һ��ϡ������ȫ�кͣ��ų�28.7kJ�����������ʾ�÷�Ӧ�к��ȵ��Ȼ�ѧ����ʽΪ��NaOH(aq)+1/2H2SO4 (aq)��NaCl(aq)+H2O(l) ��H=��57.4kJ/mol
D����֪I2(g)+ H2(g)��2HI(g) ��H1����I2(s)+ H2(g)��2HI(g )�� ��H2�����H1>��H2
C
��������
�����������A������ˮ���ȶ�״̬��Һ̬������������ȼ���ȴ���241.8kJ/mol������B����֪C(ʯī��s)��C(���ʯ��s) ��H>0�����������е�����Խ�ͣ����ʵ��ȶ��Ծ�Խǿ����ʯī�Ƚ��ʯ�ȶ�������C����20.0g NaOH�����ʵ�����0.5mol,��ȫ�кͷų�������28.7kJ����1.0mol��NaOH��ȫ�кͲ���1mol��ˮ�ų�������57.4kJ���ʱ�ʾ�÷�Ӧ�к��ȵ��Ȼ�ѧ����ʽΪ��NaOH(aq)+1/2H2SO4 (aq)��NaCl(aq)+H2O(l) ��H=��57.4kJ/mol����ȷ��D,ͬ����������������̬ʱ�����е������ȹ�̬ʱ�࣬����ǰ�߷�Ӧ�ų����������ں��ߣ���ˡ�H1<��H2,����
���㣺�����й��Ȼ�ѧ����ʽ�ı�ʾ��˵����֪ʶ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2013��2014ѧ�긣��ʡ��һѧ�ڸ����ڶ����¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���б仯��˷���ͬ��������������
A�����C60���ۻ� B����ɱ�������
C���Ȼ�����Ȼ��ص��ܽ� D�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016������ʡ��ɽ�и�һ��ѧ����ĩ���Ի�ѧ��A�����Ծ��������棩 ���ͣ�ѡ����
���ֶ�����Ԫ�������ڱ��е�λ����ͼ��ʾ������ֻ��CΪ����Ԫ�ء�����˵���������
|
| A | B |
C | D |
|
|
|
|
|
|
|
| A | B |
C | D |
|
|
A��ԭ�Ӱ뾶B��C
B��A������������Ӧˮ��������Ա�D��
C��D�������̬�⻯������ȶ��Ա�B��С
D��Bλ��Ԫ�����ڱ��еڶ����ڡ���VIA��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016������ʡ��˳����У�������һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪��HCN(aq)��NaOH(aq)��Ӧ��?H=-12.1kJ/mol��HCl(aq)��NaOH(aq)��Ӧ��?H=-55.6kJ/mol����HCN��ˮ��Һ�е����?H����( )
A��-67.7 kJ/mol B��-43.5 kJ/mol C��+43.5 kJ/mol D��+67.7kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016������ʡ��˳����У�������һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���淴Ӧ��2SO2��O2 2SO3�ﵽƽ��״̬ʱ�����ֺ��º����������м���һ������O2������˵����ȷ����(KΪƽ�ⳣ����QcΪŨ����)(����)
2SO3�ﵽƽ��״̬ʱ�����ֺ��º����������м���һ������O2������˵����ȷ����(KΪƽ�ⳣ����QcΪŨ����)(����)
A��Qc���䣬K���O2ת�������� B��Qc���䣬K���SO2ת���ʼ�С
C��Qc��С��K���䣬O2ת���ʼ�С D��Qc����K���䣬SO2ת��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016������ʡ��˳����У�������һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪X��Y��Z��W���ֶ���������Ԫ�������ڱ��е����λ����ͼ��ʾ������˵����ȷ����
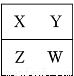
A��W��ԭ������������Y��ԭ��������2��
B�� X����Ϊ��Ԫ��
C��W����̬�⻯����ȶ���һ����Y��ǿ
D��X��Y��Z��W����Ԫ�ص�����������֮�Ϳ���Ϊ25
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�츣��ʡ���ݰ��и�һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
19.2gͭ��������ŨHNO3��Ӧ��ͭȫ����Ӧ���ռ���11.2 LNO��NO2�������(��״��)����Ӧ����HNO3�����ʵ����ǣ� ��
A��0.8 mol B��1.1 mol C��1.2 mol D��2.0 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�츣��ʡ���ݰ��и�һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����Ṥҵ�����У�Ϊ��������SO2��ת�������ܳ���������ܣ��������м����Ƚ������Ӵ��ң���ͼ���������ܱ���ϵ���������������A������������Ϊ( )
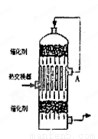
A��SO2 B��SO3��O2 C��SO2��SO3 D��SO2��O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�캣��ʡ�ڶ�ѧ�ڸ�һ��ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��һ�������µ��ܱ������У�һ����˵����ӦA(g)+3B(g) 2C(g)+2D(g)�ﵽƽ��״̬����
2C(g)+2D(g)�ﵽƽ��״̬����
A����Ӧ��ϵ����ѹ�㶨 B��B��Ũ�Ȳ���
C��C(A):C(B)=1 : 3 D��2V(B)�� = 3V(C)��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com