
在一定条件下的密闭容器中,一定能说明反应A(g)+3B(g) 2C(g)+2D(g)达到平衡状态的是
2C(g)+2D(g)达到平衡状态的是
A.反应体系的总压恒定 B.B的浓度不变
C.C(A):C(B)=1 : 3 D.2V(B)正 = 3V(C)逆
BD
【解析】
试题分析:A.该反应是反应前后气体体积相等的反应,所以无论反应是否达到平衡,体系的总压恒定不变,因此不能判断反应达到平衡状态,错误;B.若反应达到平衡状态,各种物质的物质的量浓度不变,B的浓度不变,则反应达到平衡,正确;C.A、B发生反应是按照1:3关系进行的,若开始加入物质是按照1:3加入,则在任何时刻都存在C(A):C(B)=1 : 3,因此不能作为判断反应达到平衡的标志,错误;D.在任何时刻都存在:2V(B)正 = 3V(C)正;而2V(B)正 = 3V(C)逆,则V(C)正=V(C)逆,化学反应达到平衡状态,正确。
考点:考查可逆反应达到平衡状态的判断的知识。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2016届辽宁省抚顺市六校联合体高一下学期期末考试化学试卷(解析版) 题型:选择题
下列有关热化学方程式的表示及说法正确的是( )
A.已知2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ/mol,则氢气的燃烧热为241.8kJ/mol
B.已知C(石墨,s)=C(金刚石,s) △H>0,则金刚石比石墨稳定
C.含20.0g NaOH的稀溶液与稀硫酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式为:NaOH(aq)+1/2H2SO4 (aq)=NaCl(aq)+H2O(l) △H=-57.4kJ/mol
D.已知I2(g)+ H2(g)=2HI(g) △H1, I2(s)+ H2(g)=2HI(g ) △H2 则△H1>△H2
查看答案和解析>>
科目:高中化学 来源:2016届湖北省孝感市七校联考高一下学期期中考试化学试卷(解析版) 题型:填空题
I.用元素符号回答原子序数11-18的元素的有关问题:(填对应物质的化学式)
(1)最高价氧化物的水化物碱性最强的是 ;其电子式为:
(2)最高价氧化物的水化物呈两性的是 ;
(3)能形成气态氢化物且最稳定的是 ,其电子式为 .
II.化学是一门以实验为基础的自然科学,根据已有实验知识回答下列问题。
下列说法错误的是 。
A.将Cl2通入紫色石蕊试液,溶液先变红后褪色
B.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
C.配制1L0.5mol·L-1的NaCl溶液,需用托盘天秤称量29.25gNaCl固体
D.常温下,可以用铁质容器储运浓硝酸
E.实验室可以用加热氯化铵的方法制取少量氨气
F.实验室保存硫酸亚铁溶液,需在试剂瓶内加入铁粉或铁钉,防止硫酸亚铁被氧化
G.除去KCl溶液中少量MgCl2:加入适量NaOH溶液,过滤
查看答案和解析>>
科目:高中化学 来源:2016届海南省第二学期高一期末考试化学试卷(解析版) 题型:填空题
(12分)
(1)分别取1 mol葡萄糖进行下列实验:
①若使之完全转化为CO2和H2O,所需氧气的体积在标准状况下为_____________L,反 应的化学方程式为_____________________________________________________。
②与乙酸反应生成酯,从理论上讲完全酯化需要______ g 乙酸。
(2)将蔗糖溶于水,配成10%的溶液,分装在两个试管中,在第一支试管中加入新制Cu(OH)2悬浊液后加热没有变化,原因是蔗糖分子中___________;在第二支试管中 加入几滴稀H2SO4,再在水浴中加热,加NaOH中和酸后也加入新制Cu(OH)2悬浊液后加热,现象是 _________________,原因是____________。
查看答案和解析>>
科目:高中化学 来源:2016届海南省第二学期高一期末考试化学试卷(解析版) 题型:选择题
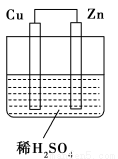
3.如图所示是Zn和Cu形成的原电池,其实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是( )
A.①②③ B.②④ C.④⑤⑥ D.③④⑤

查看答案和解析>>
科目:高中化学 来源:2016届海南省第二学期高一期末考试化学试卷(解析版) 题型:选择题
下列装置或操作能达到实验目的的是
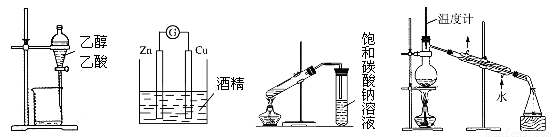
A.除去乙醇中的乙酸 B.形成原电池 C.制取乙酸乙酯 D.石油的蒸馏
查看答案和解析>>
科目:高中化学 来源:2016届浙江省温州市十校联合体高一下学期期中联考化学试卷(解析版) 题型:选择题
如图所示的两个实验装置中,溶液的体积均为200 mL,开始时电解质溶液的浓度均为0.1 mol/L,工作一段时间后,测得导线上均通过0.02 mol电子,若不考虑溶液体积的变化,则下列叙述中正确的是

A.产生气体的体积:(1)> (2)
B.电极上析出物质的质量:(1)> (2)
C.溶液pH的变化:(1)增大,(2)减小
D.电极反应式:(1)中阳极:4OH--4e-===2H2O+O2↑,(2)中负极:2H++2e-===H2↑
查看答案和解析>>
科目:高中化学 来源:2016届浙江省温州市十校联合体高一下学期期中联考化学试卷(解析版) 题型:选择题
已知汽车尾气无害化处理反应为2NO(g)+2CO(g) N2(g)+2CO2(g),下列说法中正确的是
N2(g)+2CO2(g),下列说法中正确的是
A.使用适当的催化剂不改变反应速率 B.降低压强能提高反应速率
C.升高温度能提高反应速率 D.改变压强对反应速率无影响
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高一下学期期中考化学试卷(解析版) 题型:选择题
根据热化学方程式:S(g)+O2(g) SO2(g) △H=-QkJ·mol-1(Q>0),下列分析正确的是( )
SO2(g) △H=-QkJ·mol-1(Q>0),下列分析正确的是( )
A.1 mol S(g)与1 mol O2(g)反应生成1 mol SO2(g)放出QkJ的热量
B.1个S(g)与1个O2(g)完全反应要放出Q kJ的热量
C.S(s)+O2(g) SO2(g) △H<-Q kJ·mol-1
SO2(g) △H<-Q kJ·mol-1
D.1 mol S(g)与1 mol O2(g)的总能量比1 mol SO2(g)的总能量低QkJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com