
下列反应的离子方程式书写正确的是( )。
A.铝片放入氢氧化钠溶液中:Al+2OH-=AlO2-+H2↑
B.Na与水反应:Na+2H2O=Na++H2↑+2OH-
C.向AlCl3溶液中加入过量NaOH溶液:Al3++3OH-=Al(OH)3↓
D.AlCl3溶液中滴入过量的氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH4+
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质。在一定温度下,氧化铁可以与一氧化碳发生下列反应:
Fe2O3(s)+3CO(g)2Fe(s)+3CO2(g)
(1)该温度下,在2 L盛有Fe2O3粉末的密闭容器中通入CO气体,10 min后,生成了单质铁11.2 g。则10 min内CO的平均反应速率为________。
(2)请用上述反应中某种气体的有关物理量来说明该反应已达到平衡状态:
①_____________________;
②_____________________。
(3)某些金属氧化物粉末和铝粉在镁条的引燃下可以发生铝热反应。下列反应速率(v)和温度(T)的关系示意图中与铝热反应最接近的是________。

(4)写出氢氧化铝在水中发生碱式电离的电离方程式:_____________________;
欲使上述体系中铝离子浓度增加,可加入的物质是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
有一种锂水电池,可作为鱼雷和潜艇的储备电源。电池以金属锂和钢板为电极材料,LiOH为电解质,使用时加入水即可放电。关于该电池的说法正确的是( )
A.钢板为正极,钢板上发生还原反应
B.放电时电子的流动方向是“正极→导线→负极”
C.放电过程中OH-向正极做定向移动
D.总反应:2Li+2H+==2Li++H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨反应为3H2+N2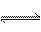 2NH3,其反应速率可以分别为v(H2)、v(N2)、v(NH3)[mol·(L·s)-1]表示,则正确的关系式为( )
2NH3,其反应速率可以分别为v(H2)、v(N2)、v(NH3)[mol·(L·s)-1]表示,则正确的关系式为( )
A.v(H2)=v(N2)=v(NH3) B.3v(H2)=v(N2)
C.v(NH3)=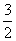 v(H2) D.v(H2)=3v(N2)
v(H2) D.v(H2)=3v(N2)
查看答案和解析>>
科目:高中化学 来源: 题型:
写出铝单质与强酸、强碱溶液反应的离子方程式,并标出电子转移的方向和数目:________、________。日常生活中接触到的易拉罐有铁质和铝质之分,听装啤酒是铝质易拉罐,向一只充满二氧化碳气体的铝质易拉罐中加入适量的氧氧化钠溶液,并及时堵住,观察到的现象是________,用化学方程式表示产生这一现象的原因是________。若用薄铁质易拉罐做上述实验出现的结果是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于反应能量的说法正确的是( )
A.Zn(s)+CuSO4(aq)===ZnSO4(aq)+Cu(s)
ΔH=-216 kJ/mol,反应物总能量>生成物总能量
B.CaCO3(s)===CaO(s)+CO2(g) ΔH=+178.5 kJ/mol,反应物总能量>生成物总能量
C.101kPa时,2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ/mol,H2的燃烧热为571.6 kJ/mol
D.H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ/mol,含1 molNaOH的氢氧化钠溶液与含0.5 mol H2SO4的浓硫酸混合后放出57.3 kJ的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
已知难溶于水的盐在水中存在溶解平衡,例如氯化银在水中的溶解平衡为AgCl(s) Ag++Cl-
Ag++Cl-
在一定温度下,水溶液中银离子(Ag+)和氯离子(Cl-)的物质的量浓度的乘积为一常数,可用Ksp表示:Ksp=c(Ag+)·c(Cl-)=1.8×10-10
现把氯化银(足量)分别放入:①100 mL蒸馏水中;②100 mL0.1 mol/L盐酸溶液中;③1 000 mL0.1 mol/L的氯化铝溶液中;④100 mL 0.01 mol/L的氯化镁溶液中,充分搅拌后,相同温度下,银离子浓度由大到小的顺序是(用序号回答)________________________。
在0.1 mol/L氯化铝溶液中,银离子的物质的量浓度最大可达到__________mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
通过粮食发酵可获得某含氧有机化合物X,其相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13.0%。
(1)X的分子式是______________________。
(2) X与空气中的氧气在铜或银催化下反应生成Y,Y的结构式是________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com