
铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质。在一定温度下,氧化铁可以与一氧化碳发生下列反应:
Fe2O3(s)+3CO(g)2Fe(s)+3CO2(g)
(1)该温度下,在2 L盛有Fe2O3粉末的密闭容器中通入CO气体,10 min后,生成了单质铁11.2 g。则10 min内CO的平均反应速率为________。
(2)请用上述反应中某种气体的有关物理量来说明该反应已达到平衡状态:
①_____________________;
②_____________________。
(3)某些金属氧化物粉末和铝粉在镁条的引燃下可以发生铝热反应。下列反应速率(v)和温度(T)的关系示意图中与铝热反应最接近的是________。

(4)写出氢氧化铝在水中发生碱式电离的电离方程式:_____________________;
欲使上述体系中铝离子浓度增加,可加入的物质是______________________。
解析:(1)Fe2O3(s)+3CO(g)2Fe(s)+3CO2(g)
3 2
0.3 mol 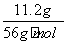
则v(CO)= =0.015 mol·L-1·min-1。
=0.015 mol·L-1·min-1。
(2)如果CO[或CO2]的消耗速率和生成速率相等时,达到化学平衡状态。或某一气体浓度保持不变,也说明达到平衡状态。
(3)铝热反应非常剧烈,温度越高,反应速率越大。
(4)Al(OH)3中存在平衡Al(OH)3Al3++3OH-,减少c(OH-)可使平衡右移,c(Al3+)增加,如加酸。
答案:(1)0.015 mol/(L·min)
(2)①CO[或CO2]的消耗速率和生成速率相等
②CO[或CO2]的质量不再改变(其他合理答案也正确) (3)b (4)Al(OH)3Al3++3OH-
盐酸(或其他合理答案)


科目:高中化学 来源: 题型:
一定量某营养液中溶质的配方分别如下:
配方一:0.2mol KCl,0.1mol K2SO4,0.3 molZnSO4
配方二:0.1 mol KCl,0. 3 mol K2SO4,0.1 molZnCl2
3 mol K2SO4,0.1 molZnCl2
对于两种营养液的成分,下列说法中正确的是( )
A.只有n (K+)相同 B.只有n (Cl-)相同
C.各离子的物质的量完全相同 D.各离子的物质的量完全不同
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是 ( )
A.1L水中溶解了58.5 g NaCl,该溶液的物质的量浓度为1mol/L
B.从1L2mol/L的H2SO4溶液中取出0.5L,该溶液的浓度为1mol/L
C.配制500mL0.2mol/L的CuSO4溶液,需25g胆矾
D.中和100mL1mol/L的H2SO4溶液,需NaOH4g
查看答案和解析>>
科目:高中化学 来源: 题型:
T ℃时在2 L的密闭容器中X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图(1)所示;若保持其他条件不变,反应温度分别为T1和T2时,Y的体积分数与时间的关系如图(2)所示。
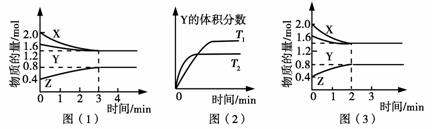
则下列结论正确的是( )
A.反应进行的前3 min内,用X表示的反应速率v(X)=0.3 mol·(L·min)-1
B.容器中发生的反应可表示为3X(g)+Y(g)2Z(g)
C.保持其他条件不变,升高温度,反应的化学平衡常数K减小
D.若改变反应条件,使反应进程如图(3)所示,则改变的条件是增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实不能用勒夏特列原理解释的是( )
A.由NO2和N2O4组成的平衡体系加压后颜色先变深后变浅
B.增大压强可加快SO2转化为SO3的速率
C.黄绿色的氯水光照后颜色变浅
D.在含有Fe(SCN)3的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.0.5 mol O3与11.2 L O2所含的分子数一定相等
B.25 ℃与60 ℃时,水的pH相等
C.中和等体积、等物质的量浓度的盐酸和醋酸所消耗的n(NaOH)相等
D.2SO2(g)+O2(g)===2SO3(g)和4SO2(g)+2O2(g)===4SO3(g)的ΔH相等
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关说法正确的是( )
A.CaCO3(s)===CaO(s)+CO2(g)室温下不能自发进行,说明该反应的ΔH<0
B.镀铜铁制品镀层受损后,铁制品比受损前更容易生锈
C.N2(g)+3H(g)===2NH3(g) ΔH<0,其他条件不变时升高温度,反应速率v(H2)和H2的平衡转化率均增大
D.水的离子积常数Kw随着温度的升高而增大,说明水的电离是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列过程伴随的能量变化中,属于反应热的是( )
A.形成1 mol H—Cl键放出的能量
B.石墨转变成金刚石吸收的能量
C.1 mol O2形成2 mol O原子吸收的能量
D.水蒸气变成液态水放出的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应的离子方程式书写正确的是( )。
A.铝片放入氢氧化钠溶液中:Al+2OH-=AlO2-+H2↑
B.Na与水反应:Na+2H2O=Na++H2↑+2OH-
C.向AlCl3溶液中加入过量NaOH溶液:Al3++3OH-=Al(OH)3↓
D.AlCl3溶液中滴入过量的氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH4+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com