
【题目】A、B、C分别是元素甲、乙、丙的单质,它们都是常见的金属或非金属,D、E、F是常见的三种氧化物,且有如图所示转化关系,则下列说法不正确的是( )

A. A、B、C中一定有一种是氧元素的单质
B. 单质B肯定是氧化剂
C. D、E中一定都含有A的元素
D. 若A是非金属,则B一定为金属
【答案】B
【解析】
由转化关系可以知道A+D![]() E和A+C
E和A+C![]() E都是化合反应,故E中一定含有甲元素,而B+D
E都是化合反应,故E中一定含有甲元素,而B+D![]() A+F是置换反应,D、E、F是常见的三种氧化物,则C应为O2,结合转化关系可以知道,若A为C,D为CO2,E为CO,B为Mg,F为MgO符合转化关系。
A+F是置换反应,D、E、F是常见的三种氧化物,则C应为O2,结合转化关系可以知道,若A为C,D为CO2,E为CO,B为Mg,F为MgO符合转化关系。
A.由上述分析可以知道,C为氧气,所以A选项是正确的;B.在氧化物中O为-2价,B为单质,B与氧化物D发生置换反应时,D被还原为A,则B失去电子作还原剂,故B错误;C.由A+D![]() E和A+C
E和A+C![]() E都是化合反应,故E中一定含有甲、丙元素,而B+D
E都是化合反应,故E中一定含有甲、丙元素,而B+D![]() A+F是置换反应,B是单质(含乙元素),A是甲元素的单质,则甲元素只能来自化合物D,所以C选项是正确的;D.由上述分析可以知道,A为非金属C,则B为金属Mg,所以D选项是正确的;答案:B。
A+F是置换反应,B是单质(含乙元素),A是甲元素的单质,则甲元素只能来自化合物D,所以C选项是正确的;D.由上述分析可以知道,A为非金属C,则B为金属Mg,所以D选项是正确的;答案:B。


科目:高中化学 来源: 题型:
【题目】(13分)用辉铜矿(主要成分为 Cu2S,含少量Fe2O3、SiO2,等杂质)制备难溶于水的碱式碳酸铜的流程如下:

(1)下列措施是为了加快浸取速率,其中无法达到目的的是____(填字母)。
A.延长浸取时间 | B.将辉铜矿粉碎 |
C.充分搅拌 | D.适当增加硫酸浓度 |
(2)滤渣I巾的主要成分是MnO2、S、SiO2,请写出“浸取”反应中生成S的离子方程式:_______。
(3)研究发现,若先除铁再浸取,浸取速率明显变慢,可能的原因是___________。
(4)“除铁”的方法是通过调节溶液pH,使Fe3+转化为Fe(OH)3,则加入的试剂A可以是_______(填化学式);“赶氨”时,最适宜的操作方法是________。
(5)“沉锰”(除Mn2+)过程中有关反应的离子方程式为_______。
(6)滤液Ⅱ经蒸发结晶得到的盐主要是___________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应的离子方程式正确的是( )
A.0.01mol/L NH4Al(SO4)2溶液与0.02mol/L Ba(OH)2溶液等体积混合NH4++Al3++2SO42﹣+2Ba2++4OH﹣=2BaSO4↓+Al(OH)3↓+NH3H2O
B.Na2O2加入H218O中:2Na2O2+2H218O=4Na++4OH﹣+18O2↑
C.NH4HCO3溶液与过量NaOH溶液共热:NH4++OH﹣![]() NH3↑+H2O
NH3↑+H2O
D.浓硝酸中加入过量铁粉并加热:Fe+3NO3﹣+6H+![]() Fe3++3NO2↑+3H2O
Fe3++3NO2↑+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某试液中只可能含有K+、NH4+、Fe2+、Al3+、Cl-、SO42-、CO32-、AlO2- 中的若干种离子,离子浓度均为0.1 mol·L-1。某同学进行了如下实验,下列说法正确的是
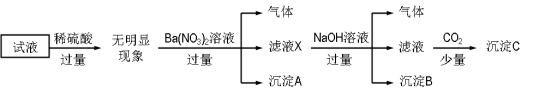
A.无法确定原试液中是否含有Al3+、Cl-
B.滤液X中大量存在的阳离子有NH4+、Fe2+和Ba2+
C.无法确定沉淀C的成分
D.原溶液中存在的离子为NH4+、Fe2+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在酸性溶液中可发生如下反应: R2O72-+ 6Fe2+ + 14H+ =6Fe3+ +2Rn+ +7H2O,则Rn+中R的化合价是
A. +3 B. +4 C. +5 D. +6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的说法不正确的是
A.天然气的主要成份是乙烯
B.芳香烃主要来自于煤干馏后的煤焦油
C.汽油、煤油、柴油主要来自于石油的常压蒸馏
D.乙烯是石油裂解后的产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机化合物名称正确的是( )
①1-甲基丙烷 ②3,4-二甲基戊烷 ③2-乙基丁烷 ④2-甲基-3-乙基戊烷
A.②③B.③④C.①②③④D.④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电镀工业上,为了提高镀锌的效果,通常采用Zn(CN)42-溶液代替Zn2+溶液进行电解。请回答下列问题:
(1)元素锌在周期表中的位置为_____________,基态Zn的价电子排布式为_____________。
(2)Zn(CN) 42-所含元素中,电负性最大的元素是_____________,Zn(CN) 42-中含有的化学键类型有σ键和_____________。
(3)CN-中C的杂化类型为_____________,与CN-互为等电子体的单质为_____________。
(4)H2CO3与HNO3的酸性相差较大,请解释其原因_____________。
(5)N和Al可组成一种新型半导体材料AlN;AlN具有耐高温,耐磨性能。其晶体类型为_____________,其晶体结构如图,已知晶胞边长为apm,则AlN的密度为_____________(用含a、NA的代数式表示)g/cm3。
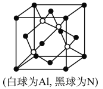
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com