
【题目】氮、磷、硼、砷的化合物用途非常广泛。根据所学知识回答下列问题:
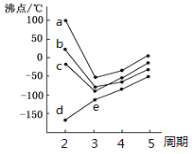
(1)如图所示,每条折线表示周期表ⅣA-ⅦA中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a、b、c、d、e对应元素电负性最大的是__(用元素符号表示),e点代表的第三周期某元素的基态原子核外电子占据的最高能层符号为__,该能层具有的原子轨道数为__。
(2)已知反应:(CH3)3C-F+SbF5→(CH3)3CSbF6,该反应可生成(CH3)3C+,该离子中碳原子杂化方式有__。
(3)一种新型储氢化合物氨硼烷是乙烷的等电子体,且加热氨硼烷会慢慢释放氢气,推断氨硼烷的结构式为__(若含有配位键,要求用箭头表示)。
(4)PCl5是一种白色晶体,在恒容密闭容器中加热可在148℃液化,形成一种能导电的熔体,测得其中含有一种正四面体形阳离子和一种正八面体形阴离子,熔体中P-Cl的键长只有198nm和206nm两种,这两种离子的化学式为__;正四面体形阳离子中键角大于PCl3的键角原因为___。
(5)砷化硼为立方晶系晶体,该晶胞中原子的分数坐标为:
B:(0,0,0);(![]() ,
,![]() ,0);(
,0);(![]() ,0,
,0,![]() );(0,
);(0,![]() ,
,![]() )
)
As:(![]() ,
,![]() ,
,![]() );(
);(![]() ,
,![]() ,
,![]() );(
);(![]() ,
,![]() ,
,![]() );(
);(![]() ,
,![]() ,
,![]() )
)
①请在图中画出砷化硼晶胞的俯视图__。
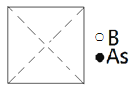
②与砷原子紧邻的硼原子有__个,与每个硼原子紧邻的硼原子有__个。
【答案】F M 9 sp3、sp2  PCl4+、PCl6- 两者磷原子均采取sp3杂化,PCl3分子中P原子有一对孤电子对,孤电子和对成键电子对斥力更大,PCl4+中P没有孤电子对,正四面体形阳离子中键角大于PCl3的键角
PCl4+、PCl6- 两者磷原子均采取sp3杂化,PCl3分子中P原子有一对孤电子对,孤电子和对成键电子对斥力更大,PCl4+中P没有孤电子对,正四面体形阳离子中键角大于PCl3的键角  4 12
4 12
【解析】
(1)从图中可以看出,a、b、c、d都是第二周期元素的氢化物的沸点,由于NH3、H2O、HF分子间都能形成氢键,使它们的沸点升高,只有CH4分子间不能形成氢键,所以沸点最低,从而得出d为CH4的沸点,e为SiH4的沸点。在形成氢化物的分子中,HF形成氢键的能量最大,沸点最高。
(2) (CH3)3C+离子中,CH3-价电子对数为4,与3个-CH3相连的C,价电子对数为3,由此可确定碳原子杂化方式。
(3)氨硼烷是乙烷的等电子体,则氨硼烷的结构简式为H2NBH2,由此可推出其结构式。
(4)PCl5晶体中,正四面体形阳离子应为AB4+型,正八面体形阴离子应为AB6-型,由此可得出两种离子的化学式;正四面体形阳离子中键角大于PCl3的键角,其原因可从孤电子对的排斥作用进行分析。
(5)从砷化硼晶体中原子的分数坐标可以看出,B原子在立方体的顶点和面心:As原子在晶胞中的八个小立方体的体心。
①砷化硼晶胞的俯视图中,B原子位于正方形的中心、顶点和棱心,4个As原子位于对角线上,且离顶点四分之一处。
②与砷原子紧邻的硼原子位于小立体的体心,砷原子位于小立方体的顶点;与每个硼原子(设此硼原子在立方体的顶点)紧邻的硼原子在相交于此顶点的三个面心。
(1)由以上分析可知,d为CH4的沸点,e为SiH4的沸点。在形成氢化物的分子中,HF形成氢键的能量最大,沸点最高。从而得出a、b、c、d、e对应元素电负性最大的是F,在Si的基态原子中,核外电子占据的最高能层符号为M,该能层具有的原子轨道(包括3s、3p、3d所具有的轨道)数共为9。答案为:F;M;9;
(2) (CH3)3C+离子中,CH3-价电子对数为4,与3个-CH3相连的C,价电子对数为3,由此可确定碳原子杂化方式分别为sp3、sp2。答案为:sp3、sp2;
(3)氨硼烷是乙烷的等电子体,则氨硼烷的结构简式为H2NBH2,由此可推出其结构式为 。答案为:
。答案为: ;
;
(4)PCl5晶体中,正四面体形阳离子应为AB4+型,正八面体形阴离子应为AB6-型,由此可得出两种离子的化学式分别为PCl4+、PCl6-;正四面体形阳离子中键角大于PCl3的键角,其原因是:两者磷原子均采取sp3杂化,PCl3分子中P原子有一对孤电子对,孤电子和对成键电子对斥力更大,PCl4+中P没有孤电子对,正四面体形阳离子中键角大于PCl3的键角。答案为:PCl4+、PCl6-;两者磷原子均采取sp3杂化,PCl3分子中P原子有一对孤电子对,孤电子和对成键电子对斥力更大,PCl4+中P没有孤电子对,正四面体形阳离子中键角大于PCl3的键角;
(5)从砷化硼晶体中原子的分数坐标可以看出,B原子在立方体的顶点和面心:As原子在晶胞中的八个小立方体的体心。
①砷化硼晶胞的俯视图中,B原子位于正方形的中心、顶点和棱心,4个As原子位于对角线上,且离顶点四分之一处。则砷化硼晶胞的俯视图为 。答案为:
。答案为: ;
;
②与砷原子紧邻的硼原子位于小立体的体心,砷原子位于小立方体的顶点,则与砷原子紧邻的硼原子有4个;与每个硼原子(设此硼原子在立方体的顶点)紧邻的硼原子在相交于此顶点的三个面心,则与每个硼原子紧邻的硼原子有12个。答案为:4;12。


科目:高中化学 来源: 题型:
【题目】氯化亚铜(![]() )在化工、印染、电镀等行业应用广泛。
)在化工、印染、电镀等行业应用广泛。![]() 微溶于水,不溶于醇和稀酸,可溶于
微溶于水,不溶于醇和稀酸,可溶于![]() 浓度较大的溶液,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量
浓度较大的溶液,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量![]() )为原料,采用硝酸铵氧化分解技术生产
)为原料,采用硝酸铵氧化分解技术生产![]() 的工艺过程如图。回答下列问题:
的工艺过程如图。回答下列问题:

(1)步骤①中N元素被还原为最低价,写出此反应的离子方程式______________。
(2)步骤②中,亚硫酸铵要略保持过量,原因是___________,滤液中可循环利用的物质是__________。
(3)步骤⑤中,用“醇洗”可快速去除滤渣表面的水,防止滤渣被空气氧化为![]() 被氧化为
被氧化为![]() 的化学方程式为______________________。
的化学方程式为______________________。
(4)用![]() 溶液测定氯化亚铜样品纯度(假设杂质不参与反应),步骤如下:准确称取所制备的氯化亚铜样品
溶液测定氯化亚铜样品纯度(假设杂质不参与反应),步骤如下:准确称取所制备的氯化亚铜样品![]() ,将其置于过量的
,将其置于过量的![]() 溶液中,待样品完全溶解后,加入适量稀硫酸配成
溶液中,待样品完全溶解后,加入适量稀硫酸配成![]() 溶液,取溶液
溶液,取溶液![]() 用
用![]() 溶液进行滴定,反应中
溶液进行滴定,反应中![]() 被还原成
被还原成![]() ,相关数据记录如表所示:该样品中
,相关数据记录如表所示:该样品中![]() 的质量分数__________________。
的质量分数__________________。
实验编号 | 1 | 2 | 3 |
消耗 | 14.98 | 16.03 | 15.02 |
(5)制造印刷电路板产生的废液中含大量![]() 等离子,利用膜电解技术对此废液进行电解,电解装置如图所示。电解后的阴极液中加入适量盐酸并用水稀释可得到
等离子,利用膜电解技术对此废液进行电解,电解装置如图所示。电解后的阴极液中加入适量盐酸并用水稀释可得到![]() ,电解时阴极的电极反应式为___________,生成
,电解时阴极的电极反应式为___________,生成![]() 的离子方程式为________________________________。
的离子方程式为________________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图装置电解硫酸钾溶液来制取氧气、氢气、硫酸和氢氧化钾。
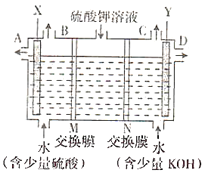
(1)X极与电源的________(填“正”或“负”)极相连。氢气从________(填“B”或“C”)口导出。
(2)已知离子交换膜只允许某类离子通过,则M为________(填“阴离子”或“阳离子”)交换膜。
(3)若制得氧气5.6L(标准状况),则生成氢氧化钾的质量是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人们对苯及芳香烃的认识有一个不断深化的过程,回答下列问题:
(1)由于苯的含碳量与乙炔相同,人们认为它是一种不饱和烃,写出分子式为C6H6的一种含两个三键且无支链的链烃的结构简式________.
(2)已知分子式为C6H6的有机物有多种,其中的两种为:(Ⅰ)![]() 、
、![]() .
.
①这两种结构的区别表现在以下两方面:
定性方面(即化学性质方面):(Ⅱ)能________(填字母),而(Ⅰ)不能.
a.被高锰酸钾酸性溶液氧化 b.与溴水发生加成反应
c.与溴发生取代反应 d.与氢气发生加成反应
定量方面(即消耗反应物的量的方面):1 mol C6H6与H2加成时:(Ⅰ)需要H2________mol,而(Ⅱ)需要H2________mol.
②今发现C6H6还可能有一种如图所示的立体结构![]() ,该结构的二氯代物有________种.
,该结构的二氯代物有________种.
(3)萘也是一种芳香烃,它的分子式是C10H8,请你判断它的结构简式可能是________(填字母).
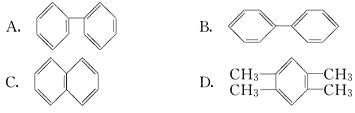
(4)现代化学认为,萘分子中碳碳键是________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了测定某有机物A的结构,做如下实验:
①将2.3 g该有机物完全燃烧,生成0.1 mol CO2和2.7 g水;
②用质谱仪测定其相对分子质量,得如图一所示的质谱图;
③用核磁共振仪处理该化合物,得到如图二所示图谱,图中三个峰的面积之比是1∶2∶3。试回答下列问题:
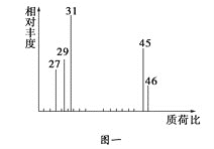
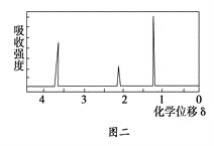
(1)有机物A的相对分子质量是________。
(2)有机物A的实验式是________。
(3)A的分子式是_______________________________________。
(4)A的结构简式为___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用 NA 表示阿伏加德罗常数,下列说法中正确的是
A.1 L 1 mol·L-1 的醋酸溶液中 H+的数目为 NA
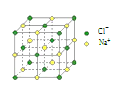
B.4 mol NaCl 晶体中含有右图所示的结构单元的数目为 NA
C.71 g Cl2 通入水中,HClO、Cl-两种粒子数目总和为 2NA
D.标准状况下,22.4 L CHCl3 和 CCl4 的混合物所含有分子数目为 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】描述弱电解质电离情况可以用电离度和电离平衡常数表示,下表是常温下几种弱酸的电离平衡常数(Ka)和弱碱的电离平衡常数(Kb)
酸或碱 | 电离平衡常数(Ka或Kb) |
CH3COOH | 1.8×10-5 |
HNO2 | 4.6×10-4 |
HCN | 5×10-10 |
HClO | 3×10-8 |
NH3H2O | 1.8×10-5 |
下表是常温下几种难(微)溶物的溶度积常数(Ksp):
难(微)溶物 | 溶度积常数(Ksp) |
BaSO4 | 1×10-10 |
BaCO3 | 2.6×10-9 |
CaSO4 | 7×10-5 |
CaCO3 | 5×10-9 |
请回答下列问题:
(l)写出HCN的电离方程式:___________,HClO的电子式__________。
(2)表中所给的四种酸中,酸性最强的是__________(用化学式表示)。下列能使醋酸溶液中CH3COOH的电离程度增大且电离常数改变的操作是__________(填字母序号)。
A.加少量冰酷酸 B.降低温度 C.加水稀释 D.升高温度 E.加少量的CH3COONa固体
(3)CH3COONH4的水溶液呈__________(选填“酸性”、“中性”或“碱性”),该溶液中存在的各离子浓度大小关系是__________。
(4)工业中常将BaSO4转化为BaCO3后,再将其制成各种可溶性的钡盐(如BaCl2)。具体做法是用饱和的纯碱溶液浸泡BaSO4粉末,并不断补充纯碱,最后BaSO4转化为BaCO3。现有足量BasO4悬浊液,在该悬浊液中加纯碱粉末并不断搅拌,为使SO42-物质的量浓度不小于0.02 mol·L-1,则溶液中CO32-物质的量浓度应≥__________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
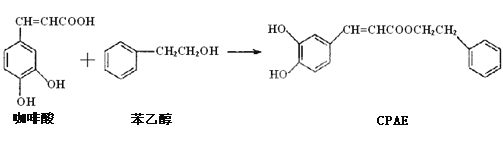
【题目】CPAE是蜂胶的主要活性成分,由咖啡酸合成CPAE的路线如下:
 +H2O
+H2O
下列关于上述所列有机物的说法中正确的是( )
A.咖啡酸、CPAE及苯乙醇都能发生取代、加成、氧化及消去反应
B.用FeCl3溶液可以来检测上述反应中是否有CPAE生成
C.苯乙醇是最简单的芳香醇,与邻乙基苯酚互为同系物关系
D.1mol的咖啡酸最多可与4mol Br2发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D是中学化学的常见物质,且A、B、C均含有同一种元素。在一定条件下它们之间的相互转化关系如图所示(部分反应中的H2O已略去)。请回答下列问题:

(1)若A可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,加热蒸干B的溶液不能得到B。则B的化学式为__。
(2)若D是氯碱工业的主要产品之一,B有两性,则反应②的离子方程式是__。
(3)若A、C、D都是常见气体,C是导致酸雨的主要气体,则反应③的化学方程式为___。
(4)若A的焰色反应呈黄色,D为二氧化碳,则反应②的离子方程式是___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com