
【题目】描述弱电解质电离情况可以用电离度和电离平衡常数表示,下表是常温下几种弱酸的电离平衡常数(Ka)和弱碱的电离平衡常数(Kb)
酸或碱 | 电离平衡常数(Ka或Kb) |
CH3COOH | 1.8×10-5 |
HNO2 | 4.6×10-4 |
HCN | 5×10-10 |
HClO | 3×10-8 |
NH3H2O | 1.8×10-5 |
下表是常温下几种难(微)溶物的溶度积常数(Ksp):
难(微)溶物 | 溶度积常数(Ksp) |
BaSO4 | 1×10-10 |
BaCO3 | 2.6×10-9 |
CaSO4 | 7×10-5 |
CaCO3 | 5×10-9 |
请回答下列问题:
(l)写出HCN的电离方程式:___________,HClO的电子式__________。
(2)表中所给的四种酸中,酸性最强的是__________(用化学式表示)。下列能使醋酸溶液中CH3COOH的电离程度增大且电离常数改变的操作是__________(填字母序号)。
A.加少量冰酷酸 B.降低温度 C.加水稀释 D.升高温度 E.加少量的CH3COONa固体
(3)CH3COONH4的水溶液呈__________(选填“酸性”、“中性”或“碱性”),该溶液中存在的各离子浓度大小关系是__________。
(4)工业中常将BaSO4转化为BaCO3后,再将其制成各种可溶性的钡盐(如BaCl2)。具体做法是用饱和的纯碱溶液浸泡BaSO4粉末,并不断补充纯碱,最后BaSO4转化为BaCO3。现有足量BasO4悬浊液,在该悬浊液中加纯碱粉末并不断搅拌,为使SO42-物质的量浓度不小于0.02 mol·L-1,则溶液中CO32-物质的量浓度应≥__________mol·L-1。
【答案】HCN![]() H++CN-
H++CN- ![]() HNO2 D 中性 c(
HNO2 D 中性 c(![]() )=c(CH3COO-)> c(H+)= c(OH-) 0.52
)=c(CH3COO-)> c(H+)= c(OH-) 0.52
【解析】
(1)由表可知,HCN为弱酸,其电离方程式为:HCN![]() H++CN-;HClO为共价化合物,其电子式为:
H++CN-;HClO为共价化合物,其电子式为:![]() ;
;
(2)电离平衡常数越大,酸的酸性越强,由表中数据可知,酸性最强的是:HNO2;要使电离平衡常数该变,则温度必须该变,弱电解质的电离为吸热过程,因此升高温度可增加电离程度,故答案为:D;
(3)CH3COOH的酸性与NH3H2O的碱性相同,因此CH3COONH4的水溶液呈中性;因微粒水解较为微弱,且CH3COO-与![]() 水解程度相同,故溶液中离子浓度大小关系为:c(
水解程度相同,故溶液中离子浓度大小关系为:c(![]() )=c(CH3COO-)> c(H+)= c(OH-);
)=c(CH3COO-)> c(H+)= c(OH-);
(4)该过程涉及反应:![]() ,该反应的平衡常数
,该反应的平衡常数 ,当溶液中
,当溶液中![]() 浓度不低于0.02mol/L,则
浓度不低于0.02mol/L,则![]() 。
。


科目:高中化学 来源: 题型:
【题目】含镁、氮、磷、砷等元素的化合物在化工生产、药物化学及催化化学等领域应用广泛。回答下列问题:
(1)下列状态的镁中,电离最外层一个电子所需能量最大的是_____(填序号)。
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
(2)晶格能又叫点阵能。它是1mol 离子化合物中的正、负离子从相互分离的气态结合成离子晶体时所放出的能量。MgO 晶格能可通过如图所示的Borm Haber循环计算得到。
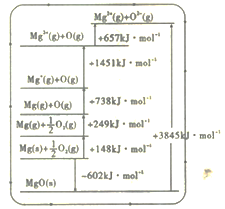
Mg的第二电离能为______kJ·mol-1;MgO的晶格能为___________kJ·mol-1。
(3)乙二胺(H2NCH2CH2NH2) 是一种有机化合物,其中N原子的杂化类型是____,该有机化合物能与Mg2+、Cu2+等金属离子形成稳定环状离子,其原因是______,其中与乙二胺形成的化合物稳定性相对较高的是_______(填 “Mg2+ ”或“Cu2+” )。
(4) PCl5是一种白色固体,加热到160°C不经过液态阶段就变成蒸气,测得180°C下的蒸气密度(折合成标准状况)为9.3g·L-1,分子的极性为零,P-Cl键长为204pm和211pm两种。在180°C下PCl5蒸气中存在的分子形式为____(填化学式),分子的空间构型为______,P、Cl的电负性由大到小顺序为________。
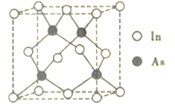
(5)砷和铟组成的一种化合物属于半导体材料,其晶胞结构如图所示。已知晶胞的参数为a pm,阿伏加德罗常数的值为NA,则该晶体的密度为_____g. cm-3 (用含a和NA的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮、磷、硼、砷的化合物用途非常广泛。根据所学知识回答下列问题:
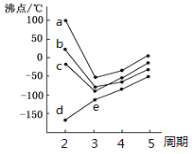
(1)如图所示,每条折线表示周期表ⅣA-ⅦA中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a、b、c、d、e对应元素电负性最大的是__(用元素符号表示),e点代表的第三周期某元素的基态原子核外电子占据的最高能层符号为__,该能层具有的原子轨道数为__。
(2)已知反应:(CH3)3C-F+SbF5→(CH3)3CSbF6,该反应可生成(CH3)3C+,该离子中碳原子杂化方式有__。
(3)一种新型储氢化合物氨硼烷是乙烷的等电子体,且加热氨硼烷会慢慢释放氢气,推断氨硼烷的结构式为__(若含有配位键,要求用箭头表示)。
(4)PCl5是一种白色晶体,在恒容密闭容器中加热可在148℃液化,形成一种能导电的熔体,测得其中含有一种正四面体形阳离子和一种正八面体形阴离子,熔体中P-Cl的键长只有198nm和206nm两种,这两种离子的化学式为__;正四面体形阳离子中键角大于PCl3的键角原因为___。
(5)砷化硼为立方晶系晶体,该晶胞中原子的分数坐标为:
B:(0,0,0);(![]() ,
,![]() ,0);(
,0);(![]() ,0,
,0,![]() );(0,
);(0,![]() ,
,![]() )
)
As:(![]() ,
,![]() ,
,![]() );(
);(![]() ,
,![]() ,
,![]() );(
);(![]() ,
,![]() ,
,![]() );(
);(![]() ,
,![]() ,
,![]() )
)
①请在图中画出砷化硼晶胞的俯视图__。
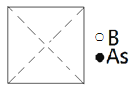
②与砷原子紧邻的硼原子有__个,与每个硼原子紧邻的硼原子有__个。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向100 mL 0.01 mol·L-1 HA溶液中逐滴加入0.02 mol·L-1 MOH溶液,图中所示的曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计)。下列说法中,正确的是
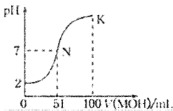
A.HA为一元弱酸
B.MOH为一元强碱
C.N点水的电离程度小于K点水的电离程度
D.K点时,则有c(MOH)+c(OH-)-c(H+)=0.005 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
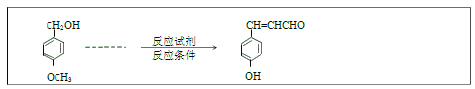
【题目】乙酸甲酯催化醇解反应可用于制备甲醇和乙酸己酯,该反应的化学方程式为: CH3COOCH3(l) +C6H13OH (l) ![]() CH3COOC6H13(l) +CH3OH(l)
CH3COOC6H13(l) +CH3OH(l)
反应开始时,己醇和乙酸甲酯按物质的量之比 1:1 投料,测得 348 K、343 K 两个温度 下乙酸甲酯转化率(α)随时间(t)的变化关系如下图所示:
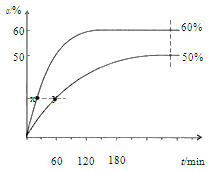
下列说法不正确的是
A.该醇解反应的ΔH > 0
B.反应速率:v(x)> v(y)
C.343K时,以物质的量分数表示的化学平衡常数 Kx=2.25
D.348K时,初始投料![]() 分别按 1:1和2:1进行,Kx 相同
分别按 1:1和2:1进行,Kx 相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】托特罗定(G)是毒蕈碱受体拮抗剂,其一种合成路线流程图如下:
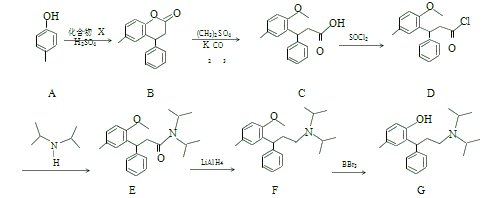
请按要求回答下列问题:
(1)A 的名称:_____;最多共平面的原子数目为_____。C 中含氧官能团名称为_________。
(2)D→E的反应类型为_____。
(3)B 与 NaOH 溶液加热条件下反应的化学方程式:____________。
(4)C→D 反应过程使用的液态 SOCl2(![]() )沸点为 77℃,遇水剧烈反应,产生酸雾和刺激性气味的气体。写出 SOCl2 与水的化学方程式:____________。
)沸点为 77℃,遇水剧烈反应,产生酸雾和刺激性气味的气体。写出 SOCl2 与水的化学方程式:____________。
(5)同时满足下列条件的 C 的同分异构体共有______________种。写出其中一种结构简式______________。
a.在酸性条件下完全水解,得到两种产物:有机物 M 和碳酸(![]() )
)
b.M 分子中有 4 种不同化学环境的氢,且能与 FeCl3 溶液发生显色反应。
(6)已知:R'-CHO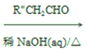 R'-CH=CCHO (R1、R2 代表烃基或 H),请结合上述信息,写出以
R'-CH=CCHO (R1、R2 代表烃基或 H),请结合上述信息,写出以![]() 和乙醛为主要原料制备
和乙醛为主要原料制备 ![]() 的合成路线流程图_____________(无机试剂任选):
的合成路线流程图_____________(无机试剂任选):
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在15mL0.lmol/LKOH溶液中逐滴加入0.2mol/L甲酸(HCOOH,弱酸)溶液,溶液pH和加入甲酸的体积关系曲线如图所示,下列关系正确的是
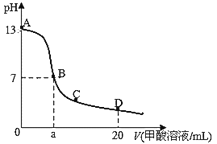
A.在B点:c(K+)=c(HCOO-)>c(OH-)=c(H+),且a=7.5
B.在A、B间任意一点,c(HCOO-)>c(K+)>c(OH-)>c(H+)
C.B→C段:水的电离程度先增大后减小
D.在D点:c(HCOO-)+c(HCOOH)>2c(K+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有4种无色液态物质:①CH3(CH2)3CH=CH2、②CH3(CH2)4CH3、③![]() 、④
、④![]() 。
。
(1)不能与溴水和酸性KMnO4溶液反应,但在铁屑作用下能与液溴反应的是___(填序号,下同),生成的有机物是___(填名称),反应的化学方程式为___。
(2)能与溴水和酸性KMnO4溶液反应的是___,与溴水反应的化学方程式是___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com