
��1������ר����Ϊ�����ý�������ˮ���е�NO![]() ת��ΪN2���Ӷ������Ⱦ���÷�Ӧ���漰�������У�H2O��Al��OH
ת��ΪN2���Ӷ������Ⱦ���÷�Ӧ���漰�������У�H2O��Al��OH![]() ��Al(OH)3��NO
��Al(OH)3��NO![]() ��N2���뽫�����ӷֱ��������¿ո��ڣ�������ƽ����
��N2���뽫�����ӷֱ��������¿ո��ڣ�������ƽ����
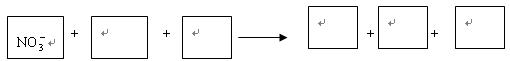
�÷�Ӧ�����У��������뱻��ԭ��Ԫ�ص����ʵ���֮��Ϊ ��
��2���ҹ��״��ĺ������Ժ�ˮΪ�������Һ������ܷ�ӦΪ��4Al+3O2+6H2O=
4Al(OH)3����������ĵ缫��ӦʽΪ ���������ϲ����˲��������ò���Ϊ�������ŵ��� ��
��3����֪��4Al(s)+3O2(g)=2Al2O3(g) ��H=��2834.9kJ/mol
Fe2O3(s)+![]() C(s)=
C(s)= ![]() CO2(g)+2Fe(s) ��H=234.1kJ/mol
CO2(g)+2Fe(s) ��H=234.1kJ/mol
C(s)+O2(g)=CO2(g) ��H=��393.5kJ/mol
д�������������������ȷ�Ӧ���Ȼ�ѧ����ʽ ��
��4����һ�������������Ͻ�����ˮ�У��Ͻ�ȫ���ܽ⣬�õ�20mol��pH=14����Һ��Ȼ��2mol/L����ζ����ɵó������������ĵ����������ϵ����ͼ��
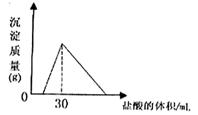
��Ӧ�����в��������������Ϊ L����״������

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��1������ר����Ϊ����������ˮ�е�NO3- ת��ΪN2���Ӷ������Ⱦ���÷�Ӧ���漰�������У�H2O��Al��OH-��Al��OH��3��NO3-��N2���뽫�����ӷֱ��������¿ո��뽫��������ʽ��ƽ��д�ڴ���ֽ�ϣ���
��1������ר����Ϊ����������ˮ�е�NO3- ת��ΪN2���Ӷ������Ⱦ���÷�Ӧ���漰�������У�H2O��Al��OH-��Al��OH��3��NO3-��N2���뽫�����ӷֱ��������¿ո��뽫��������ʽ��ƽ��д�ڴ���ֽ�ϣ���| 3 |
| 2 |
| 3 |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 3 |
| 2 |
| 3 |
| 2 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��������Ϫһ�и�����ѧ�����п������ۻ�ѧ�Ծ��������棩 ���ͣ������
��12�֣���1������ר����Ϊ�����ý�������ˮ���е�NO3 - ת��ΪN2���Ӷ�������Ⱦ���÷�Ӧ���漰�����У�H2O��Al��OH����Al(OH)3��NO3-��N2���뽫��Щ���г�NO3-��������������¿ո��ڣ�������ƽ����

�÷�Ӧ�����У��������뱻��ԭ��Ԫ�ص����ʵ���֮��Ϊ ��
��2���ҹ��״��ĺ������Ժ�ˮΪ�������Һ������ܷ�Ӧ��4Al ��3O2 ��6H2O =4 Al(OH)3 ����������ĵ缫��Ӧʽ�� ������13.5 g Alʱת��_________mole-��
��3������ijЩ�����������ڸ����µķ�Ӧ��Ϊ���ȷ�Ӧ��������ұ�����۵�Ľ�����
��֪��4Al(s) ��3O2(g) = 2Al2O3(s) ��H = ��2830 kJ/mol
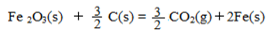 ��H = ��230 kJ/mol
��H = ��230 kJ/mol
C(s)��O2(g) = CO2(g) ��H = ��390 kJ/mol
�����������������ȷ�Ӧ���Ȼ�ѧ����ʽ�� �����ȷ�Ӧ����______������ĸ����Ӧ��
a��������ԭ b�����ֽ� c���û�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010���Ͼ�һ�и�����ǰ��̻�ѧ�� ���ͣ������
��1������ר����Ϊ�����ý�������ˮ���е�NO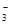 ת��ΪN2���Ӷ������Ⱦ���÷�Ӧ���漰�������У�H2O��Al��OH
ת��ΪN2���Ӷ������Ⱦ���÷�Ӧ���漰�������У�H2O��Al��OH ��Al(OH)3��NO
��Al(OH)3��NO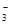 ��N2���뽫�����ӷֱ��������¿ո��ڡ�
��N2���뽫�����ӷֱ��������¿ո��ڡ�
NO3��+ + + +
�÷�Ӧ�����У��������뱻��ԭ��Ԫ�ص����ʵ���֮��Ϊ ��
��2���ҹ��״��ĺ������Ժ�ˮΪ�������Һ������ܷ�ӦΪ��4Al+3O2+6H2O=
4Al(OH)3���������ϲ����˲��������ò���Ϊ�������ŵ��� ��
��3����֪��4Al(s)+3O2(g)=2Al2O3(g) ��H=��2834.9kJ/mol
Fe2O3(s)+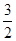 C(s)=
C(s)=
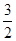 CO2(g)+2Fe(s)
��H=+234.1kJ/mol
CO2(g)+2Fe(s)
��H=+234.1kJ/mol
C(s)+O2(g)=CO2(g) ��H=��393.5kJ/mol
д�������������������ȷ�Ӧ���Ȼ�ѧ����ʽ ��
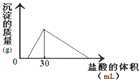
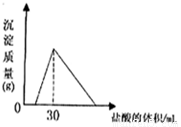
��4����һ�������������Ͻ�����ˮ�У��Ͻ�ȫ���ܽ⣬�õ�20mL pH=14����Һ��Ȼ��2mol/L����ζ����ɵó������������ĵ����������ϵ����ͼ����Ͻ������Ϊ �ˡ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com