
【题目】以炼锌厂的烟道灰![]() 主要成分为ZnO,另含少量
主要成分为ZnO,另含少量![]() 、CuO、
、CuO、![]() 、MnO等
、MnO等![]() 为原料可生产草酸锌晶体ZnSO4·2H2O,摩尔质量为189g/mol。
为原料可生产草酸锌晶体ZnSO4·2H2O,摩尔质量为189g/mol。

有关氢氧化物开始沉淀和沉淀完全的pH如下表:
氢氧化物 |
|
|
|
|
开始沉淀的pH |
|
|
|
|
沉淀完全的pH |
|
|
|
|
请问答下列问题:
(1)滤渣A的主要成分为_________,滤渣B的主要成分为_______________。
(2)除锰过程中产生![]() 沉淀的离子方程式为_______________________。
沉淀的离子方程式为_______________________。
(3) ①除铁![]() 部分
部分![]() 可能被除去
可能被除去![]() 时加入ZnO控制反应液pH的范围为______________。
时加入ZnO控制反应液pH的范围为______________。
②若某溶液中含有![]() ,可能含有
,可能含有![]() ,请设计实验证明
,请设计实验证明![]() 的存在。________。
的存在。________。
(4)沉淀后要获得干燥纯净草酸锌晶体,需进行的操作是_______________。
(5)将草酸锌晶体加热分解可得到一种纳米材料。加热过程中固体残留率随温度的变化如图所示,![]() 范围内,发生反应的化学方程式为_________________。
范围内,发生反应的化学方程式为_________________。

【答案】![]()
![]()
![]()
![]() 取少量此溶液于试管中,滴加几滴酸性高锰酸钾溶液,若
取少量此溶液于试管中,滴加几滴酸性高锰酸钾溶液,若![]() 紫
紫![]() 红色褪去,则此溶液含有
红色褪去,则此溶液含有![]() 过滤、洗涤、干燥
过滤、洗涤、干燥![]() 或烘干
或烘干![]()
![]()
![]()
【解析】
![]() 与盐酸不反应,用盐酸酸浸时
与盐酸不反应,用盐酸酸浸时![]() 不溶解,过滤分离,滤渣A为
不溶解,过滤分离,滤渣A为![]() ,滤液中加入过氧化氢进行除锰,再通过调节溶液pH,使
,滤液中加入过氧化氢进行除锰,再通过调节溶液pH,使![]() 转化为
转化为![]() 沉淀,过滤分离,滤渣B为
沉淀,过滤分离,滤渣B为![]() 滤液中再加入ZnS,
滤液中再加入ZnS,![]() 转化为CuS沉淀,过滤除去CuS,滤液为氯化锌,加入草酸铵得到草酸锌晶体,最终的滤液中含有氯化铵等。
转化为CuS沉淀,过滤除去CuS,滤液为氯化锌,加入草酸铵得到草酸锌晶体,最终的滤液中含有氯化铵等。
(1)据以上分析可知,滤渣A为SiO2,滤渣B为Fe(OH)3,故答案为:, SiO2;Fe(OH)3;
(2)除锰过程中,酸性条件下,锰离子与双氧水发生氧化还原反应生成![]() 沉淀,反应离子方程式为:
沉淀,反应离子方程式为:![]() ,故答案为:
,故答案为:![]() ;
;
(3) ①除铁![]() 部分
部分![]() 可能被除去
可能被除去![]() 时加入ZnO控制pH使铁离子沉淀完全,而
时加入ZnO控制pH使铁离子沉淀完全,而![]() 不能沉淀,故控制反应液pH的范围为
不能沉淀,故控制反应液pH的范围为![]() ,故答案为:
,故答案为:![]() ;
;
②有![]() 具有还原性可以被酸性高锰酸钾溶液氧化,所以酸性高锰酸钾紫色褪去,故答案为:取少量此溶液于试管中,滴加几滴酸性高锰酸钾溶液,若
具有还原性可以被酸性高锰酸钾溶液氧化,所以酸性高锰酸钾紫色褪去,故答案为:取少量此溶液于试管中,滴加几滴酸性高锰酸钾溶液,若![]() 紫
紫![]() 红色褪去,则此溶液含有
红色褪去,则此溶液含有![]() ;
;
(4)沉淀后的滤液溶质是草酸锌,经过过滤、洗涤、干燥,即可制得草酸锌晶体,故答案为:过滤、洗涤、干燥![]() 或烘干
或烘干![]() ;
;
(5)草酸锌晶体中的![]() 质量分数为
质量分数为![]() ,故A点完全失去结晶水,化学式为
,故A点完全失去结晶水,化学式为![]() ,假设B点为ZnO,则残留固体占有的质量分数为
,假设B点为ZnO,则残留固体占有的质量分数为![]() ,故B点残留固体为ZnO,结合原子守恒可知还生成等物质的量的CO与
,故B点残留固体为ZnO,结合原子守恒可知还生成等物质的量的CO与![]() ;
;![]() 范围内,则发生反应的化学方程式为:
范围内,则发生反应的化学方程式为:![]()
![]() ;故答案为:
;故答案为:![]()
![]() 。
。


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
【题目】钼![]() 最重要的用途是作为铁合金的添加剂,用CO还原
最重要的用途是作为铁合金的添加剂,用CO还原![]() 制备单质Mo的装置如图所示
制备单质Mo的装置如图所示![]() 尾气处理装置已省略
尾气处理装置已省略![]() 下列说法正确的是
下列说法正确的是![]()
![]()
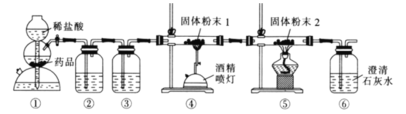
A.装置![]() 中的药品为石灰石粉末
中的药品为石灰石粉末
B.装置![]() 中盛有饱和碳酸氢钠溶液,
中盛有饱和碳酸氢钠溶液,![]() 中盛有澄清石灰水
中盛有澄清石灰水
C.在装置![]() 中生成了钼单质
中生成了钼单质
D.![]() 中溶液变浑浊,说明产生的
中溶液变浑浊,说明产生的![]() 一定是来自
一定是来自![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学研究性学习小组利用以下装置制取并探究氨气的性质。在A装置中发生反应的化学方程式为2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O。
CaCl2+2NH3↑+2H2O。
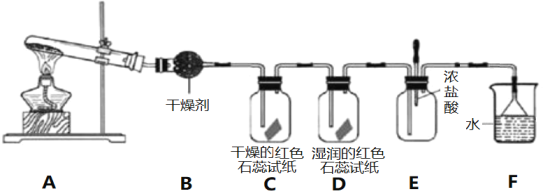
(1)B装置中的干燥剂是_________________(填“碱石灰”或“浓硫酸”)。
(2)C、D装置中试纸颜色会发生变化的是___________(填”C”或“D”)。
(3)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1-2滴浓盐酸,可观察到E装置中的现象是产生_____________(填”白烟”或“白雾”)。
(4)烧杯F中水的作用是________________________。
(5)欲制得标准状况下11.2 LNH3,至少需要Ca(OH)2的质量为____________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组拟实验探究锡及锡的化合物的部分性质。经查阅资料知:Sn的熔点为![]() ;
;![]() 易被氧化,且易水解;
易被氧化,且易水解;![]() 常温下易分解,
常温下易分解,![]() 常温下为无色液体,熔点为
常温下为无色液体,熔点为![]() ,沸点为
,沸点为![]() ,回答下列问题:
,回答下列问题:
(1)该小组用以下流程制备![]() 晶体:
晶体:
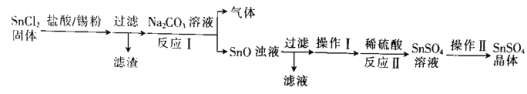
![]() 加入锡粉的作用为______________________________________。
加入锡粉的作用为______________________________________。
![]() 反应Ⅰ的离子方程式为______________________________。
反应Ⅰ的离子方程式为______________________________。
![]() 操作Ⅰ为沉淀的洗涤,请简述如何判断沉淀是否洗涤干净:_____________________。
操作Ⅰ为沉淀的洗涤,请简述如何判断沉淀是否洗涤干净:_____________________。
(2)用熔融的锡与干燥的氯气制备![]() ,实验装置如下:
,实验装置如下:
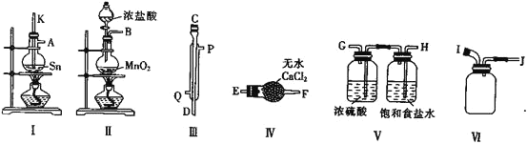
![]() 装置Ⅲ为冷凝管,则水流从__________
装置Ⅲ为冷凝管,则水流从__________![]() 填“Q”或“P”
填“Q”或“P”![]() 口进入。
口进入。
![]() 请用大写英文字母表示的接口按从左到右顺序组装仪器:__________________________。
请用大写英文字母表示的接口按从左到右顺序组装仪器:__________________________。
![]() 整个装置存在的不足之处为_________________________。
整个装置存在的不足之处为_________________________。
(3)该小组通过下列方法测定所用锡粉的纯度:取产品![]() 溶于稀硫酸中,加入过量的
溶于稀硫酸中,加入过量的![]() 溶液,再用
溶液,再用![]() 的
的![]() 溶液滴定
溶液滴定![]() ,消耗
,消耗![]() 溶液
溶液![]() 。已知
。已知![]() ,
,![]() ,
,![]() 。则锡粉的质量分数为
。则锡粉的质量分数为![]() 杂质不参与反应
杂质不参与反应![]() ______________
______________![]() 结果保留三位有效数字
结果保留三位有效数字![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近我国成功研制出高效电催化固氮催化剂Mo2N,如图所示,在0.1mol·L-1盐酸溶液中,在一定电压下具有较高的产氨速率和稳定的电流效率。下列判断错误的是
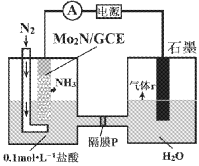
A. 石墨电极为阳极
B. P为阳离子交换膜
C. Mo2N/GCE电极区反应式为N2+6H++6e-=2NH3
D. 为提高溶液的导电性,可在石墨电极区加入适量的盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,pH=2的盐酸和醋酸各1mL分别加水稀释,pH随溶液体积变化的曲线如下图所示。下列说法不正确的是( )

A. 曲线Ⅰ代表盐酸的稀释过程 B. a溶液的导电性比c溶液的导电性强
C. a溶液中和氢氧化钠的能力强于b溶液 D. 将a、b两溶液加热至30℃, 变小
变小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)NH4Cl溶液显_________性,用离子方程式表示原因____________,其溶液中离子浓度大小顺序为_______________________________________。
(2)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH-)=________ ,在pH=3的CH3COOH溶液中,水电离出来的c(H+)=_________________。
(3)若将等pH、等体积的NaOH和NH3·H2O分别加水稀释m倍、n倍,稀释后两种溶液的pH仍相等,则m__________n(填“<”、“>”或“=”)。
(4)物质的量浓度相同的NaCl;NaOH;HCl;④NH4Cl;⑤CH3COONa 5种溶液按pH由大到小的顺序为(用④⑤代表相应溶液):_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水四氯化锡常用作媒染剂和有机合成中的氯化催化剂。实验室可用熔融的锡![]() 熔点
熔点![]() 与
与![]() 反应制备
反应制备![]() ,装置如图。
,装置如图。
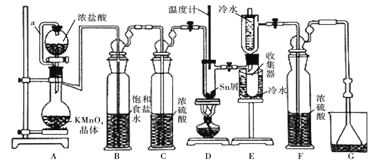
已知:![]() 、
、![]() 有关物理性质:
有关物理性质:
物质 | 颜色、状态 | 熔点/℃ | 沸点/℃ |
SnCl2 | 无色晶体 | 246 | 652 |
SnCl4 | 无色液体 | -33 | 114 |
![]() 极易水解生成
极易水解生成![]() 。回答下列问题:
。回答下列问题:
(1)导管a的作用是____________,装置A中发生反应的离子方程式为____________________。
(2)当观察到装置F液面上方___________时才开始点燃D处的酒精灯,待锡熔化后适当增大氯气流量,继续加热。此时继续加热的目的是![]() ________;
________;![]() ______
______
(3)若上述装置中缺少装置![]() 其它均相同
其它均相同![]() ,则D处具支试管中发生的主要副反应化学方程式为_________________________________。
,则D处具支试管中发生的主要副反应化学方程式为_________________________________。
(4)![]() 和锡的反应产物有
和锡的反应产物有和
![]() ,为防止产品中带入过多的
,为防止产品中带入过多的![]() ,可采取的措施是____________________________________________。
,可采取的措施是____________________________________________。
(5)滴定分析产品中2价![]() Ⅱ
Ⅱ![]() 的含量:用分析天平称取
的含量:用分析天平称取![]() 产品于锥形瓶中,用蒸馏水溶解,加入淀粉溶液,用
产品于锥形瓶中,用蒸馏水溶解,加入淀粉溶液,用![]() 的碘标准溶液滴定至终点时消耗
的碘标准溶液滴定至终点时消耗![]() ,则产品中
,则产品中![]() Ⅱ
Ⅱ![]() 的质量分数为___________。
的质量分数为___________。![]() 小数点后保留2位,已知
小数点后保留2位,已知![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X是某金属单质,X、A、B、C含同一种元素,可发生如下转化:
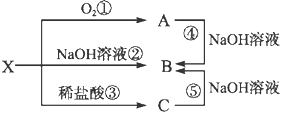
(1)写出以下反应的离子方程式:
②___________________________;
④___________________________。
(2)确定化学式B_______ X_______
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com