
下列说法正确的是
A.需加热才能发生的反应一定是吸热反应
B.任何放热反应在常温条件一定能发生反应
C.反应物和生成物分别具有的总能量的相对大小决定了反应是放热反应还是吸热反应
D.当△H<0时表明反应为吸热反应
科目:高中化学 来源:2014-2015学年吉林延边州汪清六中上第一次月考高一化学试卷(解析版) 题型:选择题
(6分)实验室有如下仪器①试管②烧杯③量筒④蒸发皿⑤锥形瓶⑥分流漏斗⑦蒸馏烧瓶,回答下列问题:
(1)可以直接加热的有 (填序号,下同);
(2)加热时必须垫上石棉网的有 ;
(3)使用前必须查漏的有 .
查看答案和解析>>
科目:高中化学 来源:2014-2015学年吉林公主岭市高一上学期第一次月考化学试卷(解析版) 题型:选择题
下列说法中正确的是( )
A.纯净物一定由分子组成 B.由同种分子构成的物质一定是纯净物
C.混合物一定是由两种以上元素构成的 D.含有氧元素的化合物都是氧化物
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市高二上第一次质量检测化学试卷(解析版) 题型:选择题
氢气、一氧化碳、葡萄糖、甲烷燃烧的热化学方程式分别为
H2(g)+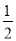 O2(g) = H2O(l) ΔH=-285.8 kJ·mol-1
O2(g) = H2O(l) ΔH=-285.8 kJ·mol-1
CO(g)+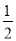 O2(g) = CO2(g) ΔH=-283.0 kJ·mol-1
O2(g) = CO2(g) ΔH=-283.0 kJ·mol-1
C6H12O6(s) +6O2(g)=6CO2(g)+6H2O(l) △H=―2800 kJ/mol
CH4(g)+2O2(g) = CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1
相同质量的氢气、一氧化碳、辛烷、甲烷完全燃烧时,放出热量最多的是
A.C6H12O6 B.CH4 C.H2 D.CO
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市高二上第一次质量检测化学试卷(解析版) 题型:选择题
硫代硫酸钠(Na2S2O3)与稀H2SO4溶液时发生如下反应:
Na2S2O3+ H2SO4=Na2 SO4+SO2+S↓+H2O 下列反应速率最大的是
A.0.1mol/L Na2S2O3和0.1mol/L H2SO4溶液各5mL,加水5mL,反应温度10℃
B.0.1mol/L Na2S2O3和0.1mol/L H2SO4溶液各5mL,加水10mL,反应温度10℃
C.0.1mol/L Na2S2O3和0.1mol/L H2SO4溶液各5mL,加水10mL,反应温度30℃
D.0.2mol/L Na2S2O3和0.1mol/L H2SO4溶液各5mL,加水10mL,反应温度30℃
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市高一上第一次质量检测化学试卷(解析版) 题型:填空题
将6.50g锌投入200mL某浓度的盐酸中,锌和盐酸恰好完全反应。求:
(1)所用盐酸中HCl的物质的量浓度c(HCl)= ;
(2)反应中生成的H2在标准状况下的体积V(H2)= 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市高一上第一次质量检测化学试卷(解析版) 题型:选择题
取物质的量浓度为0.05 mol·L-1的金属氯化物(RClx) 溶液20 mL,使之恰好与20 mL 0.15 mol·L-1的AgNO3溶液完全反应。则该氯化物的化学式为( )
A.RCl B.RCl2 C.RCl3 D.RCl4
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省玉溪市高一上学期期中化学试卷(解析版) 题型:选择题
下列离子方程式中,正确的是
A.铁与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑
B.硫酸溶液中加入Ba(OH)2溶液:SO42- + Ba2+= BaSO4↓
C.用稀硫酸洗去铁锈:Fe2O3+6H+=2Fe3++3H2O
D.将铝片插入硝酸铜溶液中:Cu2++Al=Al3++Cu
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com