
����Ŀ��ij�����Ĺ�ҵ��ˮ�к��д�����FeSO4���϶��Cu2+��������Na+��Ϊ�˼�����Ⱦ�����Ϊ���������ƻ��Ӹù�ҵ��ˮ�л������������ͽ���ͭ�����������ͼ���ش�����������

��1��д����Ӧ���ʵĻ�ѧʽ����Ϊ________________________����Ϊ_____________________________��A�к��е�����____________________��
��2��������������Ϊ__________________��
��3��ĸҺ�к��е�������Ҫ�У������ӷ��ţ���__________________��
��4�������۰���_______________________________���ˣ��پ�ϴ�ӡ�����������Եõ�������FeSO47H2O���壬��
��5�������������У��漰�������ӷ���ʽ��______________________________________________��
���𰸡�Fe H2SO4 Fe��Cu ���� Fe2+ ![]() ������Ũ������ȴ�ᾧ Fe+Cu2+=Fe2++Cu Fe+2H+=Fe2++H2��
������Ũ������ȴ�ᾧ Fe+Cu2+=Fe2++Cu Fe+2H+=Fe2++H2��
��������
�������̵�Ŀ�ģ��Ʊ�FeSO4��7H2O��Cu����ˢټ��������Ϊ������Fe������Fe��Cu2��=Fe2����Cu��Ȼ����ˣ���������Ϊ���ˣ�AΪCu��Fe�Ļ���CΪFeSO4��Һ���ڼ������ᣬ����Fe��H2SO4=FeSO4��H2����Ȼ����ˣ���������Ϊ���ˣ�BΪFeSO4��H2SO4�Ļ��Һ��B��C��ϣ�Ȼ������Ũ������ȴ�ᾧ�ķ����õ�FeSO4��7H2O��
��1������������������ΪFe����ΪH2SO4��A�к��е�������Fe��Cu��
��2�������ڵ�����Ϊ���ˣ�
��3����������������ĸҺ�к��е�������Fe2����SO42����������H����
��4����Ϊ�õ�FeSO4��7H2O�������Ҫ����Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ�������Եõ�FeSO4��7H2O��
��5���������������������ķ�ӦʽFe��Cu2��=Fe2����Cu��Fe��2H��=Fe2����H2����


 �ǻ�С��ϰϵ�д�
�ǻ�С��ϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������0.1mol/L��H2A��Һ��H2A��HA-��A2- ��������ռ���ʵ���������pH�仯�Ĺ�ϵ��ͼ��ʾ.���б�����ȷ����( )
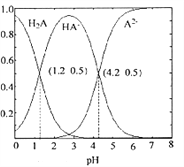
A. �ں�H2A��HA-��A2-����Һ�У�ͨ������HCl,HA-�����ʵ�������һ�����
B. �������ʵ�����NaHA��Na2A����ˮ�У�������Һ�д��ڣ�c(Na+)+c(H+)=c(HA-)+c(A2-)+c(OH-)
C. �� 0.1mol/L NaHA ��Һ�У�������Ũ�ȴ�С��ϵΪ��
c(Na+)��c(HA-)��c(H+)��c(A2-)��c(OH-)
D. �������ʵ�����NaHA��Na2A����ˮ�У�������ҺpHǡ��Ϊ4.2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ˮ���ڷ��ú�����������Һ�в����ٵ��ǣ� ��
A.HClO
B.Cl��
C.Cl2
D.ClO��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪ��ˮ����CO2������̼ѭ����ԭ��ʾ��ͼ������˵���������

A. ����ϡ�������̫����ת��Ϊ��ѧ��
B. �ƻ����ͷ�CO2�ķ�ӦΪ��2 NaHCO3+CaCl2==CaCO3��+CO2��+2NaCl+H2O
C. ���յ�CO2��ƻ����ͷŵ�CO2�������
D. ��̼ѭ���н�CO2ת��Ϊ������л���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��pH��12��NaOH��Һ��pH��10��NaOH��Һ�������Ϻ���Һ��
A. pH��11 B. pH��10.3
C. c(H��)��2��10��12mol/L D. c(H��)��5��10��11mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ����������Ӧ���ٶ�������������Ͷ�����̼�����ʵ��ŷ�����
��1����CH4����ԭúȼ�ղ����ĵ����������������Ⱦ��
��֪��CH4(g) + 2NO2(g)��N2(g) +CO2(g) + 2H2O(g) ��H��-867.0 kJ/mol
NO2(g)��![]() N2O4(g) ��H��-28.5 kJ/mol
N2O4(g) ��H��-28.5 kJ/mol
д��CH4����ԭN2O4(g)����CO2��N2��H2O(g)���Ȼ�ѧ����ʽ ��
��2��һ�������£���NO2��SO2�������1��2���ں��º��ݵ��ܱ������У�����NO2(g)+SO2(g)![]() SO3(g)+NO(g)����÷�Ӧ�ﵽƽ��ʱNO2��SO2�����Ϊ1��5����ƽ�ⳣ��K�� ������ֵ����
SO3(g)+NO(g)����÷�Ӧ�ﵽƽ��ʱNO2��SO2�����Ϊ1��5����ƽ�ⳣ��K�� ������ֵ����
��3����ͼ1��һ����NH3��O2�ѳ�������NO��ԭ������ԭ����NO����ת��ΪH2O�� ���ѧʽ����������1mol NH3��0.5molO2ʱ����ȥ��NO�ڱ�״���µ����Ϊ L��

��4���о�CO2�ں����е�ת�ƺ��ޣ��ǵ������ѧ�о���ǰ��������������ͼ2��ʾװ��(��Ϊ���Ե缫)�Ӻ�ˮ����ȡCO2����ˮ����̼95 % ��HCO3�����ڣ��������ڼ��ٻ������������庬����
��a�ҵĵ缫��ӦʽΪ ��
��b������ȡCO2�ķ�Ӧ�����ӷ���ʽΪ ��
��b���ų��ĺ�ˮ��pH<6������ֱ���Żش����ø�װ���в��������ʶ�b���ų��ĺ�ˮ���д������ϸ������Żش������ķ����� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������̼ͬԭ������������ϩ����Ȳ�����ֱ�ȡ���������������ڿ�������ȫȼ�����ɶ�����̼��ˮ����Ҫ�������ıȽ�����ȷ��
A. ������� B. ϩ����� C. Ȳ����� D. ����һ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������������LED��Ƭ��һ�ַ�������ܡ��������Ϊ��GaAs(�黯��)��AlGaInP(��������)��GaInN(��������)�ȡ���ش��������⣺
��1�����̬ԭ�ӵĺ�������Ų�ʽΪ______________________��
��2�������ǽ���Ԫ���⻯��ķе�Ӹߵ��͵�˳��Ϊ___________��
��3������˵����ȷ����___________
a���縺�ԣ�As<Ga b��SiC��GaAs��Ϊ�ȵ����� c����һ�����ܣ�As>Se>Ga
��4����ͼ��ʾΪGaAs�ľ����ṹ�������۵�Ϊ1237�档
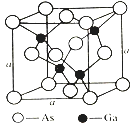
��������������ԭ�Ӽ�Ļ�ѧ��������___________��
��һ����ԭ����Χ���о����������ȵ���ԭ���γɵĿռ乹����___________��
��һ�����������Ϊ___________��
����֪�����ⳤa=5.64��10-10m����þ����ܶ�Ϊ��=___________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com