


���� ��1����������ͼ�����ʵ�ѭ�����ж�ѭ��ʹ�õ����ʣ��������ճآ���������NO��CO2��SO2��ϳ�����������NP����ȷ�����յ����壻
��2��������������Ӵ��ڵ���ƽ�⣬�����Ȼ��ƣ������ӻ�Ӱ�컯ѧƽ����ƶ�������ƽ���ƶ�ԭ�������ͣ�
��3�����ݵ��صĹ���ԭ������������Ce3+ʧ���ӵ�������Ӧ����������HSO3-�õ��ӵĻ�ԭ��Ӧ���ݴ���д���ԭ������ʽ��
��4����֪��N2��g��+O2��g��=2NO��g����H=+179.5kJ/mol
��2NO��g��+O2��g��=2NO2��g����H=-112.3kJ/mol
298k������1mol NO2��1mol CO��Ӧ����1mol CO2��1mol NO���Ȼ�ѧ����ʽΪ��2NO2��g��+4CO��g��=N2��g��+4CO2��g����H=-��368-134��KJ/mol=-234KJ/mol��
�ɸ�˹���ɣ���-��+�ۣ���2�õ���Ӧ���Ȼ�ѧ����ʽ��2NO��g��+2CO��g��?N2��g��+2CO2��g�������ݸ�˹���ɼ����ʱ䣻
��5������NԪ���غ㣬�ҵ���������ӡ�������������Լ������֮��Ĺ�ϵ�����ݵ����غ㣬�õ�Ce3+��Ce4+��S2O32-֮��Ĺ�ϵ�����м��㼴�ɣ�
��� �⣺��1����������ͼ�����ʵ�ѭ�����õ�ѭ��ʹ�õ��������Ҵ�����Ce4+���������ճآ���������NO��CO2��SO2��������������NO��ȷ�����յ�������CO2��SO2��
�ʴ�Ϊ���Ҵ�����Ce4+��CO2��SO2��
��2��HSO3-��Һ�д��ڵ���ƽ�⣺HSO3-?H++SO32-�������Ȼ����Ժ����ӻ�������������Ӳ�������Ƴ��������µ���ƽ�������ƶ���������Ũ������������ҺpH���ͣ��ʴ�Ϊ��HSO3-��Һ�д��ڵ���ƽ�⣺HSO3-?H++SO32-�������Ȼ����Ժ����ӻ�������������Ӳ�������Ƴ��������µ���ƽ�������ƶ���������Ũ������������ҺpH���ͣ�
��3�����ݵ��صĹ���ԭ������������Ce3+ʧ���ӵ�������Ӧ����������HSO3-�õ��ӵĻ�ԭ��Ӧ�����ԭ������ʽΪ��4Ce3++2HSO3-+4H+$\frac{\underline{\;ͨ��\;}}{\;}$4Ce4++2S2O32-+3H2O��
��4����֪��N2��g��+O2��g��=2NO��g����H=+179.5kJ/mol
��2NO��g��+O2��g��=2NO2��g����H=-112.3kJ/mol
298k������1mol NO2��1mol CO��Ӧ����1mol CO2��1mol NO���Ȼ�ѧ����ʽΪ��2NO2��g��+4CO��g��=N2��g��+4CO2��g����H=-��368-134��KJ/mol=-234KJ/mol��
�ɸ�˹���ɣ���-��+�ۣ���2�õ���Ӧ���Ȼ�ѧ����ʽ��2NO��g��+2CO��g��?N2��g��+2CO2��g����H=-759.8KJ/mol��
�ʴ�Ϊ��2NO��g��+2CO��g��?N2��g��+2CO2��g����H=-759.8KJ/mol��
��5��������������ӡ���������ӵ����ʵ����ֱ���m��n���Ӣ�����������泥�����NԪ���غ㣬�õ���m+n=$\frac{x��1000}{80}$��4Ce3++2HSO3-+4H+$\frac{\underline{\;ͨ��\;}}{\;}$4Ce4++2S2O32-+3H2O����ϵ���ת�ƹ�ϵ���õ�4Ce3+��2HSO3-��2S2O32-��4Ce4+��NO��NO2-��e-��NO��NO3-��e-�����ݵ����غ㣬�õ�m+3n=n��Ce4+��=4n��S2O32-�������Եõ���m+3n=4cy��1000�������٢ڽ��m=$\frac{75x}{4}$-2000cy�����ݷ�Ӧ2NH3+2H++O2+2NO2-=2NH4NO3���õ�n��O2��=$\frac{1}{2}$n��NO2-��=$\frac{75x}{8}$-1000cy��
���������V=22.4��$\frac{75x}{8}$-1000cy����10-3m3=0.21x-22.4cy���ʴ�Ϊ��0.21x-22.4cy��
���� ����Ŀһ�������̵ķ�ʽ�������йص绯ѧ���Ȼ�ѧ��������ԭ��Ӧ�Լ������غ���йؼ���֪ʶ���ۺ���ǿ���Ѷȴ�


 ���Ž�������С״Ԫϵ�д�
���Ž�������С״Ԫϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ۡ���֬�������ᶼ��ˮ�⣬��ˮ����ﲻͬ | |
| B�� | SO2���������ԣ���˿�����Ư��ֽ�� | |
| C�� | ֲ���ͺ��ѻ����Ͷ���ʹ��ˮ��ɫ | |
| D�� | �ԡ��ع��͡����з�������Ƶ����͡�ú�ͣ��ﵽ���Ϊ����Ŀ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Xֻ��1�ֽṹ | |
| B�� | ������Ϣ�ؿ�����ϩ������ʹ��ˮ��ɫ | |
| C�� | ����������ӦʽΪ��C21H41COOH+X+2H2O-2e-��C23H46+2CO32-+6H+ | |
| D�� | �����Ļ�ԭ����ΪH2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������ܵ�������Ҫ�����¼��ַ�ʽ��ֱ��ȼ�ա����ﻯѧת�����Ȼ�ѧת�� | |
| B�� | �������о������۽ṹ�Ĺ����У���ѧ����������������ɨ�������������ֲ�ͬ��εĹ۲������Ⱥ�õ���ʹ�� | |
| C�� | ��Դ�ɷ�Ϊһ����Դ�Ͷ�����Դ����ѧ��ԴҲ�ɷ�Ϊһ�ε�غͶ��ε�� | |
| D�� | ��ײ���ۺ���̬�����dz��õķ�Ӧ�������ۣ����й���̬���ۿɽ����¶ȡ������ȶԷ�Ӧ���ʵ�Ӱ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

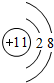 ���Ļ�ѧʽNa2S2O4
���Ļ�ѧʽNa2S2O4�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 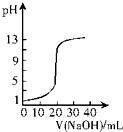 ��ͼ��ʾ0.10 mol•L-1 NaOH��Һ�ζ�20.00 mL 0.10 mol•L-1������Һ�ĵζ����� | |
| B�� | 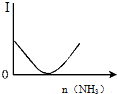 ��ͼ��ʾ������Һ��ͨ�백����������������Һ������I�ı仯 | |
| C�� | 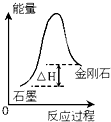 ������ͼ��ʾ��֪��ʯī�Ƚ��ʯ�ȶ� | |
| D�� | 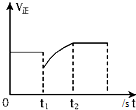 ��ͼ��ʾ��Ӧ2SO2+O2?2SO3��t1ʱ��ֻ��С��SO3��Ũ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ʽ��ȶ�������Ȼ���д�������̬�Ĺ� | |
| B�� | �մɡ�ˮ�ࡢ���������ɰ��Ϊ��ͳ���ǽ������� | |
| C�� | ˮ�ࡢ��ͨ�������Ʊ���Ҫ�õ�ʯ��ʯ | |
| D�� | �ߴ��ȵĶ�������㷺�����������ά�����ά��ǿ����Һ��Ӱ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Al��Cu��ϡH2SO4���ԭ��أ��为����ӦʽΪ��Al-3e-=Al3+ | |
| B�� | ��Mg��Al��NaOH��Һ���ԭ��أ��为����ӦʽΪ��Al-3e-+4OH-=AlO2-+2H2O | |
| C�� | ��Al��Cu��Ũ�������ԭ��أ��为����ӦʽΪ��Cu-2e-=Cu2+ | |
| D�� | ��Al��Cu��FeCl3��Һ���ԭ��أ��为����ӦʽΪ��Cu-2e-=Cu2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���Ӿ��� | NaCl | KCl | CaO |
| ������/kJ•mol-1 | 786 | 715 | 3401 |
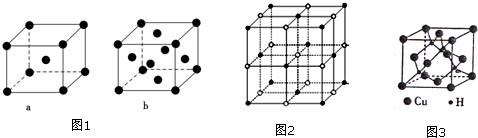
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com