
(6分)某些化学反应可用表示(未配平):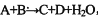 ;请回答下列问题:
;请回答下列问题:
(1)若A、C、D均含有氯元素,且A中氯元素的化合价介于C与D之间,写出该反应的离子方程式:_________________________________________________。
(2)若A为紫红色金属,D为无色刺激性气体,请写出符合上式的化学方程式:______________________________________________________________。
(3)若C、D均为气体(其中C有颜色)且分子具有相同的原子个数比,则符合上式化学方程式是:_____________________________________________________。
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:单选题
固体X只可能由A1、(NH4)2SO4 ,MgCl2.FeCl2, AlCl3, AgN03中的一种或几种组成,某同学对该固体进行了如下实验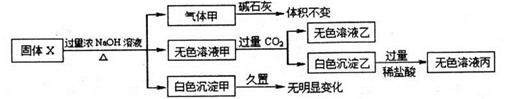
下列判断正确的是:
| A.气体甲一定是纯挣物 |
| B.白色沉淀甲可能是混合物 |
| C.固体X中一定存在AlCl3、(NH4)2SO4, MgCl2 |
| D.固体X中一定不存在FeCl2、AgNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某些化学反应可用下式表示 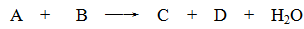
请回答下列问题:
(1)若A、C、D均含有氯元素,且A的化合价介于C与D之间,写出该反应的离子方程式: 。
(2)若C、D均为气体且都能使澄清石灰水变浑浊,则A与B的组合是 。
(3)若A、C均含有铝元素。①当B是盐酸时,C是 ;②当B是NaOH时,C是 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
有关元素X、Y、Z、D、E的信息如下:
| | 有关信息 |
| X | 元素主要化合价为-2,原子半径为0.074 nm |
| Y | 所在主族序数与所在周期序数之差为4 |
| Z | 原子半径为0.102 nm,其单质在X的单质中燃烧,发出明亮的蓝紫色火焰 |
| D | 最高价氧化物对应的水化物可溶于水,且能电离出电子数相等的阴、阳离子 |
| E | 单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某固体混合物可能由Al、(NH4)2SO4、MgCl2、AlCl3、FeCl2中的一种或几种组成,现对该混合物做如下实验,所得现象和有关数据如图所示(气体体积数据已换算成标准状况下的体积):
回答下列问题:(1)混合物中是否存在FeCl2:____________(填“是”或“否”)。
(2)混合物中是否存在(NH4)2SO4:____________(填“是”或“否”)。
(3)写出反应⑤的离子方程式:________________________。
(4)请根据图中数据分析,原固体混合物的成分为 (写化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
除去下列物质中的杂质(括号内代表杂质),请写出相应的实验方法或试剂名称及有关反应的化学方程式。
(1)NaCl溶液(Na2CO3) 试剂____________,反应的化学方程式__________________________;
(2)NaHCO3溶液(Na2CO3) 试剂____________,反应的化学方程式___________________________;(3)Na2CO3固体(NaHCO3) 实验方法____________,反应的化学方程式_____________________;
(4)铁粉(铝粉)试剂______________,反应的化学方程式__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
喷泉是一种常见的实验现象(如下图),其产生原因是存在压强差。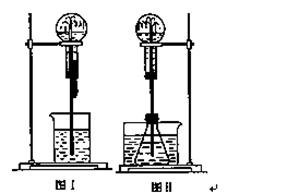
(1)图Ⅰ为化学教学中所用的喷泉实验装置。在烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有液体。下列组合中不可能形成喷泉的是(填编号字母) 。
A.HCl 和H2O B.O2和H2O
C.SO2和NaOH溶液 D.CO2和NaOH溶液
(2)某学生积极思考产生喷泉的其他办法,并设计了图Ⅱ所示的 装置。
在图Ⅱ的锥形瓶中,分别加入足量的下列物质,反应后可能产生 喷泉的是(填编号字母) 。
A.CaCO3和稀H2SO4 B.NaOH与稀HCl
C.Zn与稀HCl D.NaCl与稀HNO3
(3)比较图Ⅰ和图Ⅱ两套装置,从产生喷泉的原理分析,二者的不同点在于 。
(4)城市中常见的人造喷泉及火山爆发的原理与上述(填“图Ⅰ”或“图Ⅱ”)装置的原理相似。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
甲、乙、丙、丁四种物质中,甲、乙、丙均含有某种相同的元素,它们之间具有如下转化关系(反应条件和部分产物已略去):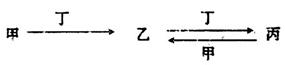
(1)若甲为常见金属单质,甲和丁的稀溶液反应生成无色气体,该气体遇空气变为红棕色。
①检验丙溶液中金属阳离子的试剂为________(填试剂名称)。
②向含n mol丁的稀溶液中加入m mol单质甲,二者恰好完全反应(假设还原产物只有上述无色气体),则n:m可能为__________(填代号)。
a.3:2 b.4:1 c.5:1 d.3:1
③常温下,丁的浓溶液可存放于甲制作的容器中,其原因是________________。
(2)若甲为氯碱工业的产品,含丙的某种药品可用于治疗胃酸过多。
①鉴别等浓度的乙溶液和丙溶液,可选用的试剂为________(填代号)
a.NaOH溶液 b.CaC12溶液 c.稀硫酸 d.澄清石灰水
②将甲、乙、丙三种溶液混合,向混合液中逐滴加入一定浓度的盐酸,生成气体的体积(标准状况)与加入盐酸的体积关系如下图所示: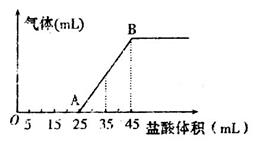
写出OA段所发生反应的离子方程式__________________________,当加入35mL盐酸时,产生气体的体积为22.4mL(标准状况),则盐酸的物质的量浓度为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
 下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中正确的是
下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中正确的是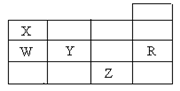
| A.常压下五种元素的单质中,Z单质的沸点最高 |
| B.Y、Z的阴离子电子层结构都与R原子的相同 |
| C.W的氢化物比X的氢化物稳定 |
| D.Y元素最高价氧化物对应水化物比W元素的最高价氧化物对应水化物的酸性强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com