
| A、新制碱性Cu(OH)2悬浊液 |
| B、FeCl3溶液 |
| C、BaCl2溶液 |
| D、酸性KMnO4溶液 |


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
 )互为同系物.
)互为同系物.
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、B的平均消耗速率为0.3mol/(L?min) |
| B、C的平衡浓度为2mol/L |
| C、平衡后,增大压强,平衡将向正方向移动 |
| D、若反应容器内气体的密度不再发生变化,说明反应已经达到平衡 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 近年来媒体多次报道了数起因食用有“瘦肉精”的猪肉和内脏,而发生急性中毒的恶性事件.这足以说明,目前由于奸商的违法经营,已使“瘦肉精”变成了“害人精”.“瘦肉精”的结构可表示为:下列关于“瘦肉精”的说法中正确的是( )
近年来媒体多次报道了数起因食用有“瘦肉精”的猪肉和内脏,而发生急性中毒的恶性事件.这足以说明,目前由于奸商的违法经营,已使“瘦肉精”变成了“害人精”.“瘦肉精”的结构可表示为:下列关于“瘦肉精”的说法中正确的是( )| A、属于芳香烃 |
| B、分子式为C12H19Cl3N2O |
| C、摩尔质量为313.5 g |
| D、不能发生消去反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
c(N
| ||
| c(NH3?H2O)c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
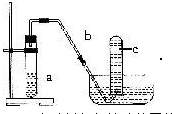
 实验室制取乙烯的装置如下图所示,请回答:
实验室制取乙烯的装置如下图所示,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com