
【题目】(1)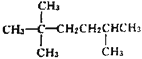 ,请用系统命名法对该物质进行命名:___。若该烃为一单烯烃的加成产物,则单烯烃可能有___种结构。
,请用系统命名法对该物质进行命名:___。若该烃为一单烯烃的加成产物,则单烯烃可能有___种结构。
(2)某含苯环的化合物A,其相对分子质量为104,碳的质量分数为92.3%,A的分子式为___。
(3)若25℃时CH3COOH的电离平衡常数Ka=1.8×10-5mol·L-1,向aLCH3COOH溶液中加入bmol CH3COONa,混合液恢复至25℃时呈中性,则原 CH3COOH溶液的物质的量浓度为____。
【答案】2,2,5-三甲基己烷 3 C8H8 ![]() mol/L
mol/L
【解析】
(1)根据烷烃的系统命名法,主链中含6个C,2,5号C上含甲基;该该烃为一单烯烃的加成产物,应该存在碳碳双键,根据碳碳双键可能存在的位置判断;
(2)根据相对分子质量和含碳量可计算含氢量,进而计算C、H原子数目,据此判断分子式;
(3)混合液呈中性,则c(H+)=c(OH-)=10-7mol/L,根据电荷守恒出c(CH3COO-),再结合电离平衡常数计算。
(1)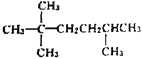 主链中含6个C,2、5号C上含甲基,则系统命名法命名为2,2,5-三甲基己烷;若该烃为一单烯烃的加成产物,该单烯烃结构中存在1个碳碳双键,碳碳双键存在3种可能的结构,分别为
主链中含6个C,2、5号C上含甲基,则系统命名法命名为2,2,5-三甲基己烷;若该烃为一单烯烃的加成产物,该单烯烃结构中存在1个碳碳双键,碳碳双键存在3种可能的结构,分别为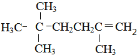 、
、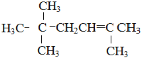 、
、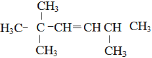 ,故答案为:2,2,5-三甲基己烷;3;
,故答案为:2,2,5-三甲基己烷;3;
(2)1molA中含有C、H的物质的量为:n(C)=![]() =8mol、n(H)=
=8mol、n(H)=![]() =8mol,则化合物A的分子式为C8H8,故答案为:C8H8;
=8mol,则化合物A的分子式为C8H8,故答案为:C8H8;
(3)向a L CH3COOH溶液中加入bmolCH3COONa,混合液恢复至25℃时呈中性,c(H+)=c(OH-)=10-7mol/L,电荷守恒得到c(Na+)+c(H+)=c(OH-)+c(CH3COO-),得到c(Na+)=c(CH3COO-)=![]() mol/L,Ka=1.8×10-5 molL-1=
mol/L,Ka=1.8×10-5 molL-1=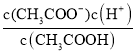 =
=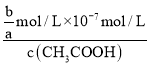 ,解得:c(CH3COOH)=
,解得:c(CH3COOH)=![]() mol/L,故答案为:
mol/L,故答案为:![]() mol/L。
mol/L。


科目:高中化学 来源: 题型:
【题目】在一定条件下发生反应 2SO3(g)![]() 2SO2(g)+O2(g),将2 mol SO3通入2 L容积恒定的密闭容器中,若维持容器内温度不变,5 min末测得SO3的物质的量为0.8 mol。则下列说法正确的是
2SO2(g)+O2(g),将2 mol SO3通入2 L容积恒定的密闭容器中,若维持容器内温度不变,5 min末测得SO3的物质的量为0.8 mol。则下列说法正确的是
A.若某时刻消耗了1 molSO3同时生成了0.5molO2,则表明该反应达到了平衡状态
B.若起始时充入3 mol SO3,起始时SO3分解速率不变
C.0~5min,SO2的生成速率v(SO2)=0.12mol·L-1·min-1
D.达到平衡时,SO2和SO3的浓度相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ·mol-1。回答有关中和反应的问题:
(1)用0.1molNaOH配成稀溶液与足量稀硝酸反应,放出_____热量。
(2)如图装置中缺少的一种玻璃仪器是___,碎泡沫塑料的作用____。
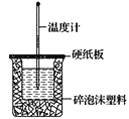
(3)若通过实验测定中和热的ΔH,其结果常常大于-57.3kJ·mol-1,其原因可能是____。
(4)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热ΔH会___(填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是实验室干馏煤的装置图,结合下图回答问题。
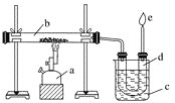
(1)指出图中仪器名称:a__________;b__________;c__________;d__________。
(2)装置c的作用是____________________________________,d中的液体有________和________。有机物可以通过________的方法使其中的重要成分分离出来。
(3)e处点燃的气体是________,火焰的颜色是________色。
(4)下列叙述错误的是________。
A.煤发生了化学变化
B.d中液体显碱性
C.d中液体不分层
D.e处的气体可以还原氧化铜,也可以使溴水褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于可逆反应:aA(g)+bB(g)![]() cC(g)+dD(g) ΔH的有关图像如下:
cC(g)+dD(g) ΔH的有关图像如下:
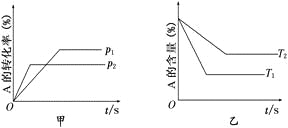
则下列不正确的是
A.p1<p2T1>T2
B.减小压强,正逆反应速率都减小,平衡右移
C.ΔH>0 ΔS>0
D.升高温度,混合气体的平均摩尔质量增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钼是一种过渡金属元素,通常用作合金及不锈钢的添加剂,这种元素可增强合金的强度、硬度、可焊性及韧性,还可增强其耐高温及耐腐蚀性能。如图是化工生产中制备金属钼的主要流程图。
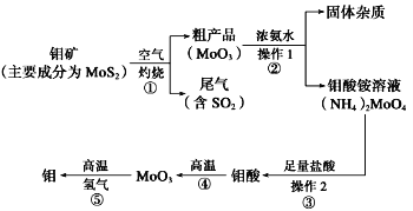
(1)写出在高温下发生反应①的化学方程_____
(2)生产中用足量的浓氨水吸收反应①的尾气合成肥料,写出该反应的离子方程式:___
(3)如果在实验室模拟操作1和操作2,则需要使用的主要玻璃仪器有_____
(4)某同学利用如图所示装置来制备氢气,利用氢气还原三氧化钼,根据要求回答问题:

①步骤⑤的化学反应方程式为___。请设计一个实验方案验证H2的还原性并检验其氧化产物,其装置连接顺序是____。
②在烧瓶A中加入少量硫酸铜的目的是__
③两次使用D装置,其中所盛的药品依次是_____、____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22。下列说法不正确的是
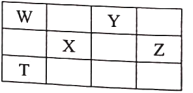
A.原子半径:r(X)>r(Z)>r(W)>r(Y)
B.单质Z2、Y3和Z与Y形成的化合物ZY2均可用于自来水消毒
C.X元素可形成两种或以上的单质,且在一定条件下可以相互转化
D.T元素的单质具有半导体的特性,其最高价氧化物对应水化物是一种强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 MnO2是一种重要的无机功能材料,工业上提纯粗MnO2(含有较多的MnO和MnCO3)实验工艺流程如下图,则下列说法不正确的是
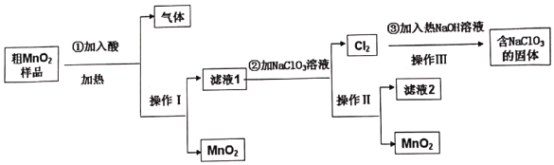
A.若①加入的是稀H2SO4,实际生产中可由滤液2进一步制得副产品Na2SO410H2O
B.操作Ⅲ是减压蒸发,理论上得到的固体NaCl和NaClO3物质的量之比为5:1
C.①加酸的目的是溶解MnO和MnCO3,实际生产可以用浓盐酸进行溶解
D.②反应的离子方程式:5Mn2++2ClO3-+4H2O=5MnO2↓+Cl2↑+8H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值。下列叙述正确的是( )
A.9g超重水(3H216O)含中子数为6NA
B.标准状况下,22.4L CCl4含有的分子数目为NA
C.常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA
D.一定条件下,将1mol N2和3mol H2混合,充分反应后转移的电子数为6NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com